抽象的
氧化剂/抗氧化不平衡涉及慢性阻塞性肺病(COPD)的发病机制。
目前的研究分别检测了抗氧化剂和促氧化酶,葡萄糖氧酶(HO)和诱导的一氧化氮合酶(INOS)的表达,在没有肺功能损伤的情况下严重COPD和对照吸烟者的患者。在外周肺中定量表达为硝基葡萄氨酸(N-TYR)的HO-1,HO-2,INOS和一氧化氮衍生氧化剂的免疫反应性。
与对照吸烟者相比,HO-1 +肺泡巨噬细胞在严重的COPD中降低,而在INOS +巨噬细胞中没有观察到差异。相比之下,严重的患者在肺泡壁中具有显着高的Inos +细胞。将这些InOS +细胞鉴定为2型肺细胞,它们的数量与HO-1 +巨噬细胞相反。两组之间的N-Tyr免疫染色没有显着差异。然而,肺术中蛋白质硝化率与InOS表达直接相关,并以较低/强制生命能力较低的价值呼气量。HO-2由2型肺细胞组成型表达,并且这些细胞在严重的COPD中增加。
总之,结果表明,涉及氧化胁迫响应的酶在肺部防御中可能具有不同的作用,并且其在慢性阻塞性肺病患者的严重损伤的发育中可能有关的这种不平衡。
由意大利大学和研究部,帕多瓦大学和阿里卡提供支持。
氧化剂/抗氧化剂不平衡涉及慢性阻塞性肺病的天球菌(COPD)1.外源氧化剂含有香烟烟雾,对COPD的主要危险因素,并由表征诊断的炎症细胞产生2.氧化应激诱导一种级联信号机制,它激活转录因子,导致促炎和抗炎细胞因子和酶的编码基因上调1.该研究侧重于这些酶中的两种,氧气氧酶(HO)和诱导型一氧化氮合酶(InOS)。HO,诱导型HO-1,组成型HO-2和HO-3的三种同种型,催化丙吡啶的降解,然后减少到胆红素,生产游离铁和一氧化碳(CO)3.-4..HO具有重要的抗氧化能力,在保护肺细胞免受氧化暴露方面具有重要意义。HO-1被证明是由多种伤害性刺激诱导的,包括活性氧(ROS)3..在一项较早的研究中,作者发现慢性吸烟者肺泡腔内HO-1和肺泡壁HO-2表达增加5..
一氧化氮(NO)合酶可能在COPD的发病和进展中发挥作用,因为NO具有直接的毒性作用,并与超氧化物反应,在细胞中产生毒性过氧亚硝酸盐6..有研究发现inos在间质性肺疾病中表达较多7..该酶在COPD发病和进展中的作用尚存争议8.那9..此外,大多数研究检测了诱导痰中的iNOS及其产物,而认为外周气道是COPD中气流限制的主要部位。研究COPD进展的机制可能被证明有助于识别易于肺功能快速下降的亚组受试者和靶向治疗干预。
目前的研究分析了具有抗氧化性质的酶(HO-1和HO-2)和促氧化性质的酶(iNOS)在COPD和严重肺功能损害患者外周血肺中的表达,并与具有类似吸烟史但肺功能未受损的受试者进行了比较。一氧化氮衍生氧化剂的参与是通过免疫染色的硝基酪氨酸加合物的蛋白质。定量肺泡巨噬细胞和肺泡壁中HO、iNOS和硝基酪氨酸的免疫反应性,结果与肺功能指标相关。
方法
主题
检查两组接受肺部切除肺部切除肺部外周癌或肺粪池的肺粪池肺粪池的受试者:11名受试者的吸烟病史> 20包和严重的固定气道阻塞(严重的固定气道)和13项受试者吸烟历史> 20包和正常肺功能,IE。强迫呼气量一秒钟(FEV1)/重要的容量(VC)超过预测值减去1.64残留SD(对照吸烟者)10.严重的气道阻塞被定义为FEV1/ VC小于预测值减去1.64残余SD和FEV1< 50% pred11.在严重COPD组的11个组织样本中,有9个来自接受LVRS的患者,而其余的样本来自癌症手术。
所有受试者均呈现出FEV的增加1吸入200μg的沙丁胺醇<15%后,与基线值相比。受试者没有加剧,没有祛痘症呼吸道感染,并且在手术前期内没有接受糖皮质激素或抗生素。它们对常见的过敏原提取物和过去的哮喘或过敏性鼻炎的历史进行了负皮肤测试。设计符合赫尔辛基的宣言,并为每个科目获得了知情的书面同意。
肺功能测试
在手术前一周内获得肺功能试验,包括肺活量测定血液气体分析和CO扩散能力12.在5名对照吸烟者中,在严重COPD Groupand中的两名患者中没有测量扩散能力。
免疫组织化学
组织块从副申请中取出,避免肿瘤所涉及的区域,固定并嵌入在其他地方的石蜡中13.用小鼠HO-1单克隆抗体(anti-HO-1;HO-2山羊多克隆抗体(C-20, sc-7697;SantaCruz Biotechnology, Inc., SantaCruz, CA, USA),与碱性磷酸酶抗碱性磷酸酶(apap)方法(Dako Ltd, High Wycombe, UK)或链霉亲和素生物素化碱性磷酸酶复合物(StreptABComplex/AP;分别Dako有限公司)。抗iNOS单克隆抗体(sc7271;Santa Cruz Biotechnology, Inc.)用Envision+TM (K4000, Dako Ltd)方法和二氨基苄啶(DAB)染色处理。仅与二抗孵育的非特异性结合的阴性对照进行处理,没有显示信号。用兔多克隆抗体(抗3-硝基酪氨酸;Upstate Biotech, Lake Placid, NY, USA),其次是过氧化物酶结合猪抗体(P399; Dako Ltd) and DAB. Positive controls were processed incubating slides with 1 mM NaNO2和1毫米H.2O.2在暴露于初生抗体之前在100mM乙酸盐缓冲液中。阴性对照在使用前用1mM硝基甲胺孵育培育初生抗体。
在支气管上皮,肺部血管,肺泡壁和肺泡巨噬细胞中使用光学显微镜(Zeiss,Oberkochen,Germany)以盲目的放大来检查免疫染色。如其他地方所述,在肺泡巨噬细胞和肺泡壁上定量HO-1,HO-2,INOS和N-Tyr染色5..简单地说,每个切片随机选取至少20个肺实质高倍场,评估肺泡内至少100个巨噬细胞。使用光学显微镜(Leica DMLB;徕卡,剑桥,英国),连接到一个录像机,录像机连接到一个计算机图像系统。
进行双免疫染色以确定对HO-1,HO-2和INOS呈积极染色的细胞型。研究了CD68(巨噬细胞)和表面活性剂蛋白(SP)-B(SP)-B(2型肺细胞) - 阳性细胞。载玻片用抗体抗CD68(山羊多克隆SC-7083,Santa Cruz Biotechnology,Heidelberg,德国Ormouse Monoclonal M814,Dako Ltd)或抗SP-B(Politonal兔抗体礼物,帕提莫斯大学)意大利)14和抗HO-1,抗HO-2或抗INOS5..通过进行双染色来获得控制载玻片,其中未加入其中一种原代抗体。
结果
Table 1⇑显示检查受试者的特征。两组受试者与年龄和吸烟史类似。严重的COPD表现出较低的动力氧张力值(P <0.001),CO差异(P <0.001)和扩散系数(P <0.01)。根据慢性阻塞性肺病(金)分类的Global倡议16,在严重的COPD组中,六分为III阶段的阶段IIB和五名患者。
重度COPD患者肺泡巨噬细胞计数(中位数154(四分位数143-174))与对照组(157(142-204))无显著差异。肺泡腔内大部分被计数为肺泡巨噬细胞的细胞cd68阳性(70.2%(55.4-83.8))。HO-1免疫染色主要见于肺泡间隙细胞,而在支气管上皮和血管中则为阴性(图1)⇓).肺泡空间中的大多数HO-1阳性细胞为CD68阳性(82.6%(72.4-88.9))。与对照吸烟者相比,HO-1阳性肺泡巨噬细胞的百分比显着降低(26.0%(12.3-32.6))(44.1%(34.7-57.5); P <0.01;表2⇓,图2⇓).iNOS+的百分比(图2)⇓)和N-Tyr+巨噬细胞在两组间无差异(表2)⇓).
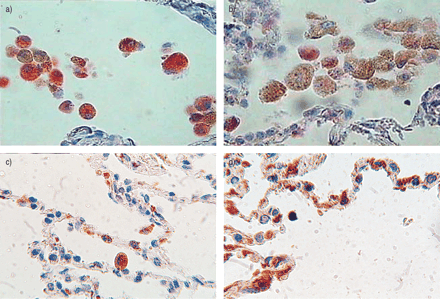
人肺手术标本的免疫组织化学研究。a)在对照吸烟者中染色氧气氧酶(HO)-1的肺泡空间。b)在严重的慢性阻塞性肺疾病(COPD)患者中染色的HO-1染色的肺泡空间。c)在对照吸烟者中用于诱导型一氧化氮合酶(InOS)的肺泡壁。d)在严重的COPD受试者中染色的肺泡壁。使用抗人HO-1抗体和碱性磷酸酶 - 抗碱性磷酸酶(APAAP)方法对免疫组织化学进行免疫组织化学,用快速红色(A,B)或抗人INOS抗体和与过氧化物酶结合的Envirision二抗产生的方法进行免疫组织化学方法用二氨基苯并(C,D)。所有部分都用血红素染色。
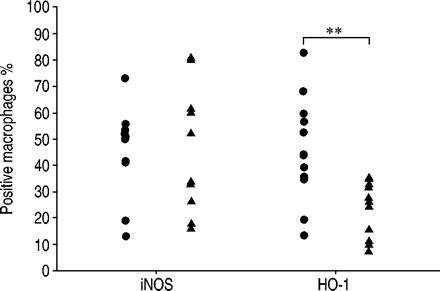
对照吸烟者(•)和严重慢性阻塞性肺疾病(Ⅵ)的诱导型一氧化氮合酶(InOS)和碘氧酶(HO)-1阳性肺泡巨噬细胞的单个值的比较。**:P <0.01。
HO-2的免疫染色于肺泡巨噬细胞,在肺泡壁,平滑肌和肺动脉的外膜细胞中存在,以及在支气管壁的几个细胞中。两组(COPD 75.4%(54.2-88.1)中相似的HO-2免疫染色的HO-2免疫染色的百分比相对控制67.9%(35.9-75.6))。严重COPD中肺泡壁中的HO-2阳性细胞的数量显着高(P <0.01)(18.0个细胞·mm-1(12.7-22.8)),而对照组(11.3细胞·mm)-1(10.6-12.2)))(表3⇓,图3⇓).双免疫染色表明,肺泡壁的HO-2阳性细胞均为2型肺细胞(92.3%(88.6-93.9))。相反,97%(93-98%)2型肺细胞是HO-2阳性。
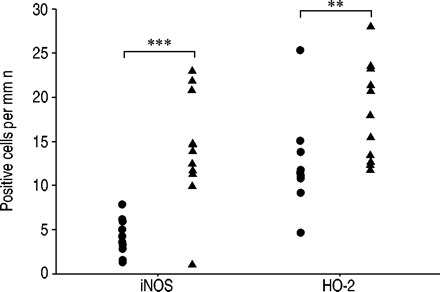
对照吸烟者(•)和严重慢性阻塞性肺疾病(▴)肺泡壁诱导型一氧化氮合酶(iNOS)和血红素加氧酶(HO)-2阳性细胞个体值的比较* *: p < 0.01;* * *: p < 0.001。
Inos染色在肺泡壁和肺泡巨噬细胞中存在,平滑肌,在肺动脉和支气管壁的外膜中。严重COPD(13.9个细胞·mm)的肺泡壁中的INOS阳性细胞的数量显着增加-1(11.4-19.2))关于对照吸烟者(4.2个细胞·mm-1(2.3-5.9);P <0.001;table 3⇑,图3⇑).双免疫染色显示,大多数inos阳性细胞对SP-B有免疫反应(85.7%(63.9 ~ 87.8)),为2型肺细胞。重度COPD患者肺泡壁N-Tyr染色程度明显大于吸烟对照组,但差异无统计学意义(p=0.07,表3)⇑).将两组在一起,在肺泡壁中的免疫反应性之间存在正,线性相关性(RHO = 0.54,P <0.05)。在InOS +巨噬细胞和N-TYR +巨噬细胞之间观察到类似的关系(RHO = 0.41,P = 0.06)。肺泡壁中的InOS +细胞与阳性相关的与阳性巨噬细胞相反(Rho = -0.44,P <0.05)。
在肺泡壁中的N-TYR免疫染色与FEV相反1/迫使生命能力(FVC)(RHO = -0.62,P = 0.05)在对照吸烟者中,并且在严重COPD组中显示出相同的趋势(RHO = -0.60,P = 0.07)。在两组患者的HO-1,HO-2,INOS和肺功能参数或吸烟历史之间没有检测到显着的关系。
讨论
本研究发现,在严重的COPD中,在肺泡巨噬细胞中被引起的HO-1表达,而表达INOSAND HO-2的2型肺细胞的数量增加。肺组织中的蛋白质硝化率与INOS的表达直接相关,并与FEV的较低值相关1/ FVC比率。
氧化应激和对宿主防御机制的不平衡涉及COPD的发病机制1.氧化剂,无论是由炎症细胞吸入还是产生,诱导肺部炎症反应通过信令机制。已经显示氧化还原转录因子,例如核因子-κB和活化剂蛋白1,在氧化应激期间在上皮细胞和炎性细胞中被驱动,导致许多抗炎基因的上调,包括这些编码对于HO-1和INOS1.对HO-1和INOS的功能意义尚不清楚,因为它们的活性可能导致保护或损伤,这取决于实验设置17那18.
过度生产没有通过INOS可通过与超氧化物阴离子和氧气的反应对肺组织产生不利影响,从而导致活性氮物质的发展19.通过其产物CO、铁和胆红素,HO被认为在细胞保护中具有抗氧化损伤的作用3..两个HO,HO-1和HO-2,具有差异的角色,只能互相替换20..在之前的一项研究中,本文作者在健康受试者和吸烟者的肺中发现了这两种亚型的不同定位,HO-1在巨噬细胞中占优势,而HO-2在肺实质中占优势,特别是在2型肺细胞中5..检测到HO-1和HO-2的类似分布,insevere COPD患者,表明炎症过程和重塑的进展不会改变这些酶的定位。
HO-1的表达在患有结节病和间质肺炎患者的肺泡巨噬细胞中最突出的,而HO-1免疫反应性在支气管上皮,肺泡上皮和内皮中是非常低的21.这与本研究中外周肺样本中的HO-1定位一致,并与哮喘较大气道中的HO-1阳性支气管上皮细胞进行造影22.在一起,这些观察结果表明HO-1在支气管上皮细胞中的表达依赖于检查支气管树的部位。
目前的作者以前表明,吸烟者的HO-1和HO-2表达增加了,但在健康吸烟者和轻度COPD的吸烟者之间没有发现差异5..通过研究更严重的COPD患者,包括高度明确破坏的患者,当前作者观察到肺泡巨噬细胞的HO-1表达降低,HO-2 + 2型肺细胞数量增加。如上所述,HO-1基因启动子多态性可降低ROS的HO-1的诱导性23从而导致卷烟烟雾造成不同的易感性。目前的调查结果证实了HO-1减少和COPD严重程度之间的关系。虽然吸烟者相对于非吸烟者表现出更高的HO-1水平,因此表明严重COPD的患者可能对抗烟雾损伤的主动防御机制可能对抗氧化应激的防御受损,尽管他们的吸烟历史与对照吸烟者不同。何的改变表达也可能是疾病的结果。由于HO-2是组成酶,并且结果仅通过2型肺细胞在肺泡壁中在肺泡壁中表达,因此其增加可以反映肺中这些细胞数量的增加。事实上,肺细胞增殖可以通过香烟烟雾诱导,尽管有破坏性过程,但是在严重的COPD中可能检测到肺泡壁增厚24那25.肺中HO组成形式的作用仍未确定。根据本作者的结果,HO-2可以防止INOS产品青睐的过量蛋白质硝化。
这是具有COPD的外周血肺组织中INOS的第一研究。以前在正常的气道上皮,哮喘,间质肺炎和粒状肺病中记录了人肺中InOS的表达。7.那26.-28..目前的研究结果对INOS的免疫反应性的结果与先前的报告一致,其显示肺细胞中酶的广泛分布,包括上皮,血管和炎症细胞29.那30..通过检测肺泡巨噬细胞,本研究证实了之前的发现,COPD受试者和健康受试者的痰巨噬细胞中iNOS表达相似8.那9..然而,在肺的实质隔室中,目前的研究检测了严重COPD的2型肺细胞中的含量较高。在人类肺部中的INOS的舱室是一致的,与大鼠的观察结果一致31..虽然巨噬细胞通常被认为是宿主防御的主要细胞介质,但大鼠2型肺细胞表达iNOS并释放类似肺泡巨噬细胞水平的NO。目前的研究结果与2型肺细胞与上皮细胞和巨噬细胞一起作为抵御肺损伤的第一道防线的假设是一致的32.,并且它们的功能对于被肺气肿破坏的肺组织可能是至关重要的33..
在超氧化物阴离子的存在下,INOS产生的过量否,促进蛋白质酪氨酸残基的硝化。酪氨酸硝化严重依赖于NO和分子环境的浓度19.文献中关于iNOS产物作为NO的作用的数据是相当矛盾的。与对照组相比,COPD受试者的呼出NO水平更高、更低或相似,呼出NO与FEV呈正相关或负相关1已经汇报过8.那34.那35..对于健康对照的COPD患者的痰,硝基吡氨酸阳性细胞更频繁8..本作者能够在严重COPD中确认后者在肺泡壁中发现后一种发现,但不在肺泡巨噬细胞中。此外,本作者的数据表明,肺组织中蛋白质的硝化可能对肺功能产生不利影响。两项研究之间的实质性差异使得难以比较结果。事实上,在ichiinose的研究中,跨越的严重程度更温和等等。8.检查呼吸道的隔间是不同的。此外,免疫组织化学技术不适用于氮化蛋白的定量评价。
肺组织中HO-1与iNOS的负相关关系可能与二者的调控相互作用有关。HO通过降解酶的组成成分haem和CO的抑制作用下调iNOS36..HO-1的降低可能会增加血供,促进iNOS的合成和最优活性,并促进促氧化副产物的形成,即由iNOS活化而产生的NO。相反,NO对HO-1信使核糖核酸具有稳定作用体外37.,这将上调HO-1。除了不,缺氧和肿瘤坏死因子-α可以作为HO-1诱导剂存在。然而,目前的结果表明,严重的患者无法通过增加HO-1的表达来响应这些刺激。
本研究中的潜在偏见对手术切除的标本进行了,所有对照吸烟者患有11种严重COPD中的肺癌患者九个患者没有,并且癌症本身的存在可能会影响结果。对HO-1表达和肺癌没有研究,同时患有原发性肺癌患者的USOS的上调38..如果是这种情况,在两个更高级患者组之间的表达差异甚至更大。另一个潜在的偏见是,在LVRS中,外科医生选择肺的最糟糕部分,这可能会夸大病理发现关于疾病的功能分类。在可用于组织学分析的组织中没有检测到明显的差异(肺泡壁的长度和肺泡巨噬细胞的数量),并且在两种严重COPD患者之间的免疫反应性计数中,两种严重的COPD患者和肺癌的剩余九个患有LVRS。然而,对于可靠细胞计数的对肺泡壁完整性的需求可能已经阻止了从不适合分析的LVRS评估某些组织的组织。
总之,目前的研究表明,两种酶响应于慢性阻塞性肺病中的氧化胁迫诱导的诱导型外周肺部。碘氧酶-1的免疫反应主要在肺泡巨噬细胞中检测,而诱导型一氧化氮合酶的免疫反应性在2型肺细胞中局部化。结果表明,这些酶可能在肺部防御中具有不同的作用,并且碘氧酶-1和诱导型一氧化氮合酶之间的不平衡可以与慢性阻塞性肺病患者的重担的发展有关。
致谢
作家感谢A. Baritussio用于表面活性剂蛋白-B的抗体的良好礼物,以及G. Fulgeri进行秘书辅助。
- 已收到2002年的10月25日。
- 公认2003年2月28日。
- ©ers Journals Ltd