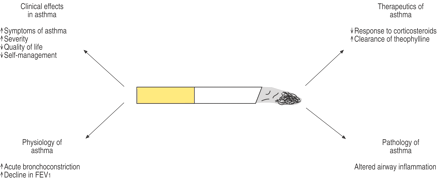
数据

意味着(95%置信区间)变化最大呼气流量(PEF;L·敏−1)在不吸烟和吸烟的哮喘病人,治疗后吸入安慰剂(□)或丙酸(└;1000天µg·−1)。#:p = 0.016,比不吸烟者afterplacebo;* * *:p = 0.001,大于吸烟者fluticasone之后。复制与许可40。
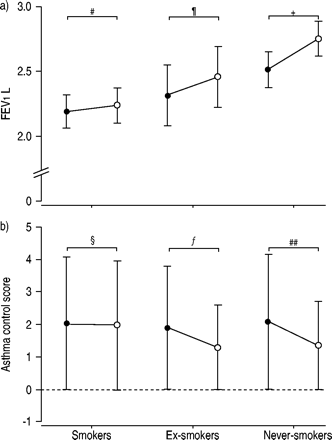
平均差(95%置信区间)后安慰剂(•)和强的松(○)与哮喘,吸烟与哮喘抽过烟,不吸烟者与哮喘)变化在一秒用力呼气量(FEV1),和b)哮喘控制分数。分数的减少意味着改善哮喘控制。#:p = 0.605;¶:p = 0.386;+:p = 0.019;§:p = 0.865;ƒ:p = 0.108;# #:p = 0.04。复制与许可41。
糖皮质激素的抗炎作用是激活介导的胞质糖皮质激素受体配体依赖性转录因子(GRs)作为,把入核抑制或诱导糖皮质激素靶基因。GR-α行为通过直接绑定到DNA序列(transactivation)或与促炎作用转录因子(transrepression)。GR-β不结合配体,主要位于细胞核,不能transactivate glucocorticoid-sensitive基因。皮质类固醇的潜在途径和机制抵抗哮喘的吸烟者包括以下:1)皮质类固醇药物动力学,如。气道黏膜渗透性增加,支气管分泌物增加;2)皮质类固醇和β2(β肾上腺素能受体2基于“增大化现实”技术)交互,如。下调的β2基于“增大化现实”技术的功能;3)炎性细胞表型,如。增加气道嗜中性粒细胞或CD8 +淋巴细胞的数量,减少气道嗜酸性粒细胞数量;4)细胞因子和介质的水平,如。增加产量的白介素(IL) 4,引发,肿瘤坏死factor-α,降低IL - 10的生产,增加nitrosative压力;5)GRs,如。GR-αGR-β的过度表达,减少表达;6)炎性转录因子激活,如。核factor-κB (NF-κB),激活蛋白1、信号transduction-activated因素;和7)皮质类固醇细胞信号传导系统,如。减少组蛋白脱乙酰酶(HDAC)活动,增加p38增殖蛋白激酶活性。帽子:组蛋白乙酰转移酶。
表
-
表1 -
皮质类固醇的潜在机制抵抗哮喘的吸烟者
皮质类固醇药物动力学 增加气道黏膜渗透性 增加支气管分泌物 皮质类固醇和β2肾上腺素能受体的相互作用 下调的β2肾上腺素能受体的功能 炎症细胞表型 气道中性粒细胞或CD8 +淋巴细胞数量增加 减少气道嗜酸性粒细胞数量 细胞因子和介质的水平 增加产量的il - 4、引发TNF-α 降低il - 10的生产 Nitrosative压力 GR 过度的GR-β 减少表达GR-α 促炎转录因子激活 过度的NF-κB 过度的激活蛋白1 过度的信号transduction-activated因素 皮质类固醇细胞信号传导系统 组蛋白脱乙酰酶活性降低 p38增殖蛋白激酶活性增加 IL:白介素;肿瘤坏死因子:肿瘤坏死因子;格:糖皮质激素受体;尼克-弗瑞:核转录因子
-
表2 -
潜在的药物治疗哮喘的吸烟者
长效β2受体受体激动剂 结合吸入型皮质类固醇激素 茶碱 新糖皮质激素受体受体激动剂 选择性phosphodiesterase-4抑制剂 中介拮抗剂 白三烯受体拮抗剂 Histamine-H1受体拮抗剂 - 2受体阻滞 TNF-α,LTB4,引发拮抗剂 其他抗炎治疗 IFN-α il - 10受体激动剂 增殖蛋白激酶的抑制剂 NF-κB抑制剂 大环内酯物抗生素 诱导一氧化氮阻滞剂 抗氧化剂 IL:白介素;肿瘤坏死因子:肿瘤坏死因子;LTB4B:白三烯4;干扰素:干扰素;尼克-弗瑞:核转录因子