摘要
先天性肺淋巴管扩张症(CPL)肺淋巴结构的异常生长发育导致严重缺氧。
本案例研究旨在确定一氧化氮合酶在cpld中的细胞来源和地形分布事后剖析1例有临床病程及CPL组织学表现的足月新生儿组织和3例无肺部病理的对照组。
结果发现,与对照组相比,CPL患者肺动脉和淋巴结构内皮细胞的内皮型一氧化氮合酶蛋白染色明显增多。
作者认为先天性肺淋巴管扩张症中血管内皮细胞和淋巴内皮细胞中内皮型一氧化氮合酶的合成上调。
先天性肺淋巴管扩张症(CPL)是一种罕见的新生儿疾病,最早由R. Virchow在150年前提出1,2.先天性肺淋巴管扩张是本病的主要特征,并已根据其在其他器官的存在和相关畸形的存在进行分类3..在大多数情况下,紫绀在出生后不久就会出现,但在单侧出现的情况下,诊断可能会延迟几周4.如果双肺都受到影响,死亡率会更高5,早期胎儿体征可为非免疫性胎儿积液6.先天性异常(心脏和肾脏)在50%的CPL病例中有报道51例因胸导管发育不全引起CPL7.虽然主要是一种足月新生儿的疾病,但CPL可出现在早产婴儿中,并可发生自然缓解8.
本研究对足月新生儿CPL的一氧化氮合酶(NOS)、内皮性NOS (eNOS)、诱导性NOS (iNOS)和神经元性NOS (nNOS)进行免疫组化染色。
材料与方法
病例报告
用胞浆内精子注射法诱导37岁初生婴儿怀孕;怀孕的过程非常顺利。自然阴道分娩发生在41周后,产妇或新生儿感染的特定危险因素均不存在。羊水量及胎盘肉眼形态正常。脐带血pH为7.27,出生体重为3400 g, 1、5、10 min时APGAR为8/8/8,未见明显畸形或畸形体征。最初的紫绀和心动过缓在产后持续存在;用100%氧气进行气囊和面罩通气,两者都没有明显改善。新生儿转运组到达时,婴儿处于100%含氧鼻咽持续气道正压状态;脉冲氧饱和度测定的最大经皮氧饱和度为50%。气管插管后心率恢复正常,氧饱和度未改善至>60%。 The latter stayed at this level during transport to the neonatal intensive care unit (Dept of General Paediatrics, Heinrich-Heine-University, Düsseldorf, Germany) and respiratory parameters were as follows: peak inspiratory pressure 2.5 kPa, positive end-expiratory pressure 0.5 kPa, rate 63·min−1吸气氧分数1.0。此阶段胸片显示双侧不均匀、条纹状浸润及左侧小气胸。超声心动图显示心脏解剖正常,并以严重的三尖瓣功能不全为量化,显示明显的肺动脉高压。治疗包括抗生素治疗、通气、吸入一氧化氮(NO;高达35ppm),体积膨胀,碳酸氢钠和儿茶酚胺。尽管高剂量儿茶酚胺可导致足够的血压和持续输注碳酸氢钠,但呼吸性和代谢性酸中毒增加。诊断为左侧张力性气胸,经胸管缓解。出生9小时后发生终末期心动过缓,对儿茶酚胺治疗无反应,婴儿死亡。尸检报告为局限于肺部的囊性CPL。
控制
对照对象从死于婴儿猝死综合征的婴儿中选择,并在洪堡大学(Charité Virchow医院,柏林,德国)的paidopology和胎盘学系进行尸检。没有一名婴儿被医务人员复苏,没有任何治疗干预措施(如。机械通气),也没有任何婴儿肺部感染的证据。
控制1
15岁初生婴儿,母亲吸烟。足月婴儿出生体重为3,000 g, APGAR为9/10,动脉动脉pH值为7.29。死亡前10天出现腹泻。婴儿在出生第73天死亡。
控制2
22岁初生婴儿,有吸烟史。足月婴儿出生体重为2740克,APGAR为8/10,动脉动脉pH值为7.24。婴儿在出生第86天死亡。
控制3
一位24岁的母亲第二次怀孕所生的婴儿,有吸烟史。分娩时间为妊娠39周,婴儿出生体重为2610克,羊水中有胎粪染色,APGAR为9/9,动脉脊髓pH为7.29。8周龄出现口腔和皮肤局部真菌感染。婴儿在出生第137天死亡。
免疫细胞化学方法学
肺组织以石蜡包埋组织块的形式提供。切下切片(4µm),再水化,然后通过微波压力烹饪或胰蛋白酶孵育回收抗原。对切片进行处理,以阻断一抗和二抗的非特异性结合以及先前描述的与发色剂的非特异性反应9.然后将切片与特异性抗体在室温下孵育60分钟。N30020, BD传感器,列克星敦,肯塔基州,美国;1:200;前处理为压力蒸煮。伊诺:猫。不。N32020, BD转导;1:50 0;前处理为压力蒸煮。 nNOS: Cat. No. 610308, BD Biosciences, Oxford, UK; 1:400; pre-treatment was pressure cooking. Nitrotyrosine: Cat. No. 06-284, Upstate Biotechnology, Lake Placid, NY, USA; 1:200; pre-treatment was trypsin incubation). Nitrotyrosine staining was included in order to verify whether or not sufficient NO was formed to induce the formation of peroxynitrite, as indicated by tyrosine nitration. Bound antibody was detected using goat anti-mouse immunoglobulin G conjugated with horseradish peroxidase using a streptavidin-biotin link and visualised with diaminobenzidine. In negative controls, the primary antibody was replaced with pre-immune serum. Sections were counterstained using haematoxylin and viewed by light microscopy.
内径<250µm的血管被认为是小肺动脉,>250µm的血管被认为是大肺动脉。
结果
内皮型一氧化氮合酶
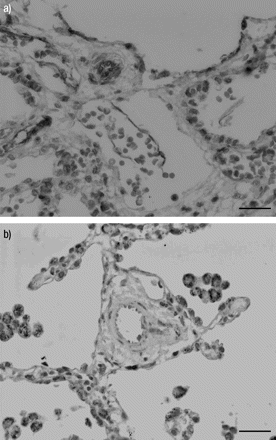
中等大小的肺动脉和较小的肺动脉分支中发现eNOS内皮细胞呈中度阳性(图1a)⇓),后者通常为阴性的eNOS。一些扩张的淋巴管内皮也有轻度阳性染色。
a)先天性肺淋巴管扩张症患者石蜡包埋肺组织样本内皮型一氧化氮合酶(eNOS)的苏木精和伊红染色免疫组化显示,在显微照片顶部,扩张的淋巴管内皮内衬染色呈阳性。在淋巴通道正下方可见突出的小肺动脉分支,内皮细胞呈强阳性。血管壁较薄的血管通道内皮阳性和一些非特异性红细胞阳性也存在于其他地方。b)对照组婴儿eNOS的苏木精和伊红染色免疫组化显示非常轻微的阳性染色,仅小肺动脉内皮内衬。比例尺= 100 μm。
在对照组中,在大动脉的内皮中有轻微的阳性,但在小动脉中没有可见的阳性(图1b⇑).
诱导型一氧化氮合酶
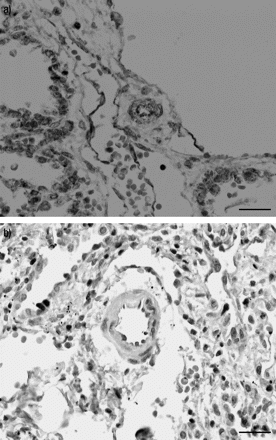
在中、小肺动脉分支中可见轻度至中度内皮阳性,也可见一些平滑肌染色(图2a⇓).一些扩张的淋巴通道显示轻度内皮阳性,尽管在一些区域内皮衬里已经丢失。支气管上皮细胞中呈中度阳性,肺泡内膜细胞中呈轻度阳性。
a)先天性肺淋巴管扩张症患者石蜡包埋肺组织样本的诱导型一氧化氮合酶(iNOS)苏木精和伊红染色免疫组化显示,位于图像右上方并垂直蜿蜒穿过图像中心的扩张淋巴通道内皮内衬染色呈阳性。夹在它们之间的是一个突出的小肺动脉分支,显示内皮阳性。左侧和右下方可见阳性的肺泡内膜细胞。b)对照组小肺动脉苏木精和伊红染色显示iNOS无明显阳性。肺泡内巨噬细胞阳性。比例尺= 100 μm。
对照组有相似的染色模式,因此与对照组相比,CPL中iNOS没有整体上调(图2b⇑).
神经元型一氧化氮合酶
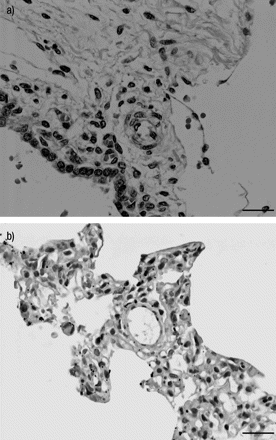
淋巴和肺动脉结构在患者和对照组中都没有令人信服的阳性染色(图3a⇓b).两组气道上皮均检测到nNOS。
a)先天性肺淋巴管扩张症患者石蜡包埋肺组织样本中神经元一氧化氮合酶(nNOS)的苏木精和伊红染色免疫组化仅在呼吸道上皮细胞中显示轻度阳性。小肺动脉分支示阴性。b)对照组小肺动脉苏木精和伊红染色,免疫细胞化学检测nNOS阴性。比例尺= 100 μm。
讨论
在一名患有cpld的新生儿中,小、中型肺动脉内皮细胞可诱导eNOS合成。该患者扩张淋巴结构的内皮内层也可诱导eNOS合成。据作者所知,这是新生儿CPL中NOS酶家族免疫组化结果的第一篇报道。
虽然并不都是致命的疾病10- - - - - -12新生儿双侧CPL的表现与肺气体交换的严重损害以及高死亡率相关。无论是临床表现还是手术时的宏观观察,都不能明确区分CPL和先天性大叶肺气肿13或CPL与肺淋巴管瘤之间14.淋巴管扩张的肺外表现不一定与更好的肺气体交换有关15.最近,作者发现eNOS在新生儿快速进行性肺动脉高压(RPPHN)患者中表达上调。9.在RPPHN和CPL中,缺氧都可能是eNOS上调的触发因素。RPPHN和CPL之间关于eNOS上调的主要区别是时间轴:而RPPHN的婴儿在活检或尸检时已经几周大了,而CPL的婴儿只有9小时大。在目前的情况下,eNOS早期上调的一个可能的解释可能是缺氧程度。本例患者动脉氧分压为1.2-3.2 kPa,因此低于正常胎儿子宫内氧水平(3.6-4.7 kPa)。16.
第二个有趣的发现是淋巴内皮细胞中eNOS的表达,这在cpls中是非常突出和致病的在体外研究建立了微淋巴管的研究模型17并提供了淋巴内皮细胞产生NO的证据18.根据刺激的类型(钙离子载体或脂多糖),NO的产生是由eNOS或iNOS上调介导的19.在活的有机体内对C57BL/6小鼠的研究表明,eNOS影响淋巴液流动,但不影响初始淋巴管的直径20..淋巴流动受收集淋巴和流出阻力程度的调控,而流出阻力受eNOS的调控。
iNOS的上调似乎不是cpld的特征。在肺动脉高压大鼠模型中,iNOS的最初上调在几天后消退,而eNOS的上调则是主要的发现21.
虽然有理由相信NO处理不影响eNOS表达,但不能排除这种可能性。至少在肺动脉高压大鼠模型中,向研究气体中添加NO并没有改变肺eNOS的表达22.
现阶段只能推测血管内皮细胞和淋巴内皮细胞中内皮型一氧化氮合酶的上调对由此引起的缺氧程度的影响。在血管内皮细胞的情况下,一氧化氮的形成会导致血管舒张,降低血管阻力,增加肺血流量和改善氧合。肺淋巴血管舒张可能意味着更少的流出阻力,改善肺部淋巴液的清除,并再次改善氧合。至少在目前的情况下,即使通过吸入方式添加外源性一氧化氮也不足以逆转严重缺氧,也不足以防止严重酸中毒和最终死亡。
致谢
作者非常感谢H. Müntefering在建立先天性肺淋巴管扩张症组织学诊断方面的支持。他们还要感谢a·a·普雷斯顿对标本的免疫组化制备和染色。
- 收到了2005年7月15日
- 接受二零零五年十一月五日。
- ©ERS期刊有限公司