摘要
进展性肺疾病决定囊性纤维化(CF)患者的发病率和死亡率。
CF肺部疾病的特点是支气管发炎持续的细菌感染和呼吸道嗜中性粒细胞的持续积累。活化的或嗜中性粒细胞坏死的蛋白酶释放到肺的微环境的结构,细胞和可溶性组件造成损坏。
在通过气道细胞释放的各种蛋白质中,Elastase术被认为在CF肺病中发挥着重要作用。基于该概念,已经开发了几种治疗方法以抑制自由弹性活性,包括小型合成化合物,半合成抑制剂和自由弹性蛋白酶的天然抑制剂。
本综述总结和讨论了抑制气道蛋白酶在囊性纤维化肺病中的病理生理学理由,方法的要求和临床意义。
尽管有各种治疗性进展,> 90%的囊性纤维化(CF)患者仍然因呼吸衰竭而死。大多数CF患者的气道慢性感染细菌病原体,特别是铜绿假单胞菌1.因此,大量的中性粒细胞在CF气道中积聚,导致持续的内核炎症2.然而,气道炎症的持续时间和强度似乎比去除违规病原体所需的要明显得多。这种过度的炎症反应可能与CF跨膜电导调节剂(CFTR)基因中的引起疾病突变有关。然而,所涉及的确切致病机制尚未完全阐明。增加粘液粘度,局部宿主防御障碍,似乎有缺陷的局部宿主防御和先天性和自适应免疫机制。其他机制,例如由突变的CFTR产生的功能的增益,导致增强的内质网应激应激响应和促炎活动也可能起到作用3..结果,CF Airways表现出对肺部造成伤害的持续炎症,导致由慢性气道破坏和重塑引起的不可逆的侧支损伤。
尽管有一些病理生理学证据支持CF气道中压倒性的促炎反应的概念2,只有少数临床研究成功地建立了CF肺病患者的抗炎策略,例如布洛芬的应用4- - - - - -6和重组人类dnase7.其他研究表明,涉及吸入类固醇的方法不良副作用的效应或发生8白三烯(LT)B4拮抗剂9.在临床试验中评估抗炎治疗的一个主要困难仍然是选择合适的结果指标(表1)⇓)。可能的结果参数包括肺功能(肺泡),支气管肺泡灌洗(BAL)流体(BALF)分析,痰分析,痰微生物学,胸部计算断层扫描(CT),婴儿和幼儿肺功能等测量通过肺部清关指数,肺部爆发,寿命质量评估,气溶胶沉积和临床症状分数。根据表1所示,应根据临床试验的阶段考虑各种结果措施⇓.表1中给出的参考文献⇓表明已使用的相应成果的措施研究。
传统的肺结果,如一秒用力呼气量(FEV)1),反映肺功能的主要变化,但不宜监测较细微的变化。因此,新的结果参数,如CT扫描结果,可能变得越来越重要,但仍需要更广泛的验证。其他结果指标,如恶化率或生活质量,可能有助于监测CF患者的肺部疾病,在进行临床研究时应予以考虑。血液、痰或尿液中的炎症结果标记物已被证明对抗生素治疗的评估特别有帮助20.- - - - - -22..
因此,对于临床研究人员来说,定义和仔细评估结果指标,以监测气道炎症和调查抗炎干预对CF肺疾病患者的影响仍然是一个持续的挑战。关于CF临床试验结果测量的更广泛的讨论,请参阅以前的综述23..
CF Airways中的蛋白酶 - 抗滴油性不平衡
以往的研究表明,CF气道液中含有大量的促炎介质,特别是白细胞介素(IL)-8,它吸引大量中性粒细胞进入气道24..这应该提供针对细菌病原体的初始免疫防御系列。然而,募集的气道中性粒细胞似乎无法清除局部病原体,而是累积,经历二次坏死,并释放其细胞内部件,例如丝氨酸蛋白酶。丝氨酸蛋白酶在细胞内的生理上很重要25.,26.和细胞外/细胞外杀伤,最近通过鉴定中性粒细胞胞外陷阱捕获细菌,促进病原体与释放的蛋白酶的密切相互作用,最终导致细菌杀伤27.- - - - - -30..
在慢性疾病条件下,蛋白酶的数量超过了抗蛋白酶的中和能力。慢性肺病的蛋白酶-抗蛋白酶失衡假说提示下呼吸道蛋白酶水平是肺损伤和肺气肿的主要决定因素31..这一假说是由调查结果证实,在患有慢性支气管炎和肺气肿疾病的严重程度呈正相关,肺蛋白酶负荷和负相关抗蛋白酶屏蔽32..
在CF患者中,一些研究已经发现,一方面和组织损伤和疾病的严重程度的蛋白酶之间的相关性的其它33.- - - - - -36..已经证明了CF气道流体中的局部蛋白酶 - 抗促释放酶不平衡,其年龄为1岁,并且其后可能持续维持33..由于CF患者表现出正常的血清和支气管肺泡水平,因此CF呼吸道中的蛋白酶 - 抗调节酶不平衡可能不是由于内在的CFTR相关的缺乏脱发缺乏缺乏鼻窦和支气管肺泡水平的抗滴发33..
通过破坏中性粒细胞释放的各种蛋白质中,人白细胞弹性蛋白酶(HLE)被认为是对周围肺部微环境造成伤害的主要因素37..可用的少量数据表明,CF痰液中绝大多数的弹性蛋白溶解活性可归因于中性粒细胞衍生的HLE,以每分钟每毫升溶液中降解的弹性蛋白的微克来评估。因此,HLE的活性占90%,蛋白酶3占7%,巨噬细胞释放的可溶性介质占70%P.铜绿假单胞菌-衍生蛋白酶,占3%38..然而,非常难以直接比较不同中性粒细胞衍生酶的各种蛋白水解活性,因为目标结构的相关性和空体内的不同微型组分未知。自由漏光降解了几种细胞外基质组分,例如弹性蛋白,胶原蛋白,蛋白花糖,纤连蛋白和其他蛋白质,从而导致肺组织破坏31.,39.- - - - - -43.此外,HLE还能灭活金属蛋白酶(TIMP)和弹力蛋白(elafin)44,进而放大整体蛋白水解活性原位.为了更广泛地讨论HLE功能,应参考以前发布的评论45- - - - - -48.
在持续的CF肺疾病中,建立了延长的支气管内蛋白酶活性(PEPA)。之所以选择这个词,是因为与急性肺疾病不同,急性肺疾病中也可以观察到细胞外蛋白酶活性暂时升高,而CF中的蛋白酶-抗蛋白酶失衡持续一段时间,从而延长。经新生儿筛查和定期随访确诊的CF患儿经BAL检查发现,PEPA在CF气道中非常早出现15.,49.这些研究表明炎症和感染之间的密切关系。然而,肺部感染和气道炎症之间的致病序列仍然不完全理解。特别是,脂肽的纵向过程以及抗生素或非抗生素治疗对脂肽的影响尚未表现。
PEPA灭活可溶和肺免疫系统的细胞成分
除了持续不清楚的问题外,胃蛋白酶造成危害肺的各种结构,细胞和可溶性组分的广泛共识50.在以下部分中,对佩马灭活肺宿主防御的机制来提取注意力,从而允许致殖民化CF气道的病原体。为了提供由HLE活性靶向的蛋白质的概述,它们被分为肺免疫系统的可溶性和细胞靶标,并且总结和下面讨论。
可溶性免疫目标
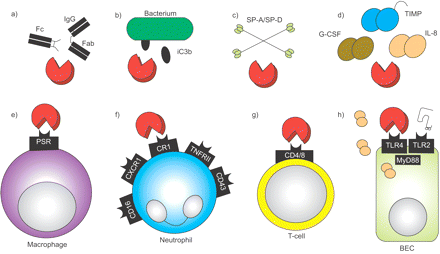
已发现HLE可影响肺部免疫反应的多种可溶性成分(图1a-d)⇓)。特别地,补体OPSONIC C3片段IC3B通过HLE在细菌的表面上切割51.HLE有能力劈裂免疫球蛋白,导致Fc和Fab片段,并导致减少在吞噬作用和杀P.铜绿假单胞菌52.HLE还被证明能降解表面活性剂蛋白(SP)-A和-D,这损害了支气管肺泡间隙的宿主天然防御53- - - - - -56.通过切割和灭活细菌鞭毛引起CF中所见的宿主防御反应的进一步变化57膜联蛋白I是一种钙依赖的磷脂结合蛋白,被认为具有抗炎特性58.此外,HLE似乎是基质金属蛋白酶(MMP)-2和组织蛋白酶基因表达的一种有效的酶原激活剂和诱导剂59,60.然后MMP-2活性的上调可能导致切割和进一步关键免疫蛋白质,如β防御素和乳铁蛋白的失活。HLE被发现是MMP-9的激活剂61和MMP抑制剂的灭活剂TIMP-144,导致MMP和TIMP中的不平衡。最近,这些发现已经在CF肺病中证明的HLE浓度证实了62,63.CF肺病中MMP-9的激活增加了许多可能的下游炎症作用,包括激活潜伏的生长因子(TGF)-β)64和胶原蛋白片段的可能释放用于中性粒细胞65.通过降解补充和释放C5a,脱嗜胞粒细胞的有效的化学反向剂,并通过增加气道浆液细胞粘液生产,还可以有助于肺炎的延续肿瘤66,67.
游离中性粒细胞弹性蛋白酶(红色)对:a-d可溶性的影响;e-h)肺免疫系统的细胞成分。a) Elastase切割免疫球蛋白G,导致Fc和Fab片段脱落。它:b)在调理菌上裂解iC3b;c)降解表面活性剂蛋白(SP)-A和-D,从而破坏宿主支气管肺泡腔的天然防御。d)弹性蛋白酶处理粒细胞集落刺激因子(G-CSF)、金属蛋白酶组织抑制剂(TIMP)和白细胞介素(IL)-8。这些事件导致生长过程的抑制(G-CSF),增加基质金属蛋白酶的活性和更活跃形式的IL-8作为中性粒细胞的趋化剂。e)弹性酶从肺泡巨噬细胞切割磷脂酰丝氨酸受体(PSRs),从而阻碍凋亡细胞从支气管肺泡间隙的清除。f)切割中性粒细胞表面的补体受体(CR)1、CD16、肿瘤坏死因子受体(TNFR)II、CXC趋化因子受体(CXCR)1和CD43,从而使中性粒细胞的细菌吞噬作用(CR1、CD16)、杀伤能力(CXCR1)、粘附作用(TNFRII)和聚集作用(CD43)失效。g)弹性酶进一步切割t细胞上的CD4和CD8,降低细胞毒性和细胞因子的产生。 h) In bronchial epithelial cells (BECs), elastase, as well as cleaved soluble CXCR1 fragments, induce IL-8 production mediated通过toll样受体(TLR) 2/4和常见的配体蛋白,髓样分化因子88 (MyD88),从而放大促炎中性粒细胞流入囊性纤维化气道。
细胞靶标
Pepa的主要细胞靶标显示在图1E-H中⇑.凋亡中性粒细胞的吞噬作用导致TGF-β的产生增加,这反过来又减少了中性粒细胞的产生促炎细胞因子。肺泡巨噬细胞从呼吸道中取出凋亡中性粒细胞通过磷脂酰丝氨酸受体(PSR / CD36),从而促进炎症过程的分辨率68,69.已发现自由毛线从肺泡巨噬细胞切割PSR,这损害了凋亡细胞的间隙70.因此,hle介导的吞噬损伤导致TGF-β的产生减少和促炎反应的放大71.此外,HLE发现通过支气管上皮细胞和LTB以诱导IL-8产生4在巨噬细胞的表达72,73.发现IL-8表达的诱导被介导通过IL-1受体相关激酶1 / myeloid分化因子(MYD)88)/核因子-γ-依赖性途径,表明Toll样受体(TLR)的参与72.此外,HLE切割补体受体(CR)151,74,肿瘤坏死因子受体II75,CD4376,CD16(低亲和力免疫球蛋白G受体(FCγRIII))76如最近所示,高亲和力IL-8受体CXC趋化因子受体(CXCR)177在嗜中性粒细胞表面上。通过这些机制,HLE禁用细菌杀伤(CXCR1),吞噬作用(CR1和CD16),粘附(TNFRII)和扩频/聚集(CD43)嗜中性粒细胞的手段。对于适应性免疫,HLE裂解CD4和CD8 T细胞上,这降低了由T细胞细胞毒性和细胞因子产生78.还发现HLE在成纤维细胞和单核细胞上切割CD14,导致对脂多糖的反应性降低79,80.
综上所述,无对抗的HLE能够破坏先天性和适应性肺免疫反应的几个关键组成部分,这些组成部分结合在一起,导致CF气道肺宿主防御的损伤。特别是补体系统的损伤51,74和IL-8 / CXCR1介导的中性粒细胞功能77可能是重要的相关性,因为这两种机制被发现是有效的体外,以及患有CF肺病的人在活的有机体内.伯杰等等。74结果表明中性粒细胞在激活与上调两CR1和CR3N- 甲基 - 甲硫基 - 白酚 - 苯丙氨酸(F-MLP)。来自CF患者分离的BALF中性粒细胞显示CR3表达增加,类似于F-MLP刺激的血细胞,但与F-MLP刺激的血细胞相比,在BALF中性粒细胞上降低CR1。通过用HLE处理分离的嗜中性粒细胞,可以再现CF BALF细胞的CR1的丧失,而CR3对HLE耐受。在随后的研究中,相同的组表明,Opsonise细菌表面上的补码片段IC3B通过蛋白水解活性切割,并且该机制是可操作的离体51.综上所述,细菌上调理素的丢失,以及气道中性粒细胞上CR1的分裂,导致局部肺调理素受体不匹配,从而损害CF肺疾病中细菌病原体的吞噬作用81.
这是最近发现,除补体系统的弹性蛋白酶体介导损伤,IL-8介导的中性粒细胞的功能也都在CF肺部疾病禁用77.IL-8介导其功能通过两个受体,CXCR1和CXCR282.据证实,CXCR1但不CXCR2传达氧化和非氧化性抗菌功能的中性粒细胞77.然而,CXCR1在CF气道中被剪切,这削弱了IL-8对气道中性粒细胞杀灭细菌的刺激作用。可溶的CXCR1剪切片段进一步被发现介导刺激支气管上皮细胞中IL-8的产生通过TLR2 / MYD88路径。通过吸入α的抑制蛋白酶1- antiTrypsin(α.1-在)在活的有机体内在很大程度上防止CXCR1和CR1切割和改善CF患者的细菌间隙在活的有机体内.
当组合观察时,CR1和IC3B的切割以及CXCR1损害介导介导的吞噬作用和中性粒细胞的直接抗菌功能,并且可以协同作用以解除CF Airways中的先天免疫应答在活的有机体内.
评估Pepa.
由于蛋白酶 - 抗促释放酶系统复杂,并且涉及几种具有非传递因素的相互依赖性,因此本综述主要集中在HLE及其天然抑制剂α上1——。最常见的是,使用标准化和敏感的发色活动测定来测量HELe83.α的量1-AT存在由免疫检测,由ELISA或通过免疫沉淀。α.1-AT可通过氧化和与HLE结合而失活。因此,除了α的量1-AT,它在复合物中与HEE中的HLE,也可以评估其中和HLE的功能能力。由于采样类型,样品制备和进一步加工等预审的问题,对Pepa的准确评估至关重要,因此在以下部分中得到解决。特别地,比较使用BAL和痰,下面讨论每种方法的缺点和缺陷。
支气管肺泡灌洗
可以在所有年龄组(需要全身麻醉或深镇静的婴儿和儿童)的患者中进行支气管镜检查,并且肺部内的局部区域可以精确瞄准84.根据灌洗液的容量,更近端(例如1 ml·kg体重−1)或更多远端区域(例如2- - - - - -4 mL·kg body weight−1)被达到。但是,它是一种侵入性的程序。不良事件,大多数发烧或局部渗透的速率可能会随着体积灌输和潜在的肺病的严重程度而增加。在评估CF患者气道的整体蛋白水解条件时进一步考虑是CF肺病通常在支气管和支气管中更明显,而BAL样品两条支气管和肺泡隔室。
通过过滤回收的BALF应释放粘液,然后通过离心分离细胞从无细胞上清液中。上清液常规用于HLE活动的测定。已经确定了人类志愿者(但不在儿童)中预期的正常漏洞活动范围(稍后讨论)。在健康的个体中通常可以检测到少量或仅次要的自由弹解活性,而抗弹性储备(α1-AT)是生理上存在的。
诱导或自发痰
通过吸入高渗剂,例如6%氯化钠,痰液可以在几乎每个受试者中诱导。痰液诱导技术是安全的,现在广泛用作治疗和诊断选择16.,85,86;由过程感应电势支气管阻塞可通过预处理支气管扩张来减轻。痰的复苏,但是,严重依赖于个人的合作。The majority of young children aged <6 yrs do not reliably spit out sputum that is induced in their bronchial tree, but instead frequently swallow it. Therefore, this technique was considered to be reliably used only in those aged ≥6 yrs. However, a recent study reported the successful application of sputum induction in CF children with a median age of 3 yrs87.尽管对这一年轻年龄组的实用性和安全性进行了进一步的研究,但后一项研究表明,痰液诱导也可用于6岁的CF婴儿。
然而,在使用痰液时应考虑一些局限性。首先,诱导痰被认为比BALF变化更大,特别是在使用连续取样时,因为连续样本可能不会取样肺内的同一区域。这与CF肺疾病尤其相关,因为CF炎症似乎不均匀地影响不同的肺部位88.其次,痰是从肺部排出的复杂材料网络,因此,非常难以将其分离成其原始组件而不会影响它们。通常在化学物质(二硫噻唑醇,DNA酶和其他酶)的帮助下选择并溶解痰液,或机械地溶解。当施加该技术时,释放出从捕获塞网中被捕获的细胞或细胞的细胞内颗粒内容物。此外,化合物可以与在样品加工过程中暴露的粘液或其他表面结合,从而损失分析。因此,预期问题对痰的加工至关重要,并且应该在临床研究之前进行评估和优化。
成人和儿童诱导痰细胞计数和组成的正常值已经确定89,90.在CF患者中,已经进行了有限数量的研究,涉及广泛的CF受试者(稍后讨论)。特别是,对诱导的痰的评估已经证明有助于研究抗生素治疗的影响20.- - - - - -22.,86.在研究抗炎疗法的更微妙效果的诱导痰的价值仍不清楚,因为没有使用从诱导的痰液获得的结果措施公开的抗炎药的研究已经令人信服地证明了一种效果。最近,Mayer-Hamblett等等。91报告了来自4个美国多中心研究的269名CF患者的荟萃分析结果,该荟萃分析探讨了咳痰生物标志物与肺功能(FEV)之间的关系1)。在几个生物标志物中,HLE水平与FEV相关1横截面和纵向,而IL-8和其他推定的生物标志物显示出这些患者中肺功能的关系,表明HLE可用作CF肺病中的生物标志物。总之,BALF和痰两者都可用于研究CF肺病中的蛋白水解活性/脂脂肪,但应考虑两种技术的差异,特别是关于患者的年龄,取样区域和预先生的问题。
具有不同胃底的临床情况
CF肺病是可变的并且在空间和时间区域化,从早期的肺部疾病无临床症状与肺组织和肺功能丧失的破坏渐进的肺部疾病。鉴于广泛CF肺病,适当患者分层为临床研究的先决条件23..本节介绍CF肺部疾病的不同阶段,他们的典型场景和抑制HLE的相关影响。
早期的肺病没有成熟的慢性感染和炎症(临床稳定)
该组包括患者,患者通常在正常范围内表现出肺功能,并且在恶化之外显示临床症状。BALF研究表明,即使是1年龄的CF婴儿也表现出增加的中性粒细胞计数和HLE活性,这取决于其BALF中的细菌病原体92,93.由于在这一人群中诱导痰的技术困难86随着时间的推移,BAL需要对这些患者进行研究。目前尚无关于这些患者HLE状态的长期数据。鉴于吸入HLE抑制剂的潜在抗炎作用94,对这种群体的检查是在检查HLE定向治疗是否能够防止持续气道炎症,改善气道内病原体的许可,以及最终降低慢性阻塞性气道病的进展.
后来的肺病与局部破坏和显着的胃底(临床稳定)
这些受试者的肺功能可能在正常范围内,尽管可能存在一些折衷,并且胸部CT扫描可以清楚地描绘局部肺部破坏的程度和位点95,96.急性加重的不适当的决议,局部的破坏性慢性肺部疾病是建立在肺的某些区域。与此条件从受试者获得诱导痰是可能代表肺内健康领域和显著蛋白水解活性和破坏的区域的混合物。后来的级分痰更精确地表示BALF组合物97.核心问题是吸入蛋白酶抑制剂的治疗是否能够克服局部破坏面积的过度蛋白水解,而不会产生预先存在的抗透明条件的其他肺部区域。在这种情况下,吸入α的效果1-AT随着时间的推移,保护肺的完整性可能是局部破坏的微环境的重要性。使用混合诱导的痰(来自整个肺的材料的收集)可用于测定是否可以实现弹性溶解活性的总体控制。相反,分析序贯痰分的分析可能有助于解决肺内的空间分布97.然而,这种方法尚未用于吸入蛋白酶抑制剂的研究中,并且在未来的调查中仍有待建立。
抑制气道中性粒细胞弹性蛋白酶
为了抑制过量的HLE活动,目前有三类抑制剂可用:1)小型合成化合物;2)通过修改其天然对应物而获得的半合成抑制剂;3)HLE的天然抑制剂(表2⇓)。
中性粒细胞弹性蛋白酶的合成抑制剂
由于有越来越多的证据表明,HLE介导的组织损伤经常发生在嗜中性粒细胞和基底,α之间的紧密界面1-AT might have difficulty in accessing this area due to its large size (52 kDa) and negative charge101..此外的药理学和经济问题表明,稍后总结了合成和半合成丝氨酸蛋白酶抑制剂(Serpins)的发展。已经合成了大量的合成化学化合物并部分地测试了抑制HLE102..理论上,这些低分子量的抑制剂可能优于α1-AT的大小不同,因此CF肺内较窄的蛋白水解位点更易进入103.- - - - - -105..然而,由于意想不到的毒性或进一步的相关问题,合成抑制剂尚未引入临床实践。两肽(如ICI 200355;ICI Americas, Wilmington, DE, USA)和非肽HLE抑制剂(ONO-5046;小野制药株式会社,大阪,日本)已经开发。例如,Sivelestat (ONO-5046/Elaspol)是一种可逆的HLE选择性抑制剂,最初在日本推出。一项针对急性肺损伤患者的2期临床研究由于该化合物的不利影响而暂停。Midesteine (mr - 889;Medea Research,米兰,意大利)是另一种可逆的低亲和力HLE抑制剂,发现它可以通过与硫醇基团的相互作用降低黏液粘度。它似乎是安全的,正在对慢性阻塞性肺病进行临床评估。 Specifically for CF, DMP-777 has been tested in phase 2 studies; however, its development was discontinued by the company. All other developments are in much earlier phases106.而且没有出版任何结果。
半合成抑制剂
半合成抑制剂通常通过天然人蛋白酶抑制剂的化学改性获得。例如,人嗜中性粒细胞弹性蛋白酶(EPI-HNE-4)的工程化蛋白抑制剂衍生自α-抑制剂的KUnitz型结构域107.,108.,这是通常存在于血浆中的血清的天然抑制剂。EPI-HNE-4是一种56-氨基酸长片段,具有4μm的非常低的平衡解离常数,用于HLE,并且具有衍生自人体并抗蛋白水解和氧化的优点107..动物和CF儿童痰液的研究表明,成功抑制了HLE,并减少了中性粒细胞迁移109..EPI-hNE-4目前正在CF患者中进行2期试验。SUPG-032是一种非糖基化重组人α1- antiChymotypsin,其中六个反应性位点氨基酸被α取代1-AT,并对HLE,组织蛋白酶G和蛋白酶3.杂交化合物还通过中性粒细胞抑制超氧化物产生。不幸的是,它的进一步发展被暂停了。最后,应提及含有α的融合蛋白1-AT和分泌白细胞蛋白酶抑制剂(SLPI)活性,目前的发育状况是未知的。
天然抑制剂
HLE的天然抑制剂包括α1-At,单核细胞/嗜中性粒细胞弹性蛋白酶抑制剂(mnei)和血清,如SLPI和ELAFIN / elafin。用α研究1-AT在下面的部分中单独解决。SLPI,一种12-KDA高度阳离子疏水性的单溶胶单链蛋白,由浆液腺细胞和糖粉细胞和杯状细胞的下呼吸道产生,似乎是一种有效的HLE活动抑制剂气道。SLPI和α.1-AT被认为是抗HLE过度的主要防御蛋白,提供了总HLE抑制能力的10-50%110.,111..由于SLPI的反应性与α的反应性不同1-AT,两种抗滴鼻症都可以互补在活的有机体内.mcelvaney.等等。112.在16名成年患者中研究了1周吸入重组人SLPI(每日两次)的重组人SLPI(每日100毫克)的效果。如BAL评估,降低了中性粒细胞的数量和IL-8的水平,并且HLE活性降低> 12小时。然而,当使用50mg 2周时,没有观察到这种效果,清楚地显示剂量依赖性。Elafin,一种类似于SLPI的6 kda肽,是一种特定的弹性蛋白酶抑制剂,这表明促进了肺的抗HLE容量的20%在活的有机体内113.,114..SLPI和ELAFIN都是通过气道上皮细胞的促炎细胞因子上调115.,116.,但是由于发现两者都发现抑制核因子-κB活性和IL-8和单核细胞化学蛋白-1生产117.,118..为了最好的本作者的知识,预蛋白酶蛋白和MNEI至今还未在患者被研究了CF.然而,动物实验数据显示,大幅减少P.铜绿假单胞菌用Mnei治疗后慢性感染的小鼠模型计数长达7天119..进一步的使用HLE天然抑制剂的临床研究需要在CF患者中进行,以便准确评估其效力、有益和有害作用以及在临床环境中的有用性。
除了防滴释放,还发现抗生素差异地影响蛋白酶。发现大环内酯抗生素显示出抑制活性,而Colistin增加了Hle活性体外100.,120..
免费抑制弹性蛋白酶雾化吸入的α1-AT患者参见CF
α.1-At是一种52kDa糖蛋白,主要由肝细胞,肺泡巨噬细胞和中性粒细胞分泌,并作为有效的丝氨酸蛋白酶抑制剂121..α的相互作用1-AT导致蛋白酶的快速和不可逆的灭活。在健康个体中的血清浓度范围为20-60μm。α.1-AT,由肝脏释放,扩散到肺部。虽然肺的水平较低(〜2-7μm),α1-AT被认为有助于肺舱中存在的抗甲解能量的90%122..考虑α时1- 作为治疗剂,源可以是在其他系统中表达的人血清或重组蛋白,例如微生物或转基因动物123..商业α.1-AT制剂可从人血浆(prolatin;Talecris生物治疗,研究三角公园,NC,美国)。prolestin耐受性好,有效在活的有机体内,但准备的纯度只有〜60%124..小说α.1-AT替代制剂,如Zemaira或Aralast,在增加α方面显示与Prolastin相当1-At血清和肺泡上皮水平,提供比常规制剂更高的纯度(Zemaira>芳骨>脯氨酸)124.- - - - - -126..然而,在使用这些制剂CF患者的临床数据是不可用的日期。
静脉内α.1-AT应用最初用于α的个体1-AT缺乏,已据报道是安全和耐受性的127.,目前推荐用于严重遗传(PIZZ / NULL)α的个体1——缺乏128.,129..然而,在CF Airways中,存在的游离蛋白酶量非常高(大部分>10μm,有时甚至可达100μm),并且CF肺中的受影响的位点可能几乎可以到α1——。α.1-AT管理通过i.v.被认为治疗CF患者。然而,初步研究表明,需要大剂量和重复的给药来实现有益的长期影响130..因此,雾化α1-AT已越来越受到关注:1)疾病直接位点靶向,达到较高的肺浓度;2)系统副作用不太可能;3)较少量的α1-AT是必需的;4)无I.v.访问是必需的。
转基因技术使活性重组蛋白的大批量生产成为可能,与纯化的人血清α相比,其成本效益高1——。PPL治疗学(Roslin,UK)开发了转基因绵羊,在其牛奶人α中产生1-AT几乎与人类衍生的α完全相同1-AT,具有一些侧链的糖的例外131..自重组α1-AT半衰期短,I.v.局部排除,但气溶胶给药是可行的132..CF患者使用重组α的试验研究1-AT源自转基因绵羊,没有过敏作用,高达500mg重组α1——·天−1133..然而,使用重组α1-AT可能具有对吸入非人蛋白痕量的抗体反应的问题,并且可能导致过敏反应134..
表3.⇓4.⇓使用BAL总结已发表的研究(表3⇓) and sputum (table 4⇓)评估吸入α的效果1CF肺疾病患者的-AT
第一阶段的研究评估了α的生化作用1- 在CF患者中吸入,并为雾化α的潜在效果提供了重要的洞察1-AT在CF肺病中98.Twelve adult subjects with CF inhaled 100–200 mg (1.5–3.0 mg·kg body weight−1)α1-AT两次,每天1周。雾化器提供α的估计疗效1-At进入肺部是〜10-20%,导致肺部沉积〜10-40mg。在吸入之前,所有受试者都会测量他们的Balf Hle活动。如果上皮衬里流体浓度α1-AT增加到一个>8μm的水平,所有自由的HLE被阻塞。有趣的是,治疗后的Balf没有抑制中性粒细胞杀伤P.铜绿假单胞菌体外,正如使用预处理BALF所发现的那样,表明HLE有效地损害抗菌性嗜中性粒细胞功能在活的有机体内.本研究患有FEV的CF患者1>的60%预测值清楚地显示肺泡腔内游离HLE,在某些情况下呈剂量依赖性中和并达到游离抗HLE能力。在另一项较小的研究中,α治疗1-AT在较低剂量范围内导致总蛋白水平、分子量<20 kDa的蛋白数量和数量以及SP-A的降解产物的降低137..在后一项研究中,α无作用1- 在表面活性剂转化酶上,注意到由丝氨酸蛋白酶抑制剂抑制的肺泡酶,被注意到138..在健康成人中,α1-AT half-life is 69.2 h and the half-life of anti-elastolytic capacity is 53.2 h, suggesting that once daily dosing may be appropriate. However, the functional half-life under specific conditions, such as CF, may be different and remains to be determined.
在唯一的随机安慰剂对照CF试验中,使用诱导痰来评估不同剂量吸入α的效果1-AT (125, 250 and 500 mg), levels of myeloperoxidase, a surrogate for neutrophil activity, were reduced after α1-AT治疗,但只在组接受α的最高剂量1-AT (500 mg)133..同样,牛磺酸(中性粒细胞的替代物)的水平也略有下降139..符合此发现,发现α后嗜中性粒细胞的数量以及促炎细胞因子水平降低1-At吸入94.有趣的是,在这些研究中,痰的HLE活动不是133.,139.,或只是部分地94,减少了。Berger仅以摘要形式发表了另一项涉及22名成年CF患者的研究等等。136.,显示HLE水平的降低,但在雾化α时,IL-8水平和中性粒细胞数量没有变化1-AT治疗。痰与balα之间这种差异的原因是什么?1-AT研究?首先,痰和BAL样本不同区域的肺部。预期由BAL采样的外周区域表现出较低的炎症活性和细菌载荷84.CF肺病几乎完全被排除在肺泡空间之外,并且即使在肺移植后获得的严重受损的肺部肺部,也只在肺泡中观察到少量炎症细胞140..其次,在制备BALF上清液的过程中,灌洗回收的黏液往往在过滤过程中被去除,其中含有被截留的白细胞等附着的元素。相反,在制备痰液时,细胞碎片和凋亡的白细胞可能被纳入分析。最后,应考虑使用不同的方法获得痰上清。当溶胶相被制备时,细胞内和细胞外未确定的成分可以被释放到上清液中。这与用机械、酶或生化方法制备的无细胞上清不容易比较。
试图在CF患者的肺部内定义最佳区域进行α1-AT,优惠外围设备(肺泡)沉积相比更中心(支气管)沉积94.在两种沉积方法之间发现了任何结果参数的差异。在组合这两个组中,前述研究表明,吸入α1-AT增加α.1-AT水平和HLE活动水平降低,中性粒细胞率的百分比,促炎细胞因子和殖民地的含量P. eruginosa。肺功能不受α的影响1-AT吸入,这可能是由于在相对短的治疗期。抗蛋白酶治疗的缺点是气雾状抗蛋白酶,与大多数其他药物,勉强可以在肺的通风较差的是需要治疗最沉积。此外,复杂的环境,如在CF肺部的药物动力学特性和动态特性是难以建立。因此,挑战仍然有效地沉积α1- 在CF肺病的遗址。因此,这是关键的是,在短时间内优化递送系统以最小的时间,气溶胶损失最小。这可以通过组合产生气溶胶的有效雾化器来实现,该装置具有保证优化的呼吸图案的装置。Akita(用于控制治疗气溶胶的受控吸入的电子调节装置)装置,用于使用智能卡的个体呼吸图案编程,代表这样的系统。使用这种方法,〜85%的气溶胶可以送入肺部94.与以前的系统相比,这种装置在定位和将相对大量的气溶胶输送到肺部方面更优越。对依从性的自动监测有助于确定对治疗的依从性。
涵义进行临床试验
鉴于CF肺病中肽的众多靶标,可以设想许多用于临床阶段1和2A研究的临床阶段的潜在结果变量。这些方法将允许对CF肺病的病理生理学更加了解。然而,对于CF患者的HEL抑制的未来临床研究,重要的是,相关的目标种群是明确定义和分层的。这些试验中的成功只会通过以下方式实现:1)选择的代表性研究人群,2)精心设计的主要和次要结果参数,3)适用于样品制备的方案,4)现场培训,以遵守这些程序的现场培训.最后,在经验丰富的中央实验室中可以获得存储的所有变量的批量分析至关重要。对于第2B阶段和3阶段的研究,结果变量如FEV1和加重的速度和时间是合适的;替代标记的额外分析,例如细胞因子分析,在研究中,副中心可以有助于解释结果。吸入α的大型研究1-At或其他蛋白酶抑制剂对Sle抑制作为CF肺病中的治疗方法的效果的系统评价至关重要。
总结
气道中性粒细胞弹性蛋白酶的抑制代表了限制中性粒细胞衍生蛋白酶活性在囊性纤维化肺病中的自毁过程的致病方法。尽管有几次旨在实现这一目标的尝试,但临床上有用的概念才刚刚开始发展。α.1抗胰蛋白酶,弹性蛋白酶自由的天然抑制剂,已在几个临床研究中被采用,并取得了承诺,但尚未有说服力的,结果。代表性研究人群,阐述了用于样品制备,方法的准确性和相关端点的协议,以便是必要的进一步验证在囊性纤维化肺病的弹性蛋白酶抑制的有用性。
感兴趣的语句
没有宣布。
- 已收到2007年11月5日。
- 接受2008年3月31日。
- ©ers Journals Ltd