摘要
抗病毒性先天免疫反应可能在哮喘中受损,尽管其机制尚不清楚。toll样受体(TLRs) 7和3分别识别单链病毒RNA和双链病毒RNA,这两种受体在启动对常见呼吸道病毒的应答时特别相关。本研究的目的是探讨TLR7和TLR3在14岁以上哮喘青少年中的作用。
从17名特应性哮喘患者,29特应性,非哮喘和21名健康,非特应性个体获得的外周血单核细胞,刺激与所述TLR7激动剂咪喹莫特和TLR3激动剂聚I:C。通过实时PCR测量的抗病毒分子的表达。干扰素γ诱导细胞因子蛋白(IP)-10和白细胞介素(IL)的浓度-6通过ELISA测量。
TLR7-induced myxovirus resistance protein A and 2′5′ oligoadenylate synthetase mRNA expression and protein levels of IP-10 were significantly lower in asthma subjects compared with healthy subjects (p = 0.041, p = 0.003 and p = 0.001 respectively). There was a significant negative correlation between total serum immunoglobulin E and IP-10 following TLR7 stimulation. However, TLR3-induced responses did not vary with asthma or atopy. IL-10 mRNA and IL-6 protein synthesis were similar in asthmatic and control subjects. In conclusion, TLR7 function is reduced in adolescents with asthma and this may contribute to susceptibility to respiratory viral infections.
病毒性呼吸道感染,尤其是鼻病毒(RV),是哮喘加重的儿童和成人的主要病因1-3。成人哮喘患者并不一定比健康人更频繁地感染右心室病毒,但当右心室病毒感染发生时,他们会诱发更频繁和更持久的下呼吸道症状4。
病毒感染加重哮喘气道炎症和高反应性的机制是复杂的,还没有完全被了解,尽管抗病毒免疫反应的缺陷越来越被认识。急性RV感染期间的病毒血症在哮喘急性加重儿童中比在非哮喘性感冒儿童中更常见五这表明,哮喘与限制病毒系统性传播的能力降低有关。此外,在哮喘急性发作数周后,40%的哮喘患儿的呼吸道分泌物中可检测到RV RNA6从呼吸道暗示的能力降低要么明确RV,或恢复期,以防止新的感染。
最近的研究为研究哮喘的抗病毒先天免疫提供了重要的见解。RV感染的支气管上皮细胞培养时,细胞从哮喘受试者产生更少的干扰素(IFN) -β和IFN-λ相对健康的捐赠者7,8。肺泡巨噬细胞和哮喘患者循环白细胞也似乎具有缺陷的能力,以合成I型和III型IFN7,9,10,这表明在哮喘受损的抗病毒反应涉及不循环内的前体肺的只是结构性的细胞,也是洄游的免疫细胞和。然而,导致改变抗病毒先天免疫哮喘的分子机制尚不清楚。
先天免疫响应于病毒感染是涉及病毒成分的初始检测一个多步骤的过程,随后的IFN调节因子(脉冲响应函数),随后的IFN基因转录,和一个大家族“下游”的最后的感应的表达IFN-刺激的基因诱导的细胞内抗病毒状态,从而限制了病毒复制。病毒通过一个家族的细胞质受体和通过病毒感测细胞内检测到的Toll样受体(TLR),其位于核内体内11,12。TLR7和TLR3是特别相关关于RNA病毒(如。它们分别识别单链病毒RNA和双链病毒RNA(在病毒复制过程中形成)并对其作出反应。
这项研究的目的是研究在哮喘TLR7和TLR3功能。我们假设,哮喘会在TLR7和/或TLR3反应不足有关。该研究的主要终点是IRF7的表达(被鉴定为抗病毒免疫的“主调节器”13),两个IFN刺激的基因,粘病毒抵抗蛋白A(MxA蛋白)和2'5'寡腺苷酸合成酶(OAS)和IFN-γ诱导细胞因子蛋白(IP的分泌)-10(也称为CXCL10)。双方的MxA和美洲国家组织有直接的抗病毒特性:目标的MxA广泛的RNA病毒的核蛋白14,而OAS增强病毒RNA降解15。IP-10充当用于激活T辅助-1细胞和自然杀伤细胞的化学引诱物和已被紧扣哮喘的病毒发作16。此外,我们还检测了促炎细胞因子白细胞介素(IL)-6和免疫调节细胞因子IL-10。
我们在青少年队列研究这些目标,使用外周血单核细胞刺激的咪喹莫特,合成TLR7配体,和聚肌苷酸:聚胞苷酸(聚I:C),合成的双链RNA类似物激活TLR3。为了确定是否遗传性过敏症本身影响抗病毒反应,过敏性都和非过敏性科目谁没有哮喘进行了研究。
材料和方法
主题
这项病例对照研究是一项更大的纵向出生队列研究的一部分,该研究已在其他地方进行了描述17。17名目前活跃的特应性哮喘患者在过去的一年中被医生确诊为哮喘并出现喘鸣。对照组包括29例特应性但无哮喘患者,以及21例非特应性、非哮喘患者(健康对照组)(表1)⇓)。Atopy was defined as any one of the following: a positive skin prick test (SPT) result (weal diameter ≥3 mm); specific immunoglobulin (Ig)E (≥0.35 kU·L-1)至至少一种变应原;or total serum IgE ≥150 kU·L-1。下面的过敏原使用:Dermatophagoides pteronyssinus油,花生油,食品混合物(特异性IgE只),黑麦草,沙发/百慕大草,模具混合物和草混合物(SPT只)。从受试者的父母和同意获得书面同意。这项研究是由人类伦理委员会,玛格丽特公主儿童医院(澳大利亚珀斯)。
细胞制备和培养
血液样本收集到等量的RPMI 1640 (Invitrogen-Life Technologies,墨尔本,澳大利亚),其中含有不含防腐剂的肝素(20 U·mL)-1)。外周血单核细胞(PBMC)通过密度梯度离心法分离并在液氮中冷冻保存,如先前所描述18。此过程不会扭曲细胞免疫应答19,20,和has been used routinely in our laboratories in numerous studies over the last 15 yrs.
在功能研究和流式细胞术中,PBMC解冻、计数和重悬时间为1×106可行的细胞·毫升-1在RPMI 1640补充10%胎牛血清和庆大霉素。采用2.5×10圆底96孔板培养PBMC,评价TLR的活化情况五细胞·好-1in duplicate in medium alone (unstimulated control), with poly I:C (50 μg·mL-1;Sigma, Castle Hill, Australia) or with imiquimod (R837) (1 μg·mL-1,根据剂量反应研究得出的最佳剂量;数据未显示)并由Berghofer使用等。21(InvivoGen Corporation制,圣地亚哥,CA,USA)中在37℃,5%CO26 h。这个时间的选择是基于初步的时间响应实验,如图1所示⇓和2⇓,which showed peak mRNA expression at 6 h. In some experiments, PBMC were cultured in the presence or absence of dexamethasone (Sigma) at concentrations between 10-6 M and 10−10M。细胞微球于-20℃裂解缓冲液(Qiagen Pty Ltd, Clifton Hill, Australia)中保存,直至RNA提取。
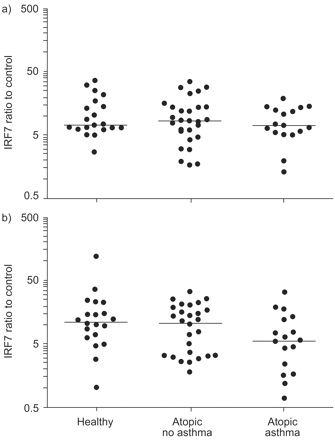
干扰素调节因子(IRF)7在a) toll样受体(TLR)3 (poly I:C)或b) TLR7 (imiquimod)刺激后的表达,在对数刻度上绘制。mRNA表达为受刺激与未受刺激样品的比值。水平线表示中值。统计学意义采用有序Kruskal-Wallis检验(p = 0.065)。
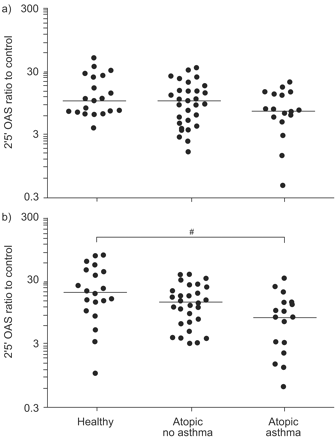
2’5’寡聚腺苷酸合成酶(OAS)在a) toll样受体(TLR)3 (poly I:C)或b) TLR7 (imiquimod)刺激下的表达,在对数刻度上绘制。mRNA表达为受刺激与未受刺激样品的比值。水平线表示中值。统计学意义首先通过有序Kruskal-Wallis检验进行评估(p = 0.002)。#:p = 0.003 from pair-wise Mann–Whitney tests.
MxA蛋白,OAS,IRF7和IL-10 mRNA的表达的实时PCR分析
使用RNeasy 96试剂盒(Qiagen Pty Ltd)从细胞微丸中提取总RNA,使用Omniscript II试剂盒(Qiagen Pty Ltd)用寡核苷酸- dt引物(Promega, Madison, WI, USA)和RNase抑制剂(Perkin Elmer, Boston, MA, USA)按照制造商的说明进行逆转录。将单链cDNA按1:5稀释,在ABI PRISM 7900HT (Applied Biosystems, Melbourne, Australia)上使用定量SYBR green PCR试剂盒(Qiagen Pty Ltd)进行实时PCR。IRF7、MxA、OAS和IL-10的内含子跨越引物由Primer Express软件(Applied Biosystems)自行设计或直接购买(Applied Biosystems)。详细的引物序列和PCR条件可以在网上的补充材料中找到。熔点曲线分析用于评估分析的特异性。拷贝数通过PCR产物或质粒标准品的10倍连续稀释确定,并归一化为参考基因UBE2D222。数据表示为刺激对照(未刺激)的样品的比例。
IL-6,IL-10和IP-10
The level of IL-6 and IL-10 protein was analysed from the cell culture supernatants using time-resolved fluorometry (limit of detection 10 pg·mL-1),详情请参阅其他资料23,24。抗体对分别来自BD Biosciences(澳大利亚悉尼)获得。使用重组IL-6或IL-10(BD Biosciences)中的连续稀释液产生标准曲线。对于检测,铕标记的链霉亲和第一,随后加入增强溶液(两者都来自DELFIA WALLAC,图尔库,芬兰)。IP-10水平也分析了细胞培养上清液使用标准ELISA技术通过BD Biosciences公司的建议。抗体对和重组IP-10用于获得标准曲线的所有自BD Biosciences获得。所有的蛋白质数据表示为δ值(受激样品减去对照样品中蛋白质水平在蛋白质水平)。
统计分析
组间差异的统计显着性首先是由秩和检验测试的有序版本,即Jonckhere-Terpstra检验分析25。This test assumes that the groups are inherently ordered (as shown by the increasing IgE levels across the healthy, atopic and atopic asthma groups) (table 1⇑)。在一个显著差异(p <0.05)被发现的情况下,成对比较中使用Mann-Whitney U-检验然后进行分析。在情况下,IL-6的增量值是≤0,5的任意值被分配到允许它们被对数标度绘制,但统计数字对原始数据进行的。使用Fisher精确检验和配对样本之间的差使用Wilcoxon配对符号秩检验来评估,分析在致敏图案组之间的差异。斯皮尔曼的Rho是用来评估的相关性。SPSS的Mac OS X(SPSS公司,Chicago,IL,USA)中的数据和p的分析中使用<0.05被认为是统计学显著。
结果
研究人群
The characteristics of the study groups are outlined in table 1⇑。The pattern of sensitisation was similar in atopic subjects with or without asthma, with the exception that more asthmatics had specific IgE to “food mix” than atopic non-asthmatics (p = 0.048; data not shown). Both the atopic asthmatic and atopic non-asthmatic group had significantly higher total IgE levels than the healthy control group (p<0.001 for both comparisons). 11 (64.7%) asthmatics were prescribed inhaled corticosteroids (ICS) at the time of the study.
对TLR3和TLR7刺激的反应
用poly I:C (TLR3配体)和imiquimod (TLR7配体)刺激PBMC,结果以未刺激细胞的比例表达。对照组未受刺激细胞经real-time PCR检测到IRF7、MxA和OAS表达水平,经刺激后明显升高(p<0.001;数据未显示)。未刺激细胞的IRF7、MxA和OAS表达无统计学差异(数据未显示)。在最初的时间-过程实验中(补充图1)⇑和2⇑), expression of IRF7, MxA and OAS was readily induced by 6 h, and remained stable at 24 h. All experimental end-points were, therefore, measured at 6 h following stimulation.
IRF7基因转录
在TLR7刺激后,与健康受试者相比,特应性哮喘组的IRF7表达有下降趋势(图1)⇑),但无统计学显著。与此相反,IRF7表达在以下TLR3刺激所有三个组中相似。
OAS和MxA基因转录
在TLR7刺激后,哮喘患者OAS和MxA的表达均显著低于两组健康对照组(p = 0.003和p = 0.041;无花果2⇑和3⇓)。同样,无论是MxA还是OAS,健康对照组与无哮喘特应性组之间也没有差异。相比之下,三组在TLR3刺激后OAS和MxA表达均相似。
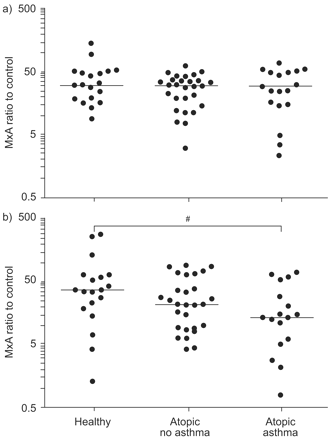
粘病毒抵抗蛋白A(MxA蛋白)的表达之后的)Toll样受体(TLR)3(聚I:C)或b)TLR7(咪喹莫特)刺激,绘制在对数标度。mRNA表达为受刺激与未受刺激样品的比值。水平线表示中值。Statistical significance was first assessed by the ordered Kruskal–Wallis test (p = 0.024).#: p = 0.041,来自成对的Mann-Whitney检验。
IP-10、IL-10、IL-6蛋白表达
Following TLR7 stimulation, protein levels of IP-10 were significantly (p = 0.001) reduced in the cell culture supernatants from asthmatic subjects compared with healthy control subjects (fig. 4⇓)。相比之下,在TLR3刺激后,三组患者的IP-10水平无差异(图4)⇓)。这与之前提出的抗病毒分子的mRNA数据是一致的。此外,当所有三组患者的数据一起分析时,TLR7刺激后产生的IP-10的量与血清总IgE (Spearman rho r2 = −0.350, p = 0.008).
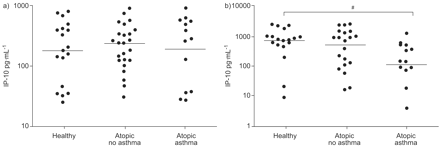
干扰素γ诱导细胞因子蛋白(IP)-10生产下列一)Toll样受体(TLR)3(聚I:C)或b)TLR7(咪喹莫特)刺激,绘制在对数标度。数据表示为在δ值(刺激减去控制)。水平线表示中值。Statistical significance was first assessed by the ordered Kruskal–Wallis test (p = 0.007).#:p = 0.001 from pair-wise Mann–Whitney tests.
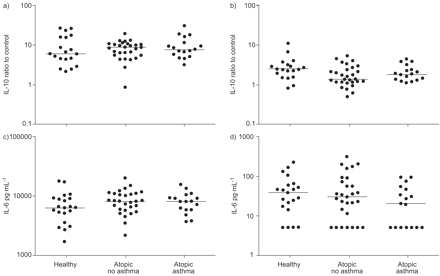
为了确定在哮喘见于OAS和MxA蛋白基因转录和IP-10生产的减少是否会反映先天免疫功能的损害一般,我们还调查了细胞因子IL-6和IL-10。以下两者TLR3和TLR7刺激IL-6蛋白产量为容易检测的。然而,IL-10蛋白生产TLR3刺激,这表明在对照和哮喘患者之间IL-10蛋白的浓度没有显著差异(平均值±后是唯一可检测SE1,491。6±220.0 pg·mL-1和1,五24。五±376.9 pg·mL-1, 分别)。As the concentration of IL-10 was below the level of detection (10 pg·mL-1TLR7激活后,检测IL-10 mRNA的表达。与蛋白数据一致,IL-10 mRNA的表达在哮喘患者和两组对照组细胞受到刺激时无明显差异通过TLR3 (fig. 5⇓)。同样的,刺激通过TLR7showed no difference in IL-10 mRNA expression between the asthmatic and control groups (fig. 5⇓)。相对于IL-6释放,刺激通过TLR3引起的反应大于刺激通过TLR7。然而,IL-6释放的图案没有显著哮喘和两个对照组,之间不同的细胞是否刺激无论通过TLR3 or TLR7 (fig. 5⇓)。
A,B)白细胞介素(IL)-10的表达和c,d)IL-6释放以下Toll样受体(TLR)3(聚I:C; A,C)或TLR7(咪喹莫特; B,d)刺激,绘制在对数刻度。IL-10的mRNA是作为刺激对照(未刺激)的样品的比例。水平线表示中值。IL-6蛋白水平显示为增量值(刺激减去控制)。δ值<0分别给予5的任意值(检测的一半极限)。
糖皮质激素对TLR3和TLR7功能的影响
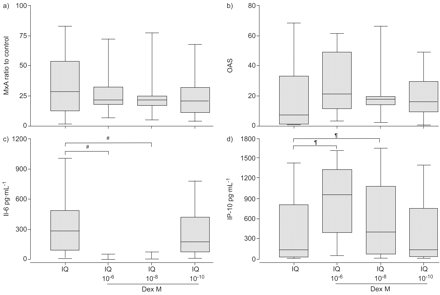
因为在这项研究中,17名哮喘患者中有11人在研究时服用了ICS,所以确定这是否会产生影响是很重要的体外细胞的反应。然而,在哮喘患者中,经TLR3或TLR7刺激后IRF7、OAS和MxA的表达与非经TLR3或TLR7刺激后的IRF7、OAS和MxA的表达无显著差异(数据未显示)。由于从青少年队列获得的细胞有限,成年PBMC受到刺激体外用咪喹莫特和地塞米松。地塞米松的添加浓度为10-6 M and 10−10 M to cell cultures had no discernible effect on MxA or OAS transcription after TLR7 stimulation (fig. 6⇓), whereas dexamethasone significantly inhibited IL-6 (p = 0.012) and increased IP-10 (p = 0.017) synthesis in a dose-dependent manner (fig. 6⇓)。
响应;地塞米松(DEX)的Toll样受体(TLR)7(IQ咪喹莫特)效果。粘病毒抵抗蛋白A(MxA蛋白)和2'5'寡腺苷酸合成酶(OAS)mRNA的表达水平表示为刺激对照(未刺激的)样品的比例。白细胞介素(IL)-6和干扰素γ诱导细胞因子蛋白(IP)被示出-10水平的增量值(刺激减去控制)。n = 8.#: p = 0.012;¶:p = 0.017. The p-values are from Wilcoxon-matched pairs signed-rank test for paired responses.
讨论
病毒诱发哮喘加重的确切机制尚不清楚,但先天免疫功能的损害似乎起着关键作用。我们的研究中出现的新发现是,哮喘青少年的PBMC在TLR7激活后,OAS和MxA mRNA表达减少,IP-10的产生减少通过与健康对照组相比。此外,血清总IgE与TLR7刺激后产生的IP-10的量呈显著负相关。TLR3功能正常,IRF7、OAS、MxA mRNA表达及IP-10水平与哮喘组及对照组相似。
研究者的几个小组已经报道,成人和儿童哮喘合成培养的细胞较少I型和响应于III型IFN体外感染活病毒7-10。我们的研究在哮喘突出异常TLR7功能,这意味着受损响应的病毒ssRNA(天然配体为TLR7)可能在这种疾病导致受损的抗病毒先天免疫增加了这些早期研究。有趣的是,在变型TLR7基因似乎是慢性丙型肝炎病毒感染的危险因素26。据我们所知,虽然最近有报道称在哮喘中存在遗传变异,但此前没有研究检测TLR7在哮喘中的作用TLR7基因,以及密切相关的TLR8基因,与哮喘和特应性的其他病症相关的27。
在考虑这些发现对哮喘的意义之前,考虑其他潜在的混杂因素是很重要的。在没有哮喘的情况下,特异性反应与TLR7或TLR3功能的改变无关。我们也没有发现任何证据表明生长或青春期状态的变化可以解释我们的发现。所有被研究的年轻女性均已进入月经初潮,根据Tanner分期,大部分年轻男性已进入青春期。身高与先天免疫反应无关(数据未显示)。虽然许多哮喘患者都曾被开过处方,但似乎最不可能的是我们的体外结果可以归因于这些药物,如IRF7,OAS和MxA蛋白表达与ICS用途而变化。此外,OAS和通过刺激的PBMC的MxA表达出现于地塞米松曝光相对耐体外,即使浓度高达10-6M。这些浓度远远高于低至中等剂量ICS治疗哮喘患者的血清皮质类固醇水平。
值得注意的是,虽然TLR7函数,哮喘受损,一个TLR3的配体的能力来诱导关键的抗病毒分子是哮喘和对照组相似。这可以涉及通过TLR7和TLR3引起的不同的信号传导途径来激活免疫应答的基因。而TLR7利用接头蛋白的MyD88,TLR3信号通过接头蛋白TRIF和相对独立的MyD88的28。
导致哮喘TLR7功能受损的分子机制可能是复杂的,将是今后研究的重点。TLR7在哮喘患者和对照组未受刺激的PBMC中表达程度相似(数据未显示)。IRF7是IFN基因的上游调控因子,因此我们在哮喘中观察到的IRF7低表达的趋势将被预测为产生低IFN基因转录。然而,一些报告表明,活病毒和TLR7配体也可以直接诱导下游抗病毒途径,独立于IFN29-31。这是在哮喘的另一个潜在机制可能随后导致下游抗病毒基因如MxA蛋白和OAS,和降低的IP-10的合成降低的转录。据报道,RV-暴露PBMC从哮喘患者与健康对照产生更多的IL-10比PBMC32。然而,我们发现在所有群体中TLR3-和TLR7激活PBMC这种免疫调节细胞因子的表达相似;因此,IL-10似乎并不解释在哮喘所见的损害TLR7功能。
我们必须承认当前研究的局限性。我们的研究结果是基于IRF7,美洲国家组织和表达的MxA通过实时PCR表达,我们没有测量这些分子的蛋白表达。这三种方法都不能在培养上清液中测定细胞内的蛋白质,以及血液中的研究没有提供足够的细胞材料进行蛋白质印迹或以测量IRF7磷酸化和从细胞质至细胞核的转位收集的体积。为了解决这个蛋白质缺乏数据的测量,我们已经紧密联系在一起的哮喘发作病毒的IP-10,趋化因子的水平16在下面的TLR刺激的培养物上清液。在与mRNA的数据相一致,减少蛋白质生产的IP-10以下TLR7,但不是TLR3,刺激哮喘青少年文化强化的概念,即TLR7功能在减少哮喘与健康对照。
患有哮喘的研究对象有轻度到中度的疾病,因此在更大范围的疾病严重程度和不同年龄的患者中检测TLR7功能对未来的研究将是重要的。我们所描述的发现似乎不太可能是针对青春期哮喘的,特别是TLR7功能降低和抗病毒分子表达减少与以前哮喘儿童和成人气道上皮细胞和免疫细胞合成IFN低的报道广泛一致7-10。
利用针对特定病毒识别受体的活病毒和分子进行研究,可能为深入研究抗病毒先天免疫机制提供补充信息。虽然我们的发现强调了TLR7功能在哮喘中的潜在重要性,但这并不排除哮喘中其他病毒检测受体功能的异常,如视黄酸诱导基因I和黑色素瘤分化相关蛋白-5。更好地理解先天免疫反应将是开发治疗哮喘病毒感染的新方法的基础。
支持声明
这项研究是由美国国家卫生和医学研究理事会(堪培拉,澳大利亚)的资助,芬兰科学院(赫尔辛基,芬兰)和昆士兰州的哮喘基金会(Fortitude Valley的,澳大利亚)。
利益声明
没有宣布。
致谢
作者希望感谢研究参与者和他们的家人。
脚注
这篇文章有补充材料可从www.www.qdcxjkg.com
- 收到2008年11月12日。
- 公认2009年7月16日。
- ©ERS杂志有限公司