摘要gydF4y2Ba
慢性阻塞性肺病(COPD)是第三大死亡原因。他汀类药物可能对COPD等呼吸道疾病有治疗潜力,但是否能预防支气管上皮损伤尚不清楚。我们假设辛伐他汀可减轻急性烟草烟雾诱导的中性粒细胞性肺炎症和气道上皮损伤。gydF4y2Ba
自发性高血压大鼠给予辛伐他汀20 mg·kggydF4y2Ba−1gydF4y2Bai.p。gydF4y2Ba)在接触烟草烟雾前7天和接触烟草烟雾后3天,或仅在接触烟草烟雾期间。gydF4y2Ba
在吸烟暴露之前和整个暴露过程中持续使用辛伐他汀预处理可减少白细胞、中性粒细胞和巨噬细胞流入肺和气道的总量。辛伐他汀减弱烟草烟雾诱导细胞浸润肺实质和气道上皮下和间质间隙。1周的辛伐他汀预处理几乎完全阻止了烟致气道上皮层剥蚀,而辛伐他汀仅与烟暴露同时使用没有效果。gydF4y2Ba
辛伐他汀可能是治疗吸烟所致肺部疾病(如COPD)的一种新的辅助疗法。鉴于他汀类药物需要预处理,可能存在一个关键的调节过程,这对于他汀类药物的抗炎作用是必要的。未来的工作需要阐明他汀类药物保护作用的机制。gydF4y2Ba
简介gydF4y2Ba
慢性阻塞性肺疾病(COPD)是美国第三大死亡原因,目前的治疗方法并不能显著改变疾病的进展[gydF4y2Ba1gydF4y2Ba].美国大约有2000万成年人患有慢性阻塞性肺病,死亡率为10万分之20 [gydF4y2Ba2gydF4y2Ba].一般人患慢性阻塞性肺病最常见的原因是吸烟[gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3.gydF4y2Ba].持续炎症是COPD发病机制的一个关键组成部分。细支气管壁增厚伴有炎症细胞(包括中性粒细胞、巨噬细胞和淋巴细胞)的涌入,是COPD的特征[gydF4y2Ba4gydF4y2Ba- - - - - -gydF4y2Ba8gydF4y2Ba].gydF4y2Ba
除降低胆固醇外,他汀类药物("他汀类药物")还具有多效抗炎、免疫调节、抗氧化和抗增殖特性,具有心血管疾病以外的潜在临床应用[gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba].由于这些多效性作用,他汀类药物已被提出作为一种潜在的新型治疗炎症性呼吸道疾病,包括支气管哮喘和慢性阻塞性肺病[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba].COPD发病率、死亡率的显著降低和肺功能的改善归因于他汀类药物的使用[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba13gydF4y2Ba- - - - - -gydF4y2Ba18gydF4y2Ba].此外,他汀类药物已被发现可减少细胞培养中中性粒细胞的跨内皮迁移[gydF4y2Ba19gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba]以及中性粒细胞炎症和流入动物肺组织[gydF4y2Ba19gydF4y2Ba,gydF4y2Ba21gydF4y2Ba- - - - - -gydF4y2Ba24gydF4y2Ba].gydF4y2Ba
他汀类药物的抗炎作用部分是介导的gydF4y2Ba通过gydF4y2Ba抑制甲羟戊酸途径。具体来说,他汀类药物抑制3-羟基-3-甲基-戊二酰辅酶a (HMG-CoA)还原酶,这是胆固醇生物合成中的限速步骤。HMG-CoA还原酶的直接产物是甲羟戊酸盐,它被代谢成非固醇类异戊二烯,法尼基焦磷酸和香叶酰焦磷酸,以及胆固醇。这些代谢产物对于翻译后异丙烯化和细胞内单体小g蛋白(Ras, Rho, Rac, Cdc42,gydF4y2Ba等。gydF4y2Ba).单体小g蛋白(或GTPases)控制许多重要的生物学功能,包括免疫细胞功能、细胞骨架动力学、转运和细胞增殖[gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,gydF4y2Ba25gydF4y2Ba],并被认为至少可以调节他汀类药物的一些有益效果。gydF4y2Ba
另一些人发表了辛伐他汀在减轻吸烟引起的肺气肿、肺动脉高压和小气道重塑方面的有益作用[gydF4y2Ba26gydF4y2Ba,gydF4y2Ba27gydF4y2Ba].然而,没有研究评估他汀类药物是否能抑制吸烟引起的大气道或支气管上皮损伤。这个问题与人类与吸烟有关的肺部疾病(如慢性阻塞性肺病)高度相关。因此,在本研究中,我们假设辛伐他汀全身治疗可以:1)减轻急性烟草烟雾引起的肺部炎症;2)抑制气道上皮损伤。我们评估辛伐他汀治疗是否影响甲羟戊酸通路和肺Ras和Rho GTPase激活。我们使用了COPD自发性高血压大鼠模型,因为它对烟草烟雾暴露有很强的中性粒细胞炎症反应[gydF4y2Ba28gydF4y2Ba- - - - - -gydF4y2Ba34gydF4y2Ba].该模型在暴露于烟草烟雾4周后产生类似copd的病理,包括黏蛋白高分泌、气道上皮鳞化和增厚、气道扩大和肺功能改变。我们选择通过急性烟草烟雾暴露来测试辛伐他汀的效果,从而诱导肺部炎症,以将辛伐他汀对白细胞招募和气道上皮损伤的预防作用与促进恢复的可能作用隔离开来。此外,这种烟草烟雾暴露方案允许我们将辛伐他汀对白细胞招募和气道上皮损伤的预防作用与预防粘液积聚分离开来,粘液积聚是由于粘蛋白过度分泌和纤毛上皮细胞的损失,这是在长期暴露于烟草烟雾中发生的。gydF4y2Ba
材料与方法gydF4y2Ba
动物gydF4y2Ba
12周大的自发性高血压雄性大鼠购自查尔斯河实验室(Portage, MI, USA)。到达后,所有动物都被安置在聚碳酸酯笼子里,在12小时的明暗模式下,持续获得食物和水。在开始接触烟草烟雾之前,动物已经适应了新的居住环境1周。所有动物都根据美国动物福利法进行处理,所有程序都在加州大学戴维斯分校动物护理和使用委员会的监督下进行。gydF4y2Ba
接触烟草烟雾gydF4y2Ba
每组6只自发性高血压大鼠分别暴露于过滤空气或烟草烟雾(~ 80-90 mg·m)中gydF4y2Ba−3gydF4y2Ba总悬浮粒子(TSP)),持续6小时·天gydF4y2Ba−1gydF4y2Ba3天。使用TE10烟雾暴露系统进行全身暴露于香烟烟雾[gydF4y2Ba35gydF4y2Ba]燃烧3R4F研究香烟(美国肯塔基州肯塔基大学烟草与健康研究所),每分钟一次喷出35 mL,持续时间2秒(联邦贸易委员会吸烟标准[gydF4y2Ba36gydF4y2Ba])。除了TSP,每天还监测暴露条件下的尼古丁和一氧化碳浓度。gydF4y2Ba
辛伐他汀交付gydF4y2Ba
辛伐他汀购自Sigma (St. Louis, MO, USA)。辛伐他汀为4 mg·mLgydF4y2Ba−1gydF4y2Ba用10%乙醇溶解原液作为药物载体。将100 μl乙醇、150 μl 0.1 N NaOH、750 μl PBS配制成10%乙醇1 mL。根据需要加入盐酸(0.1 N),使溶液pH值为7.0。gydF4y2Ba
大鼠给予20 mg·kggydF4y2Ba−1gydF4y2Ba辛伐他汀gydF4y2Ba通过i.pgydF4y2Ba.每天注射1)吸烟前7天,每天接触烟草烟雾前30分钟,或2)每天接触烟草烟雾前仅30分钟。gydF4y2Ba
我们选择这个剂量是基于我们和其他人之前发表的研究,这些研究表明这是一种有效的无毒剂量[gydF4y2Ba24gydF4y2Ba,gydF4y2Ba37gydF4y2Ba].很难推断人体的等效剂量是多少。在大鼠中,辛伐他汀在血液中的半衰期为4分钟,而在人类中为7小时[gydF4y2Ba38gydF4y2Ba].然而,辛伐他汀可能在组织中停留在治疗水平更长的时间。gydF4y2Ba
肺功能检查gydF4y2Ba
大鼠在暴露于烟草烟雾的最后一天后,用氯胺酮和Xylazine深度麻醉18-20小时。在颈椎气管上做了一个中线切口。一旦大鼠气管插管,插管随后连接到Scireq Flexivent (Scireq, Montreal, Canada)正压呼吸机,肺力学测量和数据采集系统。动物因琥珀胆碱而瘫痪。在模拟一个标准呼吸周期时,测量两次肺容量和压力,一次是导管对室内空气开放,一次是导管关闭。大鼠以90次呼吸频率通气gydF4y2Ba−1gydF4y2Ba潮气量为10 mL·kggydF4y2Ba−1gydF4y2Ba.肺力学评估采用强制振荡技术。测量呼吸系统输入阻抗,允许中央和周围肺力学之间的独特区别。采用“快照扰动”操作来测量整个呼吸系统(气道、肺和胸壁)的阻力、顺应性和弹性。gydF4y2Ba
组织准备gydF4y2Ba
在肺功能测试后,给予大鼠过量戊巴比妥钠。气管插管,左肺支气管结扎,右肺灌洗钙gydF4y2Ba2 +gydF4y2Ba/毫克gydF4y2Ba2 +gydF4y2Ba无汉克缓冲盐溶液(HBSS)。支气管肺泡灌洗(BAL)采用三进三出的模式,在气管内灌注和清除相同的HBSS,以丰富总细胞和蛋白质的恢复。BAL液(BALF)收集在管中并在处理前冷藏。灌洗后的肺叶冷冻在液氮中,-80°C保存直到使用。组织学上,松开左肺支气管的缝线,用4%多聚甲醛在30cm水压下充气1小时,然后将充气固定的肺浸泡在固定液中储存。gydF4y2Ba
组织学gydF4y2Ba
组织学使用横断面肺组织切片,其中包含暴露于过滤空气或烟草烟雾的大鼠的第一代和第二代肺内气道。使用切片机从石蜡包埋的组织块中切割5 μm厚的切片。切片放在载玻片上,在37°C下烘烤一夜,随后在甲苯中脱蜡,并通过分级的酒精溶液水化。对于苏木精和伊红染色,切片用以下美国MasterTech Scientific (Lodi, CA, USA)材料进行染色:Harris苏木精、分化溶液、蓝化溶液和伊红Y染色。切片在乙醇中脱水并用ClearMount(美国MasterTech Scientific Inc.)固定。gydF4y2Ba
BALF分析gydF4y2Ba
BALF以250倍离心gydF4y2BaggydF4y2Ba在4℃下浸泡10分钟,使细胞从上清液中分离。离心后,细胞颗粒在Ca中重悬gydF4y2Ba2 +gydF4y2Ba/毫克gydF4y2Ba2 +gydF4y2Ba——哈佛商学院。用台盼蓝排除法测定细胞悬液的细胞活力。使用标准血细胞计测定总细胞数。使用等份细胞悬液制备细胞旋切片(山东,匹兹堡,宾夕法尼亚州,美国),然后用Hema 3染色(Fisher Scientific,匹兹堡,宾夕法尼亚州,美国)。通过光镜下计数细胞离心机载玻片上的巨噬细胞、中性粒细胞、淋巴细胞和嗜酸性粒细胞的数量(每个样品计数500个细胞)来评估BALF中的细胞差异。每种细胞类型的比例乘以每mL的总细胞数,以确定每mL的中性粒细胞、巨噬细胞、淋巴细胞和嗜酸性粒细胞总数。嗜酸性粒细胞占总细胞的比例<0.01%,数量太少,无法进行统计分析,因此未报道。gydF4y2Ba
气道上皮损伤gydF4y2Ba
通过测量脱落的气道上皮百分比来评估气道上皮损伤。使用ImageJ软件(美国国立卫生研究院Bethesda MD)定量测量脱落的气道上皮细胞的长度,并在肺间二代苏木素和伊红染色的肺切片中按总气道上皮细胞进行划分。p值用Wilcoxon秩和检验确定。gydF4y2Ba
组织Western blot分析gydF4y2Ba
Western blot方法在B中描述gydF4y2BarattgydF4y2Baet al。gydF4y2Ba[gydF4y2Ba39gydF4y2Ba],并进行了以下修改。十二烷基硫酸钠聚丙烯酰胺凝胶电泳在还原条件下使用胞浆和膜组分(30 μg总蛋白)进行,并转移到聚偏二氟乙烯膜上。膜用1 μg·mL检测gydF4y2Ba−1gydF4y2Ba兔抗小鼠Ras (Cell Signaling Technology Inc., Danvers, MA, USA);1μg·毫升gydF4y2Ba−1gydF4y2Ba单克隆抗rho (EMD Millipore, Billerica, MA, USA);0.1μg·毫升gydF4y2Ba−1gydF4y2Ba单克隆抗e -cadherin (BD Bioscience, San Jose, CA, USA);0.001 mg·毫升gydF4y2Ba−1gydF4y2Baanti-HO-1 (ABCam, Cambridge, MA, USA);或兔抗小鼠α- actitinin IgG一抗,0.05% Tween in PBS (TBST), 40 ng·mL孵育gydF4y2Ba−1gydF4y2Ba辣根过氧化物酶(HRP)偶联山羊抗兔IgG (Pierce Biotechnology, Rockford, IL, USA)或HRP偶联山羊抗小鼠IgG (R&D Systems, Minneapolis, MN, USA)在TBST中5%干牛奶中的二抗。然后使用Western Lightning Plus-ECL底物试剂盒(PerkinElmer, Shelton, CT, USA)和Image Reader LAS-4000 V2.1 (Fuji Photo Film Co, Cypress, CA, USA)对蛋白条带进行可视化。使用ImageJ(美国国立卫生研究院)计算单个条带强度。gydF4y2Ba
胆固醇的测定gydF4y2Ba
如上所述,用匀浆器在匀浆缓冲液中手工匀浆大鼠肺。肺匀浆在5000×下离心gydF4y2BaggydF4y2Ba5分钟,清除大的组织碎片。收集上清液并将其搅拌成体积,用于测量蛋白质浓度和胆固醇。通过加入大量氯仿:甲醇(2:1)溶液,混合(通过涡流和超声),并进一步加入1 M NaCl溶液,使有机相(氯仿)与水相分离,通过离心(3000×gydF4y2BaggydF4y2Ba5分钟)发生。底相(氯仿)收集并使用快速真空干燥。脂质颗粒重悬于磷酸盐缓冲液(0.1 M磷酸钾pH 7.4, 50 mM NaCl, 5 mM脱氧胆酸,0.1% Triton X-100)中,超声处理至少1分钟以混合。然后测量胆固醇gydF4y2Ba通过gydF4y2Ba荧光测定法,Amplex红色胆固醇测定试剂盒(Invitrogen, Grand Island, NY, USA),根据制造商的说明。gydF4y2Ba
Rho和Ras GTPase分析gydF4y2Ba
使用分离缓冲液(250 mM蔗糖;20 mM HEPES, pH 7.4;2 mM EDTA;和3mm NaNgydF4y2Ba3.gydF4y2Ba)含有蛋白酶抑制剂(蛋白酶抑制剂(西格玛,1:100)和1 mM苯甲基磺酰氟)和磷酸酶抑制剂(磷酸酶抑制剂(西格玛,1:100),1 mM NagydF4y2Ba3.gydF4y2Ba签证官gydF4y2Ba4gydF4y2Ba,和1mm NaF)。肺组织均质是用dounce均质器手工进行的。粗匀浆最初以800倍离心gydF4y2BaggydF4y2Ba在4°C下加热5分钟。然后取出上清液,保存为全肺匀浆。取500 μL,以31000 ×离心gydF4y2BaggydF4y2Ba4℃30分钟,分离细胞质(可溶性)和膜(不溶性)成分。将该步骤的上清液保存为胞浆部分,剩余颗粒在500 μL分离缓冲液(与胞浆部分体积相同)中重悬。使用Micro BCA蛋白测定试剂盒(Pierce Biotechnology)测量每个样品的细胞质部分的总蛋白质浓度,并用于确定每个样品的蛋白质装载量。gydF4y2Ba
我们对我们的样品进行了Western blots,以确保细胞质部分没有被膜部分污染gydF4y2Ba反之亦然gydF4y2Ba.我们使用E-cadherin作为膜组分的指标,因为该蛋白仅在细胞膜中表达。我们的细胞质部分没有膜成分的证据,我们的膜部分肯定地证实了e -钙粘蛋白的表达。之前,我们也测量了甘油醛3-磷酸脱氢酶来确认胞质组分,进一步证实了我们的方法,但这些数据没有包括在内。gydF4y2Ba
统计分析gydF4y2Ba
为了提高统计显著性检验的有效性,在适当的情况下对具有倾斜分布的结果变量进行单向方差分析(one-way ANOVA)并进行Bonferroni校正以进行多次比较之前,将对数转换应用于结果变量。由于严重非正态分布,采用Wilcoxon秩和检验分析气道上皮损伤测量和血红素加氧酶(HO)-1密度分析。p值<0.05为有统计学意义。gydF4y2Ba
结果gydF4y2Ba
辛伐他汀需要一段预处理期来减少白细胞向肺的募集gydF4y2Ba
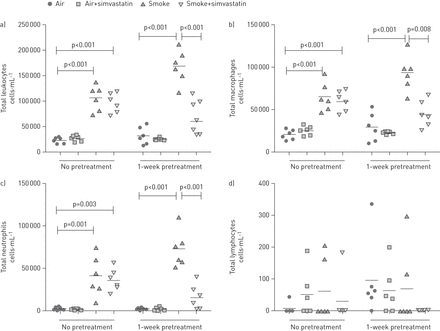
为了确定辛伐他汀是否可以预防或减少烟草烟雾诱导的肺部炎症,我们测量了BALF中恢复的白细胞。3天的香烟烟雾暴露显著增加白细胞、巨噬细胞和中性粒细胞的总数(gydF4y2Ba图1gydF4y2Ba)与暴露于过滤空气或暴露于过滤空气加辛伐他汀的大鼠相比。淋巴细胞占总细胞的<3%,暴露于烟草烟雾后淋巴细胞没有增加。与只接受吸烟治疗的自发性高血压大鼠相比,在吸烟暴露前1周接受辛伐他汀治疗的自发性高血压大鼠在暴露过程中减少了烟草烟雾诱导的肺总白细胞、巨噬细胞和中性粒细胞。相比之下,辛伐他汀与烟雾暴露日同时使用没有效果,这表明辛伐他汀的抗炎作用不是立竿而起的,或者需要一个暴露前治疗期才能获得最大的益处。gydF4y2Ba
在接触烟草前1周进行辛伐他汀预处理,并在整个接触时间内持续使用辛伐他汀,可减少烟草烟雾诱导的白细胞向肺的募集,而仅在接触烟雾日进行治疗没有效果。a)支气管肺泡灌洗液(BALF)中恢复的白细胞总数。b) BALF中恢复的巨噬细胞总数。c) BALF中恢复的中性粒细胞总数。d) BALF中恢复的淋巴细胞总数。所有组均采用单向方差分析和Bonferroni校正进行多重比较。gydF4y2Ba
辛伐他汀可预防气道炎症和上皮损伤gydF4y2Ba
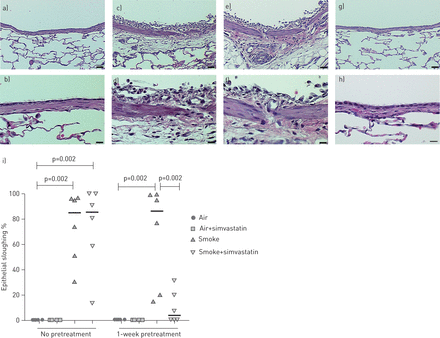
为了确定辛伐他汀是否可以预防或减少烟草烟雾对肺的损害,我们评估了苏木精和伊红染色的肺切片。通过测量脱落的气道上皮百分比来量化气道上皮损伤(gydF4y2Ba图2gydF4y2Ba).仅暴露于烟草烟雾的大鼠对气道有广泛的损伤,包括细胞浸润到上皮下间隙和上皮层明显剥蚀。气道内可见大量中性粒细胞和巨噬细胞。辛伐他汀治疗大鼠的肺组织在吸烟暴露日表现出与仅吸烟组的肺组织相同。然而,大鼠在吸烟前接受辛伐他汀治疗1周(并持续整个吸烟暴露期)可防止烟草烟雾引起的气道大上皮损伤(p = 0.02) (gydF4y2Ba图2gydF4y2Ba).6只大鼠中有4只几乎没有损伤或炎症迹象,与经过过滤的空气对照组没有区别。一只大鼠在上皮细胞中有少量细胞浸润,气道中有少量炎症细胞,另一只大鼠在肺部有明显的损伤和炎症,但其程度小于仅吸烟组的所有大鼠。gydF4y2Ba
暴露于过滤空气或烟草烟雾并用辛伐他汀治疗的自发性高血压大鼠支气管壁的上皮和炎症变化。仅暴露于烟草烟雾与显著的气道上皮损伤和脱落有关。如果在接触烟草烟雾前1周和接触烟草烟雾期间给予辛伐他汀预处理,则对烟草烟雾几乎具有完全的上皮保护作用,但如果仅在接触烟草烟雾时同时开始治疗,则无效。暴露于:a, b)过滤空气的大鼠肺间代第2代支气管气道的红atoxilin和伊红染色;C, d)烟草烟雾;E, f)吸烟加辛伐他汀,无预处理;g, h)吸烟加辛伐他汀,预处理1周。i)定量分析气道上皮脱落百分比,数据分析采用Wilcoxon秩和检验。A, c, e, g)比例尺= 25 μm。B, d, f, h)比例尺= 10 μm。gydF4y2Ba
辛伐他汀改变肺功能gydF4y2Ba
暴露于烟草烟雾3天没有显著改变气道阻力、呼吸系统顺应性或弹性(gydF4y2Ba图3gydF4y2Ba).然而,辛伐他汀预处理降低了肺顺应性(gydF4y2Ba图3 bgydF4y2Ba)及增加肺弹性(gydF4y2Ba图3 cgydF4y2Ba)与仅烟雾处理相比。仅在暴露日给予辛伐他汀未改变肺功能。gydF4y2Ba
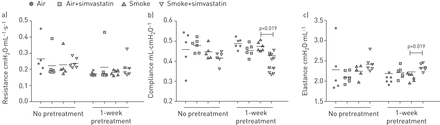
吸烟前1周及吸烟期间持续使用辛伐他汀可降低肺顺应性和增加肺弹性,而仅在暴露日使用辛伐他汀则无效果。a)抵抗b)顺从c)弹性所有组均采用单向方差分析和Bonferroni校正进行多重比较。gydF4y2Ba
辛伐他汀可以减肥gydF4y2Ba
只暴露于烟草烟雾或烟草烟雾加辛伐他汀的大鼠,无论辛伐他汀治疗何时开始,与相应的过滤空气暴露动物相比,体重显著下降(gydF4y2Ba表1gydF4y2Ba).辛伐他汀预处理与体重减轻有关,无论动物暴露在过滤空气或烟草烟雾中。事实上,暴露在烟草烟雾中并预先服用辛伐他汀的动物比任何其他组的体重减轻得更多。gydF4y2Ba
辛伐他汀未改变肺Rho或Ras GTPase膜定位gydF4y2Ba
他汀类药物的部分抗炎作用被认为是通过抑制GTPase膜定位而发生的[gydF4y2Ba10gydF4y2Ba,gydF4y2Ba19gydF4y2Ba,gydF4y2Ba24gydF4y2Ba,gydF4y2Ba25gydF4y2Ba,gydF4y2Ba40gydF4y2Ba].因此,我们测试了辛伐他汀是否减弱或抑制烟草烟雾诱导的Ras和Rho膜易位。在全肺匀浆中,我们未检测到烟雾或辛伐他汀诱导的Ras或Rho从细胞质到膜的易位变化(gydF4y2Ba图4gydF4y2Ba).gydF4y2Ba
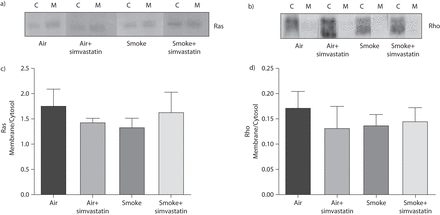
吸烟前1周的辛伐他汀治疗和暴露期间的持续治疗并没有改变胞质(C)和膜(M)组分之间Ras和Rho的定位。a)活性Ras蛋白的Western blot和c) Western blot密度测定的膜与胞质比。b)活性Rho的Western blot和d) Western blot密度测定的膜与胞质比。所有组均采用单因素方差分析。gydF4y2Ba
辛伐他汀没有改变全肺胆固醇水平gydF4y2Ba
甲羟戊酸途径向下游分支进入类异戊二烯法尼基焦磷酸盐和香叶酰焦磷酸盐,最终进入胆固醇。由于他汀类药物的主要作用是消耗血清胆固醇,而且在一些动物模型中,胆固醇与肺部炎症增加有关[gydF4y2Ba41gydF4y2Ba],我们评估了全肺总胆固醇水平。在我们的任何实验中,我们没有观察到任何吸烟或辛伐他汀引起的肺总胆固醇变化(gydF4y2Ba图5gydF4y2Ba).gydF4y2Ba
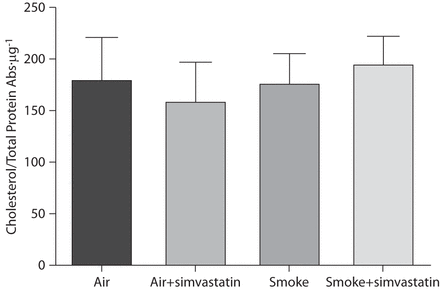
暴露于烟雾前1周及暴露期间持续使用辛伐他汀对大鼠全肺匀浆中总胆固醇无影响。测量全肺匀浆裂解物中的总胆固醇,并归一化为总蛋白质,如材料和方法所述。所有组均采用单因素方差分析。gydF4y2Ba
辛伐他汀可降低烟雾暴露大鼠的氧化应激gydF4y2Ba
我们探讨了辛伐他汀对氧化应激的影响,这可能是辛伐他汀预防气道损伤的机制。HO-1的表达随着氧化应激的增加而增加,它被认为是氧化应激的标志。在暴露于烟雾的大鼠中,暴露于烟雾前1周和暴露过程中辛伐他汀治疗显著降低了Western blot HO-1表达(gydF4y2Ba图6gydF4y2Ba).然而,与过滤空气对照相比,吸烟引起的增加没有达到显著性。辛伐他汀已被报道可增加HO-1 [gydF4y2Ba42gydF4y2Ba- - - - - -gydF4y2Ba47gydF4y2Ba],但它并没有增加暴露在过滤空气中的大鼠HO-1的表达,这表明这种影响在本研究中没有发生。gydF4y2Ba
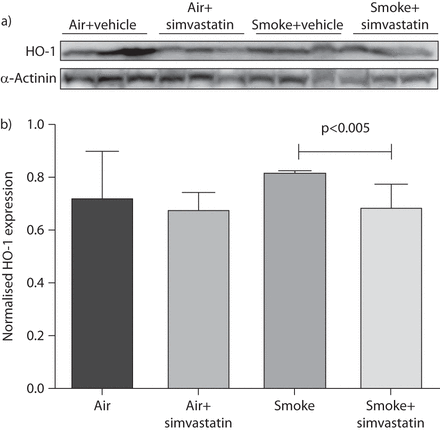
Western blot检测血红素加氧酶(HO)-1蛋白表达,作为氧化应激的标志物。a) 100 μg全肺匀浆总蛋白Western blot HO-1和α-肌动蛋白(对照)。b) HO-1表达归一化至α-肌动蛋白对照的密度分析。数据以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba.由Wilcoxon秩和检验确定的p值。gydF4y2Ba
讨论gydF4y2Ba
这项研究证明了他汀类药物的使用与预防烟草烟雾诱导的肺炎症细胞募集和急性支气管上皮损伤之间的因果关系。关于他汀类药物在烟雾性肺损伤中的保护性抗炎作用,我们发现了三个主要的新发现:1)烟草烟雾暴露前1周辛伐他汀预处理不仅减少了急性炎症细胞向肺的招募,而且完全防止了烟雾性急性气道上皮损伤和剥蚀;2)辛伐他汀的抗炎作用需要1周的前处理期,而辛伐他汀与烟雾接触同时使用时没有益处,这表明辛伐他汀抗炎作用的潜在机制不是立即的,必须在烟雾接触之前;3)这些结果与辛伐他汀对恢复、粘液积聚和气道重塑的影响无关,这些变化只发生在自发性高血压大鼠模型中长时间接触烟草烟雾时。gydF4y2Ba
上述结果表明,他汀类药物可能适用于多种支气管疾病患者,如COPD的气道疾病部分(gydF4y2Ba即。gydF4y2Ba慢性支气管炎和不仅仅是肺气肿)。目前尚不清楚辛伐他汀为何能保护自发性高血压大鼠免于急性气道上皮损伤。全身用辛伐他汀治疗可预防吸烟引起的损伤gydF4y2Ba通过gydF4y2Ba直接对上皮细胞产生影响或防止活化白细胞流入上皮细胞引起的继发性损伤。其他可能包括他汀类药物的抗氧化特性,这在吸烟所致损伤的情况下可能起主要作用[gydF4y2Ba48gydF4y2Ba- - - - - -gydF4y2Ba51gydF4y2Ba].我们调查了暴露于烟雾前和暴露期间用辛伐他汀治疗1周是否能降低氧化应激标志物HO-1。辛伐他汀可显著降低烟雾暴露大鼠HO-1的表达,支持辛伐他汀通过减少氧化应激来预防气道损伤的假设。然而,应注意不要过度解释这些结果,因为与过滤空气对照相比,烟雾诱导的HO-1表达增加并没有达到显著性。因此,在本研究中,尚不清楚氧化应激在多大程度上导致了气道损伤。此外,我们还不清楚氧化应激是直接由吸烟引起的,还是由中性粒细胞活化和随后的呼吸爆发引起的。gydF4y2Ba
他汀“预处理”似乎是辛伐他汀抗炎作用的关键过程,其效果取决于1周的预处理时间。我们推测预适应可能是由于gydF4y2Ba先天的gydF4y2Ba免疫细胞反应的调节[gydF4y2Ba52gydF4y2Ba,gydF4y2Ba53gydF4y2Ba],气道上皮水平促炎细胞因子/趋化因子基因表达降低[gydF4y2Ba54gydF4y2Ba,gydF4y2Ba55gydF4y2Ba]或间充质,或白细胞进入肺组织的血管招募减少[gydF4y2Ba56gydF4y2Ba- - - - - -gydF4y2Ba58gydF4y2Ba],以及其他机制。他汀类药物已被证明可以通过与淋巴细胞功能相关抗原(LFA)-1结合并阻止白细胞与血管内皮的高亲和性结合以促进移植到炎症组织中来抑制LFA -1。我们推测辛伐他汀不通过抑制LFA-1来阻止白细胞的募集,因为它不需要预处理。gydF4y2Ba
鉴于气道上皮在先天和适应性免疫反应中的中心作用[gydF4y2Ba59gydF4y2Ba,gydF4y2Ba60gydF4y2Ba],其中它是吸烟诱导的促炎反应的中心介质,需要进一步的研究来阐明他汀类药物对支气管上皮的保护作用。未来的工作需要确定辛伐他汀是作用于肺组织,还是直接作用于白细胞,或两者都起作用,以防止白细胞募集。gydF4y2Ba
通过证明辛伐他汀在粘液积聚和气道重塑发展之前减少了肺和气道损伤的炎症细胞募集,我们表明辛伐他汀可以独立于这些其他重要因素防止炎症细胞募集和急性气道损伤。我们的结果表明,他汀类药物在吸烟诱导的肺损伤(这可能是某些COPD表型的早期事件)中的短期益处并不依赖于减少粘液积聚和气道重塑。在治疗的10天内,他汀类药物在防止进一步的气道上皮损伤和白细胞招募方面有明显的保护作用。后者是急性COPD加重的关键组成部分,并可能(至少在一定程度上)解释为什么在大型人类流行病学研究中使用辛伐他汀与COPD加重风险降低和肺功能改善有关[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba18gydF4y2Ba].gydF4y2Ba
既往研究表明辛伐他汀可预防或逆转吸烟引起的肺气肿和逆转肺动脉高压[gydF4y2Ba29gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba],当长期吸入烟草烟雾超过16周时,辛伐他汀可减弱烟雾引起的小气道重塑[gydF4y2Ba31gydF4y2Ba].据我们所知,我们的研究首次报道了辛伐他汀全身预处理可抑制吸烟引起的支气管上皮损伤和剥蚀。在我们的模型中,辛伐他汀的有益作用发生在10天内,这是一个相对较短的时间周期。其他动物研究表明,他汀类药物对肺部有抗炎作用;然而,他汀类药物是在动物肺发育期间服用的,持续一个月(或更长时间)[gydF4y2Ba21gydF4y2Ba,gydF4y2Ba29gydF4y2Ba,gydF4y2Ba31gydF4y2Ba].gydF4y2Ba
他汀类药物的抗炎作用被认为是部分介导的gydF4y2Ba通过gydF4y2Ba抑制类异戊二烯合成。因此,我们研究了辛伐他汀是否减少了可用的法尼基焦磷酸盐和香叶基焦磷酸盐的池,从而分别减少了异丙烯基或膜结合的Ras和Rho的比例。我们期望在我们的均质大鼠全肺中看到吸烟诱导的Ras和/或Rho细胞膜易位(或激活)。然而,我们没有检测到吸烟诱导或辛伐他汀诱导的这些GTPases的转位(在细胞质和膜组分之间),这表明任何吸烟诱导的变化可能是短暂的、微妙的或局限于肺内的某些细胞和/或室室,而在整个肺匀浆中无法检测到。考虑到这些可能性,测试是否与香叶酰香叶酰焦磷酸盐和法尼基焦磷酸盐联合治疗,分别在Rho和Ras激活上游的类异戊二烯分子逆转辛伐他汀的作用可能是确定Rho和Ras激活是否调节辛伐他汀的保护作用的最佳方法。gydF4y2Ba
接受辛伐他汀预处理并暴露于烟草烟雾的大鼠肺顺应性降低(并增加肺弹性)(gydF4y2Ba图3gydF4y2Ba).在人类中,COPD通常表现为肺气肿引起的异常高的肺顺应性,并导致肺弹性反冲的丧失。因此,COPD患者通常希望恢复正常或降低肺顺应性。然而,急性烟雾暴露并不能模拟这种人类病理生理学。我们推测肺顺应性的降低可能是由于肺泡表面活性物质产生的减少[gydF4y2Ba28gydF4y2Ba],而不是由于辛伐他汀的抗炎作用,因为与过滤空气对照相比,3天的烟雾暴露并没有改变依从性。此外,辛伐他汀对滞留肺泡细胞中局部胆固醇浓度的任何改变也未被我们的实验检测到;因此,我们不能将其与胆固醇联系起来gydF4y2Ba本身gydF4y2Ba.gydF4y2Ba
我们惊讶地发现,在“预处理”实验臂中,在20 mg·kg时出现了减肥效果gydF4y2Ba−1gydF4y2Ba辛伐他汀剂量,因为文献和我们之前的工作都没有揭示任何证据表明,在这个剂量或更高剂量下,大鼠和小鼠的毒性或总体重减轻[gydF4y2Ba24gydF4y2Ba,gydF4y2Ba37gydF4y2Ba].人类没有相似之处。根据过去30年持续使用他汀类药物的临床报告,他汀类药物的使用不会导致人类体重减轻。gydF4y2Ba
这项工作强调辛伐他汀是一种潜在的治疗烟草烟雾引起的炎症性肺病(如COPD)的新疗法。我们证明辛伐他汀可减弱急性烟草烟雾诱导的白细胞向肺的募集,并进一步表明辛伐他汀预处理1周几乎完全可以防止烟雾诱导的急性支气管上皮损伤。他汀类药物的保护作用可能是由于白细胞-气道上皮细胞相互作用时对肺或粘膜表面的直接作用[gydF4y2Ba37gydF4y2Ba,gydF4y2Ba61gydF4y2Ba].我们认为辛伐他汀(可能还有其他他汀类药物)有潜力成为COPD的重要辅助疗法,添加到当前的标准吸入器方案中。还需要进一步的动物实验来研究潜在的作用机制。此外,正在进行的哮喘和COPD临床试验也将引起高度兴趣。gydF4y2Ba
脚注gydF4y2Ba
支持声明:本研究的资助来自gydF4y2BaCTSC K12奖KL2 RR 024144gydF4y2Ba,gydF4y2Ba美国哮喘基金会gydF4y2Ba09 - 0269,gydF4y2Ba烟草相关疾病研究计划gydF4y2Ba(TRDRP) 18KT-0037和18XT-0154。gydF4y2Ba
利益冲突:可以在本文的在线版本中找到信息披露gydF4y2Bawww.www.qdcxjkg.comgydF4y2Ba
- 收到了gydF4y2Ba2012年3月9日。gydF4y2Ba
- 接受gydF4y2Ba2012年10月8日。gydF4y2Ba
- ©2013人队gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba