摘要
干扰素(IFN)-γ释放试验(IGRAs)可能是检测潜在感染的最准确试验结核分枝杆菌感染,但IGRAs是劳动密集型的,样本很难远距离运输。IFN-γ诱导蛋白(IP)-10的表达水平比IFN-γ高100倍,IP-10释放试验的性能与IGRAs相当。本研究的目的是探索基于干血浆斑点(DPS)的新型IP-10释放测定的诊断潜力。
ELISA检测血浆和DPS中IP-10和IFN-γ的存在。IP-10的血浆和DPS检测诊断算法是在一个由60名结核病患者和59名健康对照组组成的培训队列上开发的。在一个由78名结核病患者和98名健康对照组组成的验证队列中评估了诊断准确性。血浆在西班牙进行测量,DPS样本通过常规邮政服务送往丹麦进行分析。
IP-10是血浆和DPS中容易检测的,并且相关性是优异的(R2= 0.95)。DPS和等离子体中的Quantiferon-TB金管(QFT-TB)和IP-10分别具有相当的灵敏度(分别为78%,82%和84%),特异性(分别为100%,97%和97%)和不确定的速率(p> 0.55)。
基于dps的IP-10测试具有与QFT-TB相当的诊断准确性,可以发送样本通过传统的邮件在不影响结果的情况下进行长距离的分析。
介绍
干扰素(IFN)-γ释放试验(IGRAs)可能是对潜伏结核感染(LTBI)最准确的诊断试验[1].市场上有两种IGRA,T-SPOT.TB(英国阿宾顿牛津免疫技术公司)和QuantiFERON TB金管(QFT-TB;澳大利亚查德斯通Cellestis)。这两项试验都利用了敏感T细胞的能力,即当用来自细胞的肽刺激时,其释放IFN-γ的能力结核分枝杆菌- 特异性抗原在体外.虽然第一方法测量反应性淋巴细胞的频率在外周血单核细胞部分,后者措施释放的IFN-γ在全血的血浆浓度[2,3.].IGRAs解决了结核菌素皮肤试验的两个主要局限性:对接种卡介苗的受试者的低特异性和操作困难,试验必须在接种后2-3天阅读[4].
IGRA的实施具有主要障碍,特别是在低资源环境中[2]: T-SPOT。TBrequires access to skilled technicians to separate cells and to set up the assay for incubation. The window of time between blood sampling and laboratory analysis is short and requires that the blood be transported to the laboratory at ambient temperature. For the QFT-TB, incubation is done directly in the blood collection tubes, and following a centrifugation step, samples can be transported refrigerated or frozen. Transport of these samples requires a cold chain and safety precautions must be considered, as the plasma is potentially infectious. Simpler, safer and more flexible solutions are needed in both high- and low-resource regions.
我们利用生物标志物IFN-γ-诱导蛋白(IP)-10挑战了这些障碍。IP-10是一种在IGRA中与IFN-γ协同表达的趋化因子[5].26项临床研究评估了IP-10释放分析的诊断准确性,并确定IP-10释放分析的表现与基于IFN-γ的IGRA相当[5- - - - - -7]与T细胞衍生的IFN-γ相比,IP-10主要由抗原呈递细胞分泌。IP-10的表达受到T细胞信号下游多种信号的刺激,主要是IFN-γ和肿瘤坏死因子-α,还有白细胞介素(IL)-2、II型IFN、IL-27、IL-17/IL-23和IL-1β[6,8- - - - - -10],通过一个正反馈回路支持病原体特异性的适应性免疫反应[11].在体外, IP-10的释放水平是IFN-γ的100倍[12,这使得样品的储存和运输有了可选的方法。
血液或血浆印迹到滤纸已被证明是用于样品的小体积的用于生物标志物的分析的收集,运输和储存安全,健壮和方便的方法,例如[13].为了准备这项研究,我们开发并验证了一种ELISA检测方法,用于检测未刺激、QFT-TB和巨细胞病毒刺激全血的血浆样本、干血和血浆斑点(分别为DBS和DPS)的IP-10 [12].
本研究的目的是研究是否使用全血刺激特异性抗原的IP-10释放试验结核分枝杆菌存储为DPS可用于诊断结核分枝杆菌感染。我们将该方法应用于两组患者确诊结核病(TB)和健康对照。我们定义了基于第一组患者和控制的截止点并建立了一种诊断算法;随后,我们在其他情况下评估了测试性能和控制。
方法
研究参与者
为了建立截断和诊断算法,我们纳入了一个训练集,其中包括哥本哈根大学医院(丹麦Hvidovre)的60名微生物学上确诊的活动性结核病患者和59名健康的未暴露的丹麦对照(表1).在哥本哈根一所高中进行的一项更大的接触调查中,对照组被纳入其中。本调查显示非同窗的接触非常有限,我们纳入了非同窗无旅行、家庭或接触暴露的对照组。在验证组中对测试成绩进行了评估,该验证组包括来自西班牙巴塞罗那的78名微生物学确诊结核病患者和来自西班牙巴伦西亚的107名健康中学生。对照组是瓦伦西亚中学学生常规筛查的一部分,大多数学生(61%)是新移民或新移民的子女。连续纳入学生,排除已知的结核病暴露、既往结核病治疗或病因不明的淋巴结炎(n = 9 / 107筛查)。用于验证的患者包括78名患者和98名健康对照。
血液刺激和QFT-TB检测
所有参与者都进行了QFT-TB测试。根据QFT-TB包装插入物测定IFN-γ水平,多余的血浆储存在-80°C,用于IP-10测量和滤纸上的点胶。
滤纸的制备及贮存
QFT-TB刺激的血浆上清(25 μL)在滤纸上(903 Protein Saver™卡片;在环境温度下干燥4小时,并储存在带有干燥剂的塑料袋中。训练集样本在5°C滤纸上保存10天后进行分析;验证集样品在运输前在5°C下保存2-4天通过在环境温度下从西班牙到丹麦的正常2天邮政服务,用于分析。分析在到达后2天进行。
IP-10 ELISA(血浆和DPS)
我们使用了IP-10检测的内部ELISA [12].简言之,我们开发了大鼠和小鼠的杂交瘤细胞系产生单克隆抗体(mAbs)的特异性为IP-10。单克隆抗体合并于夹心ELISA将其用于血浆和DPS在QFT-TB样品中IP-10应答的范围进行了优化。
对于该测定,血浆样品稀释33×测定缓冲液中与辣根过氧化物酶(HRP)缀合的单克隆抗体检测(相当于每100μLELISA 3μL等离子体孔)。对于的DPS中,两个圆盘5.5毫米直径是从DPS的中心使用标准办公纸穿孔机(Impega德福,UK)冲孔,DPS圆片放置在ELISA板孔中,加入100μL测定缓冲液中的溶液。使用相同的协议稀释的血浆样品和DPS光盘进行了分析,IE。室温孵育2小时,洗三次。HRP-substrate(三甲;加入Trichem, Roskilde, Denmark),平板显示30分钟,酶反应停止,在450 nm处读取吸光度,在630 nm处减去读数。用每个重复的酶联免疫吸附测定板生成的标准曲线计算浓度,并用期望浓度与平均光密度的线性回归进行拟合。检测血浆中的IP-10,取平均值进行进一步分析。DPS样品中的IP-10由单次测量确定。ELISA检测结果线性范围为2.5 ~ 600 pg·mL−1; 有关ELISA性能特征的完整说明,请参阅[12].IP-10的血浆水平在乘以33后表示,以补偿稀释,DPS水平表示为每两个5.5 mm圆盘检测到的pg(每两个圆盘检测到的pg)。所有样本的分析均不考虑临床信息。
物流
所有ELISA试剂均在丹麦哥本哈根制备。在西班牙巴塞罗那(验证集)和哥本哈根(训练集)测定血浆样本。DPS仅在哥本哈根进行了测量。
道德
这项研究得到了哥本哈根伦理委员会(KF-01-278477)和巴塞罗那普约尔大学医院伦理委员会的批准。
统计数据
使用非参数配对和非配对方法(Wilcoxon符号秩检验、Mann-Whitney u检验和Spearman)比较生物标志物水平。采用受试者工作特征(ROC)曲线分析(敏感性高,特异性损失小)设置临界值,采用麦克尼马尔检验和κ-统计学方法比较试验的一致性。在遗漏不确定应答者后计算敏感性和特异性。p值<0.05被认为是显著的。采用SAS 9.2 (SAS Institute Inc., Cary, NC, USA)和GraphPad Prism 5.0 (GraphPad Software Inc., La Jolla, CA, USA)进行分析。
结果
比较血浆和DPS中的IP-10和使用训练集样本定义诊断测试的截止点
我们比较了由60名活动性结核病患者和59名健康对照组组成的训练队列中的IP-10 DPS和血浆样本。与对照组相比,结核患者年龄更大,62%的患者出生在西欧以外的国家(临床数据可在表1).结核患者的nil水平和抗原诱导的IP-10和IFN-γ反应明显高于对照组,而有丝分裂原反应较低(表2).有等离子体和DPS IP-10(R之间的良好的相关性2= 0.95)(图1),而IFN-γ与IP-10的相关性仅为中等(r2<0.48; 数据未显示)。

干扰素-γ-诱导蛋白(IP)-10在干血浆斑点(DPS)和血浆中检测的比较。比较了60例活动性结核病患者和59例健康对照者的DPS和血浆样本、抗原和有丝分裂原样本。血浆与DPS IP-10 (Spearman r2= 0.95)。
我们使用ROC曲线分析比较了三种方法的诊断潜力,发现曲线下可比面积(auc): IP-10血浆、IP-10 DPS和QFT-TB分别为0.95、0.94和0.89 (图2),两种测定方法之间无显著差异。ROC分析结果显示:IP-10血浆2.3 ng·mL为特异性高的临界值−1(敏感性87%,特异度100%)和IP-10 DPS 105 pg / 2椎间盘(敏感性87%,特异度100%)。作为比较,这些数据中QFT-TB的最佳临界值为0.21 IU·mL−1(敏感性83%,特异性100%)。对在QFT-TB测试算法的选项中,我们定义了一个不确定测试的截止。我们选择了在对照组中未导致不确定应答的最高丝裂原应答值为不确定检测的临界值:1.5 ng·mL−1IP-10在等离子和71 pg每2盘IP-10在DPS。对于IFN-γ结果的分析,采用制造商推荐的QFT-TB算法。
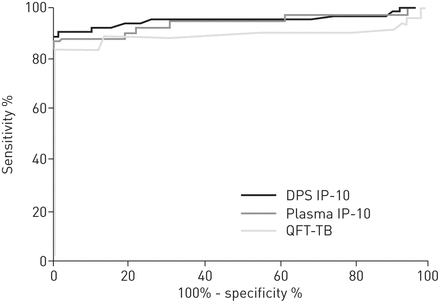
接受者操作特性曲线分析。干扰素(IFN)-γ和IFN-γ诱导蛋白(IP)的抗原特异性释放-10训练组样品中进行了比较。IP-10是使用的QuantiFERON-TB金中筒(QFT-TB)ELISA在干燥的血浆点(DPS)和血浆样品,IFN-γ检测等离子体。曲线下面积相当,为0.95,0.94和0.89对IP-10血浆,分别IP-10和DPS QFT-TB,。
使用临床样本验证基于dps的检测的诊断性能
我们在一个新的队列中验证了DPS和血浆IP-10检测算法的诊断潜力,该队列包括78例经培养证实的活动性结核病患者和98例健康对照。患者年龄大于对照组(p<0.0001),且男性患者较多(p<0.0001)。17例患者有合并症(表1).除了两种对照之外的TST测试,其中19%是TST阳性(用于非疫苗的截止物10mm,对于BCG接种疫苗的受试者为15mm),61%是BCG接种疫苗(表1).
血浆中IP-10水平与滤纸中IP-10水平之间具有极好的相关性(r2=0.93;p<0.0001(数据未显示)。两种方法得出的IP-10和血浆IFN-γ的ROC曲线的AUC相似,为0.89–0.91(数据未显示)。
测试精度和一致性
我们将IP-10阳性和不确定检测结果的临界值应用到验证集,发现这三种检测具有相当的敏感性(78-84%)、特异性(97-100%)和不确定性(对照组<1%,结核病患者中QFT-TB、IP-10 DPS和IP-10血浆检测分别为5%、10%和8%;p > 0.55) (表3).为了比较,我们还应用了队列特异性最佳截止为QFT-TB 0.21 IU·毫升−1;敏感性为82%(74个受试者中的61个),特异性为97%(98个受试者中有95个);没有任何对照和四(5%)的TB患者的结果是不确定的结果。DPS和等离子体IP-10测试之间的协议非常高(κ= 0.91; 95%CI 0.88-0.99),高于QFT-TB试验和等离子体中的IP-10之间的协议(κ= 0.83; 95%CI之间0.75-91)。将等离子体IP-10与QFT-TB测试结果相结合(IE。在任一种或两种试验的阳性结果被认为是阳性;不确定如果一个测试是不确定的,而另一个不为正),而不在特异性的折衷显著增加的灵敏度到89%(P = 0.032)。
讨论
我们研究了将用户友好的滤纸方法与IP-10释放试验相结合的可能性,目的是诊断感染结核分枝杆菌.我们证明,可以从滤纸上的QFT-TB管中的血浆干燥等离子体,在字母中在环境温度下运输样品,并在不损失信号强度或诊断准确度的情况下提取诊断信息。
IP-10是用于ICN-γ的新出现的替代生物标志物,用于细胞介导的免疫应答测定,例如IGRA [5,6,15].这项研究的结果支持了最近的一系列论文,这些论文表明,在结核病患者中,IP-10释放检测具有与QFT-TB相当的诊断准确性与控制(6,16,17].其他的研究表明,IP-10在HIV感染患者提供更好的诊断性能,独立的CD4计数低的[18- - - - - -22]; 自身免疫性疾病患者[23];在年幼的孩子[24- - - - - -27];以及被诊断患有其他细菌或病毒感染而怀疑患有活动性结核病的病人[16].所有研究中一致的发现是,IP-10和IFN-γ应答者之间存在轻微的不一致,这开启了结合标志物以提高敏感性的可能性,似乎不影响特异性[16,17].
滴入血液到用于诊断目的滤纸的概念是由Guthrie和苏西在1963年引入的作为一种工具,以屏幕为在大群体新生儿[代谢性疾病13].干燥的血液或血浆基质稳定许多分析物,并允许测定两种表型(如。生物标记物)及基因型(如。多态性)来自单一样本[13,28].运输用滤纸干燥的样本被认为是安全的[13和Whatman 903滤纸是美国食品和药物管理局批准的(二类医疗器械)。使用DBS进行新生儿筛查是全世界的标准护理[29]滤纸技术还用于许多国家的丙型肝炎和艾滋病毒病毒载荷监测和HIV筛查,包括南非[28].
我们开发了一种基于滤纸的方法,使用简单的ELISA法检测受激全血和未受激全血中的IP-10。为了优化抗原刺激样品中IP-10的检测,我们将血浆大量稀释×33倍(每个酶联免疫吸附试验板孔3 μL血浆)。这种低体积产生的信号强度与两个DPS或DBS光盘产生的IP-10信号以及用于QFT-TB ELISA中IFN-γ检测的50 μ l血浆样品相当。我们最近回顾了22个临床研究的IP-10释放检测诊断感染结核分枝杆菌.我们发现IP-10已经被五种非常不同的IP-10测定法检测到,并且在×2到×20的样品稀释中[6]这种异质性限制了分析之间的比较,并要求在现场达成共识。滤纸法实现的简单样品传输非常适合国际合作和更大的多中心研究,并应导致IP-10释放分析的更好质量和可比性研究。
年代kogstrand和他的同事们(30.,31使用基于Luminex的多重方法,在干燥的血斑中测量细胞因子和趋化因子的测量,并验证了使用鞋跟血样的新生儿的炎性病症的一系列研究中的临床应用。最近,小型概念证据评估了使用QFT-TB刺激血液的DBS样品进行多重测定[32].该研究表明,QFT-TB阳性患者和QFT-TB阴性患者之间的IFN-γ反应存在显著差异,但大多数样本(也来自结核病患者)低于本试验的定量下限[33].我们尝试使用QFT-TB ELISA从DPS样品中提取IFN-γ信号,但也未能检测到可靠的响应[12].这些结果的可能的解释是,滤纸样品中获得血浆的低容积含有太少IFN-γ可靠的决心。IP-10表达在100倍高的水平,因此更适合于这种方法[12,34].
局限性
我们的长期目标是为LTBI制定一个简单的测试,但由于LTBI没有真正的黄金标准,我们将患有活跃的TB患者作为代理结核分枝杆菌感染。这种方法提供了一个牢固的黄金标准感染,但是活动性结核病患者疾病可能损害干扰素-γ和IP-10对有丝分裂原的反应,也可能抗原,为积极的测试结果可能会导致不准确的截止值如果用于LTBI或免疫抑制患者,如。感染爱滋病毒的病人[16,35,36].然而,如在详细由Z描述侯et al。[37],新的诊断测试(或诊断算法)评估应该在几个步骤中进行;第一上选择的人群,以确保下(用于测试)的最佳条件的敏感性和特异性的评估之前可以在临床环境中被应用的测试,如。一项前瞻性研究评估测试的预测值。在评估新的测试对潜伏性结核感染的“金标准问题”是固有领域[38],所有LTBI检测,包括QFT-TB检测,均使用类似的病例对照设计进行了评估[39].
我们在培训集中的样本规模仅包括119名患者和控制。这种相对较小的队列将导致对截止值的不精确评估。但是,正如我们在培训和验证集之间发现的相当诊断准确性,尽管从非常不同的设置控制,我们怀疑这种风险受到限制。
此外,在训练和验证队列中,患者和对照组之间的年龄差异是显著的。这些差异可能会影响结果,但我们认为影响是次要的,因为我们最小的控制青少年(而不是< 5岁,只有年龄记录受损IGRA)的性能,因为IP-10似乎更少受到年轻而干扰素-γ(24,27].然而,还需要进一步的研究,这些研究的设计应允许对阳性检测结果的临界值进行调整。与类似患者组和对照组的其他研究相比,我们观察到与QFT-TB相比,IP-10应答不确定的患者数量更高[16,17];这很可能反映了在我们的研究中一个不确定的测试结果相对较低的阈值。以前对IP-10的研究使用任意值来模拟QFT-TB的速率[6],而设置QFT不确定截止的方法,据我们所知,未发表[39,40].在这项研究中,我们设置了不确定值的临界值,刚好低于在健康对照组队列中观察到的最低IP-10丝裂原反应;这是为了优化敏感性(通过认为假阴性反应的患者是不确定的)而不影响成本效益(认为真实阴性对照是不确定的)。较高的截止值呈现与QFT-TB相同的不确定率(数据未显示)。有趣的是,对于不确定的IP-10测试结果,较低的阈值并没有影响结合IP-10和QFT-TB所看到的准确性的提高[16- - - - - -18,41,42].还需要进行进一步的研究,以评估和可能调整这一界限,并在检测结果为假阴性/不确定的情况下评估发展为活动性结核病的风险。
这项研究的发现还需要在其他人群中得到证实,如。潜在的与活动性结核病;迫切需要评估该方法在HIV感染者和儿童中的表现,以及基于IFN-γ和IP-10的IGRAs阳性和阴性预测值的前瞻性评估。
透视
滤纸方法用于血浆样品的存储和运输,可以简化和集中IGRA诊断概念。IP-10可在DBS样品中检测到与DPS样品相当的水平,因此无需离心步骤即可制备受激样品[12]使用更简单的测试格式,本地实验室的工作量和要求将使IP-10释放分析更容易和更便宜地建立,如。对于低容量的用户,和外围设备或资源受到限制的设置。重要的是,简单的样品运输允许分析的更好的质量控制,如。采用参考实验室功能的可能性。用于滤纸和样品分析的全自动高通量系统是新生儿筛选的标准,可以适用于IP-10测量[29].自动化分析显著降低了与执行手动ELISA和ELISPOT分析相关的人为错误和分析可变性风险,并提高了分析精度和诊断准确性。
结论
本研究描述并验证了一种用于简化IP-10释放测定中的样品处理的方法,用于诊断结核分枝杆菌感染。我们证明,IP-10在滤纸上干燥的等离子体中是稳定的,可以用普通邮件长距离发送进行分析,显然不会影响结果。此外,该研究进一步证明,IP-10释放测定法是IGRAs的有效替代方法,而且使用滤纸方法的IP-10释放测定法具有操作上的优势。
致谢
笔者想感谢奥雅纳安德森(临床研究中心,哥本哈根大学医院,哈维德夫,哥本哈根,丹麦)的支持,并提供了框架;和TB-NET(Borstel,德国)用于促进跨欧洲研究合作,否则这项工作就不会发生。
脚注
支持声明:这项工作得到了丹麦国家先进技术基金会(003-2011-5)、哥本哈根首都大区、丹麦肺科协会、丹麦科学、创新和高等教育部、Hvidovre医院临床研究中心和Lundbeck基金会(R32-A1081)(丹麦)的支持。Jose Domínguez是由西班牙巴达拉那的卡洛斯三世研究所的Miguel Servet项目资助的。
利益冲突:可以在本文的在线版本旁找到披露www.www.qdcxjkg.com.
本文于2016年4月进行了修改,以纠正许可证信息中的错误。
- 收到了2012年8月17日。
- 接受2012年9月27日。
- ©ERS 2013
ERJ开放文章是开放获取的,并根据(188滚球软件知识共享署名非商业许可3.0)















