编辑器:
我们最近发现,阿奇霉素每日服用1年减少慢性阻塞性肺疾病急性加重的频率(AECOPDs)受试者选择有发作的风险增加(1]。既然阿奇霉素有潜在的不利影响,识别患者最有可能受益可能有用的靶向药物治疗。因此,我们在试验,包括substudy前瞻性设计,以确定等离子体水平条目,或改变水平在3个月的四个血液生物标志物,与改善临床应对有关阿奇霉素相比安慰剂。我们选择研究生物标志物的炎症通路可能与慢性阻塞性肺疾病(COPD)包括c反应蛋白(CRP)、白介素6 (IL),引发和可溶性肿瘤坏死因子受体75 (sTNFR75)。
父试验包括1142例患有慢性阻塞性肺病的患者随机接受阿奇霉素(每天250毫克口服)或安慰剂(1:1)为12个月(ClinicalTrials.govNCT00325897)[1]。丰富我们的人口为对象更容易有AECOPDs,我们要求受试者使用系统性皮质类固醇,访问一个急诊或住院AECOPD前12个月或使用连续补充氧气2]。我们必修科目免费AECOPDs或其他急性疾病≥4周之前将报名与已知的科目充血性心力衰竭(CHF)和临床定义的支气管扩张。主要结果是时间第一次AECOPD定义为“一个复杂的呼吸道症状(增加或新发病)超过下列之一:咳嗽、痰、气喘、呼吸困难、胸闷或至少3天的时间需要抗生素治疗或全身性类固醇”(2]。我们监控参与者在后续AECOPDs诊所访问1个月,3、6、9和12和每月电话联系。
我们获得了等离子体在招生和3个月的治疗后,进行ELISA对CRP、il - 6,引发sTNFR75。我们使用Cox比例风险模型(由诊所按父研究分层)先将生物标志物水平与时间AECOPD配对和未配对t在意向性治疗基础上确定阿奇霉素影响生物标志物水平(自然对数转换)与安慰剂相比。然后,我们控制了以下潜在的混杂因素:年龄、性别、吸烟状况、慢性支气管炎的症状,使用氧气,吸入型皮质类固醇激素、基线用力呼气量在1 s (FEV1)%预测和遵从性(通过药丸计数)。我们使用交互条款(生物标志物×治疗分配)来识别与修改相关的生物标记物的风险由治疗AECOPD。
我们获得血液样本在1037年入学的1142例(91%)的父母试验(1](41%的全球倡议慢性阻塞性肺疾病第三类,21%的吸烟者和47%的慢性支气管炎定义为对圣乔治呼吸问卷)的反应。血液样本也可用890年(78%)在3个月。
受试者的生物标志物分析,服用阿奇霉素与更长的时间比安慰剂第一恶化(HR 0.71, p < 0.001),类似于父发现审判。高血浆sTNFR75水平在招生与下降时间先恶化(HR 1.21海拔每1/2 sTNFR75, p = 0.020),当对诊所进行了统计处理。这一发现坚持当控制了年龄、性别、经常吸烟,使用氧气或吸入型皮质类固醇激素,初始FEV1% pred,慢性支气管炎和遵从性(HR 1.12海拔每1/2 sTNFR75, p = 0.017)。无显著关联观察CRP, il - 6引发以报名时间先恶化在单变量或多变量分析(p > 0.05)。
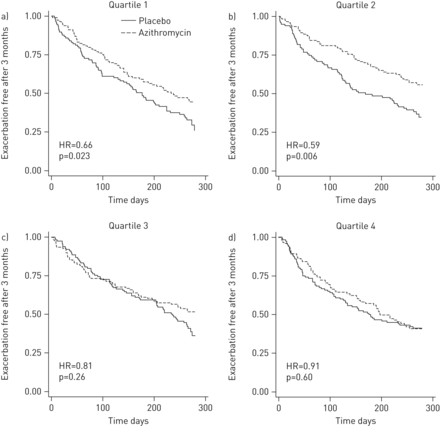
sTNFR75浓度在招生没有预测对阿奇霉素(p = 0.89的交互项cox比例风险模型虽然控制了诊所,p = 0.74虽然控制了诊所和其他潜在的混杂因素)。然而,在预先确定的变化分析生物标志物水平随着时间的推移,sTNFR75浓度下降3个月确定受试者得益于阿奇霉素后3个月的时间,第一次恶化是长的比接受安慰剂的控件(890例与生物标志物数据在招生和3个月;p = 0.02的交互项虽然控制了诊所,p = 0.018,诊所和其他潜在的混杂因素的控制)。sTNFR75策划改变的四分位数,我们发现任何sTNFR75下降水平介于0和3个月(较低的两个四分位数)确定主题在他阿奇霉素优于安慰剂后3个月(图1 a和b)。我们没有发现其他任何其他生物标记物之间的相互作用和对阿奇霉素的回应。
阿奇霉素对时间的影响首先恶化改变可溶性肿瘤坏死因子- 75 (sTNFR75)水平在3个月。890受试者的生物标志物在招生和3个月的数据。a、b)之间的任何sTNFR75水平下降0和3个月确定主题阿奇霉素优于安慰剂3个月后的是谁。c, d)受试者sTNFR75水平没有明显下降,阿奇霉素并不比安慰剂。数据中心的调整。发现存在而调整为中心和其他潜在的混杂因素,如。目前年龄、性别、吸烟、氧气使用吸入皮质类固醇的使用,用力呼气量在i1年代,支气管炎和遵从性。四分位数1:在3个月大sTNFR75下降;四分位数2:温和下降sTNFR75 3个月;第三四分位数:适度增加sTNFR75 3个月;四分位数4:大sTNFR75增加3个月。人力资源:风险比。
肿瘤坏死因子(TNF)可以绑定两个受体,肿瘤坏死因子受体1型(CD120a, p55/60和TNFR55)和肿瘤坏死因子受体2型(CD120b, p75/80和TNFR75),我们将这里称为TNFR55 TNFR75,分别。TNFR55表达在大多数组织中,而TNFR75只存在于免疫系统的细胞和内皮细胞3),特别是,标志着“非经典的”族群的单核细胞(4]。功能,可溶性肿瘤坏死因子受体可能是内源性抑制剂的影响TNF-α[5]或稳定的生物活性TNF-αhomotrimeric防止分裂的肿瘤坏死因子分子活性单体(6]。之前的研究表明,在慢性阻塞性肺病sTNFR75 sTNFR75水平可以作为标记TNF-α水平(7在稳定的慢性阻塞性肺病(),sTNFR75水平升高7)和sTNFR75水平升高在慢性阻塞性肺病急性加重但降低分辨率的恶化8]。最后,sTNFR75可以升高等条件,会使得COPD的瑞士法郎(9)或支气管扩张(10]。在这项研究中,TNF-α低于推荐的动态范围的测定(3.9 pg·-250毫升−1在大部分试验样品。因此,我们选择研究sTNFR75。我们的数据扩展测量的实用程序在慢性阻塞性肺病sTNFR75确认其价值作为未来风险恶化的预后生物标志物在大型前瞻性研究,通过建立其价值减少的生物标志物在AECOPD风险一个随机试验。sTNFR75水平可以影响在某些科目在我们试验由于共病瑞士法郎或支气管扩张(尽管是亚临床历史是用来排除患者条件条目),因为伴随药物(如。使用他汀类药物或β-blockers可以降低sTNR75水平设置的心脏疾病)或者如果sTNFR75水平升高坚持任何受试者可能有加重>报名前4周。然而,治疗分配是随机的临床试验和无边无际的并发症患者或药物的影响应该随机安慰剂与阿奇霉素。
总之,在前瞻性设计生物标志物分析病人参加一项大型的随机实验,我们发现高sTNFR75水平报名与风险增加有关AECOPDs exacerbation-prone科目,sTNF75下降与治疗有关阿奇霉素的有利影响。如果可以在将来的研究中验证这些发现,等离子体sTNFR75水平可能是有用的在瞄准阿奇霉素在慢性阻塞性肺病使用。
确认
我们感谢l·海丝特的专家协助,j . Hasday马里兰和细胞因子核心实验室(巴尔的摩,医学博士,美国)elisa的性能。在一些网站,一般临床研究中心(GCRC)被利用;M01赠款从国家研究资源中心(美国马里兰州贝塞斯达)下面列出。这个慢性阻塞性肺病的临床研究网络的成员和他们的拨款支持如下。布莱根妇女医院,波士顿,MA,美国(附属网站:依赖医疗集团,伍斯特,妈,美国;退伍军人医院,西罗克斯伯西罗克斯伯,妈,USA): J.J.小赖利(首席研究员),广义相对论Washko(首席研究员),r . Rosiello Moy和马丁(调查),c .梅奥McQuaid彼得森,k .艾蓝a .麦当劳b . Kniskern诉Danilack和k Matthess(协调员)(格兰特HL074428和GCRC格兰特RR02635)。美国丹佛市丹佛健康医学中心(附属网站:美国国家犹太医学及研究中心,丹佛,有限公司,美国;美国科罗拉多大学博尔德有限公司):上面阿尔伯特(首席研究员)、b(首席研究员),m·施瓦兹和c·韦尔奇(调查),m . Gilmartin Verano和c(协调员)(格兰特HL074409和GCRC格兰特RR00051)。洛杉矶生物医学研究所的加州大学洛杉矶分校医疗中心harbor托兰斯,CA,美国:r . Casaburi(首席研究员),j . Porszasz(研究员),r•爱、k . Norulak r . Kiledjian和g·加西亚(协调员)(格兰特HL074407和GCRC格兰特RR00425)。明尼苏达州退伍军人研究所,明尼阿波利斯,美国(HealthPartners研究基金会附属网站:,布卢明顿,锰、美国; Mayo Clinic, Rochester, MN, USA): D.E. Niewoehner (Principal Investigator), C. McEvoy, K.R. Rice and P.D. Scanlon (Co-Principal Investigators), C.B. Bourassa, P. Neuenfeldt and J. Hart (Coordinators) (grant 1U10-HL074416). Temple University, Philadelphia, PA, USA: G.J. Criner (Principal Investigator), N. Marchetti, A. Satti, V Kim, J Mamary and F. Cordova (Investigators), C. Grabianowski, D. Fehrle, H. Criner and G. Jones (Coordinators) (grant HL074408). G.J. Criner (Principal Investigator), W. Chatila, N. Marchetti, V. Kim, G. D'Alonzo, S. Krachman, F. Cordova, K. Brennan, N. Patel and J. Mamary (Investigators), D. Fehrle, C. Grabianowski and G. Jones (Coordinators) (grant HL074408). University of Alabama at Birmingham, Birmingham, AL, USA: W.C. Bailey and J.A.D. Cooper (Co-Principal Investigators), M.T. Dransfield, L.B. Gerald and P. O'Reilly (Investigators), S. Tidwell (Coordinator) (grant HL074418). University of California, San Francisco, CA, USA: S.C. Lazarus (Principal Investigator), H.A. Boushey and P.G. Woodruff (Investigators), M. Birch, R. Sakurai, K. Schardein, M. Dyjak and C. Nguyen (Coordinators) (1U10-HL074431). University of Maryland, Baltimore, MD, USA: S.M. Scharf (Principal Investigator), M. Alattar, P. Amelung, M. Cowan, J. Hanson, J. Hasday, A. Iacono, C. Shanholtz, N. Todd and A. Verceles (Investigators), T. Fitzgerald, W. Bell-Farrell and P. Wood (Coordinators) (grant HL074441 and GCRC grant RR16500). University of Michigan, Ann Arbor, MI, USA: F.J. Martinez (Principal Investigator), J.L. Curtis, M.K. Han, K.R. Flaherty, T. Standiford, S.E. Gay and T.E. Sisson (Investigators), D. Thompson, L. McCloskey, M. Christensen and D. White (Coordinators) (grant HL074422). University of Pittsburgh, Pittsburgh, PA, USA: F. Sciurba (Principal Investigator), J. Bon (Investigator), L. Kniolek, M. Pitaro and R. Folger (Coordinators) (grant HL074439 and GCRC grant RR00056). University of Minnesota (Data Coordinating Center), Minneapolis, MN, USA: J.E. Connett (Principal Investigator), N.R. Anthonisen (Steering Committee Chair), C. Wendt (Co-Principal Investigator), M. Skeans, W. Patrek, H. Voelker and S. Harnden (Coordinators) (grant 1U10- HL074424). Data and Safety Monitoring Board: B.B. Bender, S.F. Kelsey, J.R. Landis, B. Phillips, G.M. Turino, R. Veatch, A. Waldo, C. Champlin and A. Wanner (all National Heart, Lung, and Blood Institute, Bethesda, MD, USA). Protocol Review Committee: H.W. Kelly (University of New Mexico-Health Sciences Center, Albuquerque, NM, USA), J. Maurer (The Cleveland Clinic Foundation, Cleveland, OH, USA), A.J. McSweeny (Northwestern University Medical School, Chicago, IL, USA), R.M. Senior (Washington University School of Medicine, St Louis, MO, USA), E.A. Thom (George Washington University, Rockville, MD, USA), P.D. Wagner (University of California, San Diego. San Diego, CA, USA), R.L. ZuWallack (Saint Francis Hospital and Medical Center, Hartford, CT, USA). National Heart, Lung, and Blood Institute, Bethesda, MD, USA: G. Weinmann (Deputy Director, Division of Lung Diseases), T. Croxton (Director, Airway Biology and Disease Program), A. Punturieri (Program Officer) and M.P. Stylianou (Biostatistician).
脚注
支持声明:这项工作是支持的研究所Health-National心脏、肺和血液研究所(授予U10 HL074407, U10 HL074408, U10 HL074409, U10 HL074416, U10 HL074418, U10 HL074422, U10 HL074424, U10 HL074428, U10 HL074431, U10 HL074439,和U10 HL074441)。慢性阻塞性肺病的临床研究网络的成员和他们的特定的授权信息可以确认部分中找到。
利益冲突:披露可以找到与本文的在线版本www.www.qdcxjkg.com
- 收到了2013年3月19日。
- 接受2013年8月16日。
- ©2014人队