摘要
6分钟步行距离(6MWD)最近被证明与特发性肺纤维化(IPF)患者的死亡风险相关;然而,6MWD对预测死亡风险的独立贡献尚未在大量明确的IPF患者群体中进行评估。
在一项评估干扰素γ-1b (n=748)的临床试验中,使用Cox比例风险模型来表征感兴趣的危险因素与IPF患者全因死亡率之间的关系,这些患者完成了为期24周的研究访问。感兴趣的危险因素包括先前发表的临床预测模型中死亡率的独立预测因子以及6MWD和6MWD的24周变化。
基线6MWD <250 m与死亡风险增加2倍相关(风险比2.12,95% CI 1.15-3.92),而6MWD >50 m的24周下降与死亡风险增加近3倍相关(风险比2.73;95%可信区间1.60 - -4.66)。与原始模型相比,纳入6MWD数据改善了模型识别(C-statistic 0.80 (95% CI 0.76-0.85))与0.75(0.71 - -0.79))。
6MWD和6MWD的变化都是IPF患者死亡率的独立预测因素。在临床预测模型中加入6MWD较原模型提高了模型判别能力。
摘要
6MWD指数独立预测IPF的死亡率,并改善以往的临床预测模型的性能http://ow.ly/tDdmP
介绍
特发性肺纤维化(Idiopathic pulmonary fibrosis, IPF)是一种慢性且最终致命的纤维化肺疾病,其特征是进行性肺功能不全和运动能力下降[1].可能会出现短暂的临床稳定期;然而,疾病的持续进展是不可避免的[2].预后较差,估计5年生存率可与几种肿瘤疾病媲美,包括肺癌、肝癌和脑癌[3.,4].
一些研究已经确定了IPF患者死亡率的独立预测因素,包括年龄、呼吸住院、预测的用力肺活量(FVC)%和FVC%预测值的纵向变化[5- - - - - -16].6分钟步行距离(6MWD)是一种实用且广泛用于各种心肺疾病患者临床状态的测量方法[17- - - - - -22,最近被证明与IPF患者的死亡风险有关[23- - - - - -25];然而,在大量明确的IPF患者中,6MWD对死亡风险的独立贡献尚未得到正式评估。
我们之前报道了IPF患者6分钟步行试验(6MWT)的试验性能特征[23].本研究的一个新发现是,尽管6MWD和已知的各种肺功能指标之间的相关性相对较弱,但6MWD和6MWD的24周变化可以高度预测1年死亡率。基于这一观察,我们假设6MWT可能询问疾病过程的一个独立领域,并提供关于IPF患者预后的递增信息数据。因此,本研究的目的如下。1)评估6MWD对预测IPF患者全因死亡风险的贡献,独立于我们之前报道的其他预测死亡率的指标;2)当将6MWD添加到先前发表的临床模型中时,评估模型性能的变化[7].
方法
来源和研究人群
来源人群包括一项前瞻性、双盲、安慰剂对照3期试验中的所有随机患者(GIPF-007 (INSPIRE)试验;(n = 826)26].从来源人群中,我们选择了完成基线和24周研究来访的所有患者(n=748);因此,在基线至24周之间死亡(n=20)或进行肺移植(n=1)的患者被排除在分析之外。原始试验的临床疗效结果显示没有治疗效果的证据;因此,分析包括了来自两个治疗组的数据,以最大限度地提高研究的效力[26].
最初试验的登记标准已在前面说明[26].简单地说,符合条件的患者根据美国胸科学会/欧洲呼吸学会的标准有信心诊断为IPF [188bet官网地址27,28], FVC≥预测值的55%,肺对一氧化碳的扩散能力(DLCO) ≥35%的预测值,FVC或DLCO≤预测值的90%,6MWT距离≥150 m。在过去6个月内有不稳定或恶化的心脏、血管或神经疾病病史的患者,以及随机分组时在肺移植等候名单上的患者被排除在纳入对象之外。
研究协议
符合条件的患者接受了完整的体格检查和生理功能评估(FVC,DLCO在基线研究访视时和此后24周的间隔时间内,患者的呼吸困难(根据加州大学圣地亚哥分校呼吸急促问卷调查)、健康相关生活质量(根据圣乔治呼吸问卷调查)和运动能力(6MWT)。
6MWT是在室内进行的,在一个平坦、笔直、表面坚硬的走廊上。在筛查来访时进行氧滴定程序,以建立需要补充氧的患者的基线流速;研究期间的所有后续测试均使用滴定过程中建立的基线氧流速进行。在每6MWT前,患者需要在休息呼吸室空气10分钟后或在基线氧饱和度时,用脉搏血氧仪测量静息氧饱和度至少为83%2流量。患者被要求在不慢跑或跑步的情况下尽可能走远;如果他们需要减速或停下来休息,他们被允许这样做,并鼓励他们尽快恢复步行。如果患者出现胸痛、难以忍受的呼吸困难、腿抽筋、出汗或饱和度低于83%,则停止试验。
两个观察期被用来最大限度地增加事件的数量,并增强研究的力量来检测预测变量和1年死亡率之间的显著关系。分别在试验基线至第24周试验来访期间和第48周至第72周试验来访期间评估死亡率预测因子。这些时期作为“磨合”阶段,在此期间测量死亡率纵向预测指标的变化;随后48周期间发生的所有死亡都被确定并相应标记(图1).这两个时期的所有数据被合并到一个数据集中进行分析;因此,患者可能对研究数据库贡献了两个独特的观察结果。
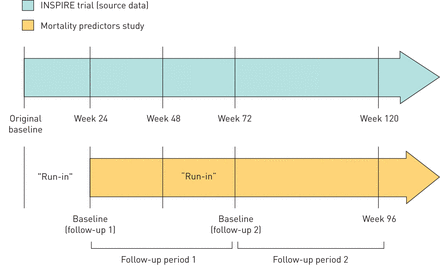
研究设计示意图。
统计分析
一个多变量Cox比例风险模型被用来描述相关危险因素和全因死亡率之间的关系。感兴趣的危险因素包括先前发表的临床模型中死亡率的独立预测因素(年龄、呼吸系统住院情况、FVC % pred和FVC % pred的24周变化)[7], 6MWD和24周变化。保留原始临床模型中感兴趣的危险因素的分类阈值;基线6MWD和6MWD 24周变化的分类阈值是根据以前的研究选择的[23].
使用已发表的方法对多重共线性、危害假设和模型判别的存在进行了评估[29,30.].模型鉴别基于C-统计量进行量化,并与先前发表的临床模型进行比较。C-统计量是对随机选择的两名患者中预测风险较高的患者最先经历事件的概率的测量。值的范围从0.5(模式识别并不比机会好)到1.0(完美识别)。假设0.70和0.80之间的值表示“可接受的”模型区分;假设值超过0.80表示“优秀”辨别。还通过计算模型的净再分类改善(NRI)来评估模型性能,包括6MWD和6MWD相对于原始模型的变化(基于研究GIPF-007中的患者)。NRI可以量化为风险类别中上升的个体比例减去发生事件的受试者下降的比例,以及下降的个体比例减去未发生事件的受试者上升的比例的差异总和[30.].
结果
在最初的临床试验中,共有748名患者完成了为期24周的研究访问,因此有资格纳入研究人群。人口统计学和基线特征总结见表1.均值±sd研究开始时的年龄为66±7.6岁,71.5%的患者为男性。FVC % pred和的平均值DLCO% pred分别为72.5±12.8和47.5±9.2。均值±sd6MWT期间步行距离为397±107 m。总共86例(11.5%)患者在6MWT期间需要补充氧;其中平均基线氧流量为2.84 L·min−1.
在两个观察期间共有79例死亡(n(患者来访)=1156;参见在线补充表E1);在第24周和第72周研究访问期间(平均随访时间为43周)发生了59例死亡,在第72周研究访问后的48周(平均随访时间为31周)发生了20例死亡。粗1年全因死亡风险为6.8% (95% CI 5.4-8.3%)。临床研究人员判定67例患者的死亡与ipf相关(粗1年风险5.8%,95% CI 4.6-7.1%)。
6MWD基线和6MWD 24周变化对1年全因死亡率和Kaplan-Meier生存分布的未调整风险进行了总结表2和图2,分别。在未经调整的分析中,基线6MWD和6MWD的24周变化均与1年死亡率风险相关。24周时6MWD >下降50 m的患者(与≤25 m下降)的相对危险度最大(危险度比(HR) 3.76, 95% CI 2.26 ~ 6.27;p < 0.001)。
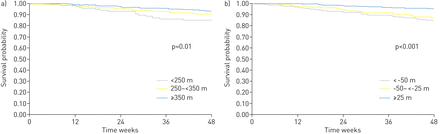
Kaplan-Meier生存分布按a)基线6分钟步行距离(6MWD)和b) 6分钟步行距离24周变化进行。p值来自Log-rank检验。
在多因素分析中发现,所有相关危险因素都是具有统计学意义的全因死亡率的独立预测因素,包括年龄、呼吸系统住院情况、FVC % pred、6MWD以及FVC % pred和6MWD的24周变化(表3)基线6MWD<250m与1年死亡率风险增加两倍独立相关(HR 2.12,95%可信区间1.15–3.92;p=0.02),6MWD>50m的24周下降与1年死亡率风险增加近三倍独立相关(HR 2.73,95%可信区间1.60–4.66;p<0.01)此外,与原始临床模型相比,6MWD中包含6MWD和24周变化改善了模型的辨别力(C-统计0.80(95%可信区间0.76–0.85)与0.75 (95% ci 0.71-0.79))。在原模型基础上增加6MWD和6MWD 24周变化导致NRI为26.1% (p<0.001);与原始模型相比,10.1%的事件和16.0%的非事件被正确地重新分类(表4).
原始临床模型中感兴趣的危险因素的危险比与以前发表的估计具有可比性。与最初的临床模型一致,FVC % pred和24周FVC % pred的变化仍然是1年死亡率的最重要预测因素;基线FVC≤50%患者的全因死亡率风险比为6.86 (95% CI 1.99-23.60) (p<0.01)。与≥80%)和5.86 (95% CI 3.33-10.81) (p<0.01)。与> -5%)。
作为最初的临床模型包括一个子集gipf - 001 330名患者的研究来说,6 mwt数据没有收集,使用预测变量的多变量分析在最初的临床模型子集的重复(n = 748)的病人中,那些包含在当前分析(在线补充表E2)。与原始临床模型相比,风险比和模型判别基本没有变化。与最初的临床模型一致,6MWD的增加和6MWD的改变改善了该队列中的模型识别(c -统计量0.80 (95% CI 0.76-0.85))与0.76(0.71 - -0.82))。
讨论
IPF的典型临床特征包括进行性肺功能不全和运动能力下降。虽然肺功能和运动能力的下降是不可避免的,但在患者内部和患者之间的疾病进展率可能存在相当大的变异性。此外,用于评估IPF患者临床状态的各种指标的纵向变化只有微弱的相关性;一种测量方法的暂时稳定期可能与其他方法的显著下降期同时出现[23,31].由于高度可变和高深莫测的临床过程,在个体患者中形成准确的预后对临床医生来说是一个独特的挑战。因此,确定在典型的临床环境中容易和可靠地确定的准确死亡率预测因子,对IPF患者的临床管理具有明显和重要的意义。
我们之前报道了一个简化的临床风险预测模型,该模型由四个在临床环境中广泛使用的预测因子组成,能够准确预测IPF患者的近期死亡率[7].预测因素包括年龄、前24周呼吸系统住院史、FVC % pred和24周FVC % pred变化。在本研究中,我们进一步证明,6MWD和6MWD的24周变化是IPF患者近期死亡率的独立预测因素,一个新的临床风险预测模型包括年龄、呼吸住院情况、FVC % pred、与以前发表的临床模型相比,6MWD和24周FVC % pred的变化和6MWD提高了根据风险区分患者的能力。
6MWT作为衡量IPF患者的临床状态有几个潜在的优势。该测试实用、价廉、可靠;它不需要特殊设备或高级培训,除了最严重的受损患者外,所有人都可以执行[32].此外,6MWD在IPF患者中具有高度的可重复性[23,33]而6MWD的变化已被证明与生理功能和健康相关生活质量测量的变化相关[23].由于6MWT是自定步速,它比其他步行测试更耐受性更强,也更能反映日常生活活动[34].最后,通过捕捉功能缺陷,6MWT可能在评估伴有合并症肺气肿的IPF患者的疾病进展方面提供了递增的信息,否则由于虚假保存FVC而被掩盖[33].
之前只有两项研究表明6MWD与IPF患者的死亡率风险之间存在独立相关性[24,25].在对44例IPF患者(其中29例在12个月时进行了额外评估)的回顾性研究中,Caminatiet al。[24]报告了基线6MWD (<212 m)和12个月时6MWD的变化与死亡风险增加独立相关。该研究受到样本量适中和分析的回顾性性质的限制,以及排除了不能在不使用辅助氧的情况下进行6MWT的患者。然而,这些发现与L埃德勒等.[25]这项研究评估了454名等待肺移植的IPF患者中6MWD的预后效用与6个月时死亡风险的增加密切相关,且作为等待名单生存率的预测因子,其表现优于基线FVC%pred。值得注意的是,6MWD的纵向变化未被评估为潜在的死亡率预测因子,且6MWT未根据标准化方案进行跨研究地点。此外,肺移植患者代表了一个独特的队列;平均而言,本研究中的患者比不适合肺移植的IPF患者更年轻,有更严重的生理损伤和更高的共病肺动脉高压患病率。因此ich研究结果可以推广到IPF患者的更广泛人群中,目前尚不清楚。
在目前的分析中,我们研究了6MWD对一大批明确诊断为IPF和广泛的疾病状态生理指标损害的患者近期死亡风险的具体贡献。基线6随钻测量< 250是独立与1年死亡率的风险,增加了1/2,50米衰减在24周6随钻测量授予近三倍增加死亡率的风险在接下来的几年中,甚至在控制了年龄、呼吸道住院、FVC % pred及24周FVC的变化。后一项发现尤其值得注意,因为它首次在一项大型跨国研究中确立了6MWD的纵向变化与IPF患者近期死亡风险之间强烈且独立的关联。而我们的研究结果也显示出显著关系24周减量6随钻测量26-50 m和1年死亡率的风险,我们选择了把重点放在50米的阈值衰减基于之前的工作中,最小的临床重要差异6 mwt估计24-45 m [23].我们之所以选择较高的阈值,是因为我们不希望为了提高敏感性而牺牲特异性。
本研究的另一个值得注意的发现是,在一个基于四种广泛可用且廉价的疾病状态测量方法的简易临床模型中加入6MWD,为IPF个体患者的预后评估提供了增加信息的数据。当将6MWD和6MWD的24周变化添加到由年龄、呼吸系统住院情况、FVC % pred和FVC % pred的24周变化组成的模型中时,通过c统计量测量的模型辨别能力从0.75 (95% CI 0.71-0.81)提高到0.80 (95% CI 0.76-0.85)。模型识别的改善幅度是显著的,因为需要与因变量有较大的独立关联,才能添加预测标记,从而导致c统计量有意义的增加[29].例如,Pencina等.[29通过将高密度脂蛋白(HDL)胆固醇引入弗雷明汉心脏研究的3264名受试者首次冠心病(CHD)事件的标准预测模型,评估了模型性能的改善。HDL胆固醇与冠心病事件风险独立相关(HR 0.64;p < 0.001);然而,将HDL胆固醇添加到由年龄、性别、吸烟状况和收缩压组成的标准模型中,对模型识别的影响可以忽略不计(c -统计量0.77)与0.76;p =无意义的)。此外,与最初的临床模型一致,新模型的识别能力优于基于弗雷明汉心脏研究的几个成熟的心血管疾病模型;这些模型的c -统计量范围为0.66-0.79 (表5) [35- - - - - -39].
我们的发现对临床实践和临床试验设计都有一些潜在的意义。6MWT是一种实用、安全、廉价的措施,几乎可以在任何环境下执行,不需要专门的设备或高级培训。我们的结果表明,从这种简单和廉价的检测中获得的数据可以用于进一步了解预后和促进临床决策。此外,根据风险进一步区分患者的能力可能有助于改进治疗性临床试验的纳入标准,从而丰富研究人群,潜在地减少必要的规模、持续时间和临床试验的成本。最后,FVC和6MWD的纵向变化与死亡风险之间具有很强的独立相关性,加上有利的测试性能特征和相对较弱的变化之间的相关性FVC和6随钻测量表明,复合端点定义的疾病进展的基础上,分类变化FVC和6随钻测量可能大幅增加的速度在临床上有意义的事件和进一步提高效率的临床试验。
我们的研究结果应该在几个重要的局限性的背景下加以解释。首先,我们分析的来源数据来自一项临床试验,该试验纳入了肺功能和运动能力基线测量中轻度至中度损害的患者。有严重功能障碍或伴有严重肺气肿和不稳定心血管疾病等合并症的患者被排除在纳入的患者之外。虽然研究人群可能包括轻度至中度肺气肿患者,以及在第二次观察期间(72周至120周)出现严重生理功能损害的患者,但我们的研究结果在多大程度上可以推广到这些人群尚不确定。
其次,确定了模型中的利益风险因素和相应的类别阈值先天的基于之前的研究。以来的主要目的是研究评估的独立贡献6随钻测量的死亡率和评估风险的预测价值6随钻测量时添加到先前发表的临床预测模型,没有正式的模型规范程序在指定的主要分析模型新创.第三,如我们之前的出版物所述[7],根据主要研究人员的临床判断,将住院治疗指定为呼吸性质,并没有正式裁定。然而,我们注意到,我们最初的目的是开发一种风险预测模型,可用于临床,根据现成的数据快速准确地制定预后。因此,我们认为,住院治疗的方式更能反映典型的临床实践,从而潜在地提高了该模式的临床效用。最后,6MWT严格按照标准的氧滴定程序进行;这种严格的方法在典型的临床环境中的复制,虽然可能,但不能保证。事实上,我们决定不开发一个修订的风险评分系统,很大程度上是基于6MWT标准化程序的临床应用可能不一致。尽管如此,我们相信6MWD和死亡风险之间的关系的强度值得在IPF患者的临床评估中考虑,并对临床试验的设计和执行具有重要的意义。
总之,本研究的结果表明,6MWD和6MWD的纵向变化都是IPF患者死亡率的强大独立预测因素。此外,临床风险预测模型由年龄、呼吸道住院、FVC % pred 6随钻测量和24周变化FVC % pred和6随钻测量可靠地预测1年死亡率IPF患者,可用于进一步完善个体病人的预后,指导临床决策。进一步的研究需要在其他大型和独立的患者群体中验证该模型。
致谢
我们感谢K.Glasscock(Intermune Inc.,布里斯班,加利福尼亚州,美国)提供医疗写作和编辑协助,并感谢所有研究中心的参与人员和患者。
脚注
有关编辑评论,请参阅1237页.
这篇文章有补充资料可从www.www.qdcxjkg.com
临床试验:本研究注册于www.clinicaltrials.gov标识号NCT00075998.
支持声明:本研究由InterMune公司(布里斯班,加州,美国)赞助。
利益冲突:可以在本文的在线版本旁找到披露www.www.qdcxjkg.com
- 收到了2013年7月30日。
- 接受2013年11月1日。
- ©ERS 2014















