摘要
我们假设患有慢性阻塞性肺疾病(COPD)的吸烟者的气道平滑肌(ASM)细胞对香烟烟雾的反应与没有COPD的吸烟者本质上不同,产生更多的促炎介质和与气道重塑相关的因素。
从患有或不患有COPD的吸烟者身上获得ASM细胞,然后用香烟烟雾提取物(CSE)或转化生长因子-β1刺激。ELISA法检测趋化因子和基质金属蛋白酶(MMPs)的产生,细胞外基质ELISA法检测胶原的沉积。通过甲苯胺蓝附着和细胞跟踪器绿色伤口愈合试验来测量CSE对细胞附着和伤口愈合的影响。
CSE增加了人ASM细胞中CXCL8和CXCL1的释放,COPD吸烟者的细胞产生更多的CSE诱导的CXCL1。CSE增加了MMP-1、-3和-10的生成以及胶原VIII α 1 (COL8A1)的沉积,特别是COPD组MMP-1的生成和COL8A1的沉积较高。CSE仅在COPD组中降低了ASM细胞附着和伤口愈合。
COPD吸烟者的ASM细胞对CSE刺激更敏感,这可能部分解释了为什么一些吸烟者会患COPD。
摘要
香烟烟雾提取物诱导COPD患者气道平滑肌细胞气道重塑相关变化http://ow.ly/wK0ey
介绍
慢性阻塞性肺疾病(COPD)是世界范围内发病率和死亡率的主要原因,造成了巨大且不断增加的经济和社会负担[1]、[2]。在慢性阻塞性肺病中,肺部发生了许多变化,即持续炎症的发展和不可逆的气流限制[3.]。
气流受限是由三个相互关联的过程引起的:小气道壁增厚(重塑)、小气道丧失和肺气肿。然而,小气道重塑被认为对气流限制的影响最大[4] - [6]。此外,小气道重塑可能是COPD的主要病理损害。在一项对COPD肺组织进行显微计算机断层扫描分析的研究中,发现终末细支气管的重塑和丧失在显微镜下先于肺气肿变化[7]。COPD小气道重塑表现为粘膜折叠、基底膜增厚、结缔组织沉积,气道平滑肌(ASM)质量增加,严重COPD尤为明显[j]。6]、[8]、[9]。结缔组织由细胞外基质(ECM)蛋白的交织框架组成,已知特异性的ECM蛋白在COPD患者的气道中发生改变[10]、[11]。
在发达国家,发展为慢性阻塞性肺病的主要危险因素是吸烟。通过两者的使用在活的有机体内和在体外吸烟对慢性阻塞性肺病病因的影响的模型正在开始被理解。大多数研究都认为COPD的病因是香烟引起的炎症导致组织损伤;然而,先前的研究表明气道重塑可能独立于炎症诱导[12]。先前发现,与非COPD患者的细胞相比,COPD患者的成纤维细胞对香烟烟雾提取物(CSE)的反应产生了过量的纤维连接蛋白和perlecan或减少的蛋白聚糖(decorin和biglycan)。12]、[13]。COPD患者的上皮细胞对CSE的反应也不同[14],但COPD ASM细胞对CSE的反应是否不同尚不清楚。
在这项研究中,我们假设COPD患者的ASM细胞对香烟烟雾的反应与非COPD患者的ASM细胞本质上是不同的,特别是在促炎介质和气道重塑相关因子的产生方面。
材料与方法
研究对象
获得受试者的诊断、吸烟史和肺功能信息。诊断为哮喘、感染性疾病或肺间质性疾病的受试者不包括在内。样本取自受试者,根据气流受限的严重程度分为以下几类[15]。1)非copd: n=21, 1 s用力呼气量(FEV)1)/用力肺活量(FVC)≥70%,FEV1≥80%。2) COPD: n=20, FEV1/ FVC < 70%。详细资料载于补充资料(表S1)。所有研究对象或其近亲均提供书面知情同意书。所有使用人体肺组织的实验均由西南悉尼地区卫生服务伦理审查委员会、悉尼圣文森特医院和悉尼大学人类研究伦理委员会(均为澳大利亚悉尼)批准。
细胞培养和样品制备
从人肺中获得ASM细胞的方法由先前描述的方法改进[16]。从大约六阶或更大的支气管上显微解剖人类ASM细胞,并在由DMEM (Invitrogen, Carlsbad, CA, USA)补充5%胎牛血清(DKSH, Melbourne, Australia), 1%抗生素(Invitrogen)和25 mM Hepes (Invitrogen)组成的生长培养基中初始培养。在进行实验之前,所有细胞的支原体检测均为阴性,并在第2代至第7代之间使用。ASM细胞接种于六孔或96孔培养板(BD Biosciences, North Ryde, Australia),密度为1×104细胞·厘米−2在生长培养基中,在37°C/5% CO下孵育2细胞在添加0.1%胎牛血清、1%抗生素和25 mM Hepes的静止培养基中饥饿24 h,然后用CSE或10 ng·mL刺激−1转化生长因子(TGF)-β1 (R&D Systems, Minneapolis, MN, USA)在静止培养基中刺激后,收集人ASM细胞(六孔板)上清液,用0.016 mM氢氧化铵(NH)裂解细胞(96孔板)4OH)在37°C下洗涤20分钟,然后用0.05% PBS-Tween (Tw)20 (vol/vol)洗涤。这些上清液和无细胞ECM板保存在-20°C直到分析。
香烟烟雾提取物
我们使用的是万宝路红香烟(Philip Morris, Victoria, Australia),每支香烟含有1.1毫克尼古丁,15毫克焦油和15毫克一氧化碳。CSE的制备方法由先前描述的[12]。简单地说,将一支万宝路香烟以25ml DMEM恒速起泡,该溶液视为100%浓度的CSE。100%的CSE在每次实验中新鲜生成,并在30分钟内稀释至最终工作浓度并使用。
细胞活力和毒性测定
如前所述,将人ASM细胞接种于96孔板中,用CSE从0.05%到50%的连续稀释度刺激细胞。活细胞线粒体活性采用Thaizolyl blue tetrazolium bromide (MTT) (Sigma Aldrich, St . Louis, MO, USA)法检测。通过乳酸脱氢酶(LDH) (Sigma Aldrich)测定法检测细胞膜的完整性,根据细胞质LDH释放到培养基中的量。刺激72 h后,用分光光度计(Spectramax M2;Molecular Devices, Sunnyvale, CA, USA)设置,吸光度分别为570 nm/690 nm和490 nm/690 nm。
趋化因子ELISA
如前所述,将人ASM细胞接种于六孔板中,用不同浓度的CSE或10 ng·mL刺激细胞−1使用商用人CXCL8/IL-8、CXCL1/GROα、CCL2/单核细胞趋化蛋白-1、CCL5/RANTES和CXCL10/诱导蛋白-10 ELISA试剂盒(R&D Systems),按照生产厂家说明书检测人ASM细胞上清液中CXCL8(白细胞介素(IL)-8)、CXCL1 (GROα)、CCL2、CCL5和CXCL10的浓度。使用分光光度计(Spectramax M2)在450 nm/570 nm处读取吸光度。
转录因子核因子-κB及激活蛋白-1活性测定
如前所述,将人ASM细胞接种于六孔板中,用CSE(5%和10%)或10 ng·mL刺激细胞−1TGF-β1作用60 min,然后收集核提取物。核因子(NF)-κB和激活蛋白(AP)-1的活性采用TransAM ELISA试剂盒(Active Motif, Carlsbad, CA, USA)根据制造商的说明进行评估。使用分光光度计(Spectramax M2)在450 nm/ 655nm处读取吸光度。
实时PCR阵列
从患有慢性阻塞性肺病(n=3)和未患有慢性阻塞性肺病(n=3)的吸烟者身上获得的人类ASM细胞受到刺激在体外5% CSE, 10% CSE或10 ng·mL−1转化生长因子-β1。在48 h收集RNA,然后使用隔离RNA迷你试剂盒(Bioline, London, UK)纯化,并使用M-MLV逆转录酶(Invitrogen)将mRNA转化为cDNA。从同一组的每个样本中提取等量的cDNA;然后根据制造商的说明书(Invitrogen)使用TaqMan阵列人细胞外基质和粘附分子96孔板检测基因表达。采用StepOne Plus检测系统进行实时PCR,使用StepOne软件(Applied Biosystems, Melbourne, Australia)收集和分析数据。利用ΔΔCt方法计算mRNA的相对丰度[17],结果归一化为18S rRNA。
基质金属蛋白酶ELISA试剂盒
如前所述,将人ASM细胞接种于六孔板中,用不同浓度的CSE或10 ng·mL刺激细胞−1总基质金属蛋白酶(MMP)-1、-2、-3、-10和-12的浓度使用人MMP ELISA试剂盒(R&D Systems),按照制造商的说明书进行测定,并使用Luminex分析仪(Luminex 200 System;Luminex,布里斯班,澳大利亚)。采用人活性MMP-1荧光检测试剂盒(R&D Systems)测定MMP-1酶活性,采用荧光板阅读器(Spectramax M2)设置,激发波长320 nm,发射波长405 nm,测定相对荧光单位。
ECM ELISA
如前所述,将人ASM细胞接种于96孔板中,用不同浓度的CSE或10 ng·mL刺激细胞−1TGF-β1作用72 h。使用无细胞ECM板,按照之前修改的方法,用ELISA法测定ECM中蛋白的沉积情况[16]。检测ECM蛋白的一抗为兔抗人COL5多克隆抗体(2 μg·mL)−1) (Abcam, Cambridge, UK),兔抗人胶原VIII α 1 (COL8A1)多克隆抗体(2 μg·mL)−1) (Novus Biologicals, Littleton, CO, USA),小鼠单克隆抗人纤维连接蛋白抗体(2 μg·mL)−1) (Millipore, Billerica, MA, USA),小鼠单克隆抗人perlecan抗体(2 μg·mL)−1)(表达载体)。兔IgG (Dako Cytomation, Glostrup, CA, USA)同型对照抗体和小鼠IgG1 κ同型对照抗体(BD Biosciences)以相同浓度作为一抗。测定COL8A1和perlecan,生物素化山羊抗兔抗体0.5 μg·mL−1生物素化鸡抗小鼠抗体0.8 μg·mL−1分别使用。
西方的屁股
如前所述,将人ASM细胞接种于六孔板中,用CSE(5%或10%)或TGF-β1刺激细胞72小时。收集每个样品的上清液,使用Western blots检测可溶性COL1和可溶性纤维连接蛋白。蛋白在10%聚丙烯酰胺凝胶上分级,转移到聚偏二氟乙烯膜上,在5% (wt/vol)脱脂牛奶溶液中阻断1 h,用8.8 μg·mL的一抗孵育−1小鼠单克隆抗col1抗体(Sigma Aldrich)或1 μg·mL−1小鼠单克隆抗人纤维连接蛋白(Millipore)在2%牛血清白蛋白/TBS-Tw中孵育2 h,然后与二抗(2.6 μg·mL)孵育−1兔抗小鼠ig -辣根过氧化物酶抗体(Dako细胞化)在2%牛血清白蛋白/TBS-Tw中进行1小时。免疫印迹检测采用Immobilon Western Chemluminescent HRP底物(Millipore),条带分析采用柯达4000 MM图像站(Eastman Kodak Co., New York, NY, USA)。每个样品中存在的蛋白质量被确定为密度计密度。
免疫组织化学
免疫组织化学样品的制备和免疫组织化学方法已在前面介绍过[18]。气道切片处理以减少非特异性背景染色,兔多克隆抗人COL8A1抗体1 μg·mL孵育−1(Abcam)和兔IgG同型控制抗体1 μg·mL−1(Dako Cytomation)。二抗标记为聚合物抗兔(EnVision+System-HRP;用底物显色剂、液体DAB (Dako Cytomation)对组织进行染色。每个切片取10张图像(每位受试者1张),使用Fiji软件(ImageJ)定量免疫染色[19]。在补充材料中提供了完整的细节。
细胞附着试验
96孔培养板在生长培养基中培养72 h,在静置培养基中培养24 h,然后在不同浓度的CSE(0.05% ~ 10%)静置培养基中培养72 h。将人ASM细胞以5×10的密度接种在处理过的培养板上4细胞·厘米−2在静止培养基中放置2小时。采用甲苯胺蓝附着法检测细胞附着,如前所述[20.]。采用分光光度法测定附着细胞的相对数量,吸光度为595 nm (Spectramax M2)。在补充材料中提供了完整的细节。
伤口愈合试验
使用Oris细胞迁移组装试剂盒(Platypus Technologies, Madison, WI, USA)进行伤口愈合试验。在处理过的96孔黑板上创面,用细胞跟踪器绿色CMFDA (Invitrogen)标记细胞。将标记的人ASM细胞以5×10的密度接种于损伤黑板上4细胞·厘米−2在生长培养基中。粘附24小时后取下塞,继续孵育4小时。使用荧光板读取器(Wallac VICTOR)测量创面愈合值2;Perkin Elmer, Waltham, MA, USA)从底部读取,激发波长设置为485 nm,发射波长设置为535 nm。在补充材料中提供了完整的细节。
统计分析
使用GraphPad Prism 5.0软件(GraphPad software, San Diego, CA, USA)进行数据分析。所有数据均以平均值±表示扫描电镜。采用单因素方差分析、双因素方差分析并酌情采用Bonferroni后验或Mann-Whitney检验来确定统计显著性。A p值≤0.05被认为是显著的。
结果
CSE对ASM细胞的细胞毒性
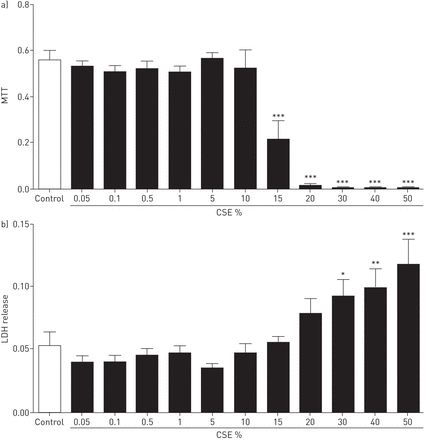
由于已知高浓度的CSE具有细胞毒性,我们使用了两种毒理学分析,评估线粒体活性通过MTT和膜完整性通过LDH释放,以确保我们使用的CSE浓度对人ASM细胞无毒性作用。浓度≥15%的CSE大大降低了存活率(图1);因此,我们在后续实验中使用0.05% ~ 10%的CSE作为刺激。
香烟烟雾提取物对细胞活力的影响。采用吸光度分别为570 nm/690 nm和490 nm/690 nm的Thaizolyl blue tetrazolium bromide (MTT)和LDH法测定CSE对人气道平滑肌(ASM)细胞(a)线粒体活性和(b)乳酸脱氢酶(LDH)释放的细胞毒性。用连续稀释的CSE刺激人ASM细胞72 h (n=4)。数据以平均值±表示扫描电镜。采用单因素方差分析加Bonferroni后验检验确定统计学显著性。*: p < 0.05;* *: p < 0.01;***: p<0.001,与对照组比较。
CSE诱导趋化因子
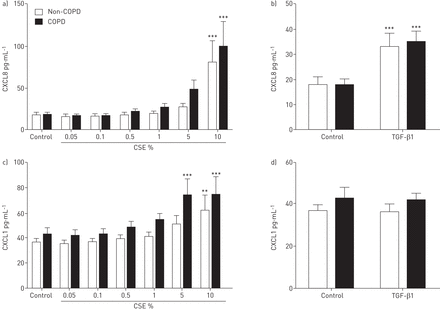
由于已知CSE可诱导人ASM细胞释放CXCL8 [21],我们使用这个输出来验证我们的在体外模型。CXCL8释放量增加10% CSE和10 ng·mL−1TGF-β1在非COPD组和COPD组的表达(图2a和图b).CXCL1的释放量在非COPD组增加10% CSE,在COPD组增加5%和10% CSE;而TGF-β1在两组均未诱导CXCL1的释放(图2c和d).在两组ASM细胞中,CXCL8和CXCL1的基础和最大产量没有差异。结果表明,CCL5和CXCL10在ASM细胞中的释放量过低,检测不到(检测限为15.625 pg·mL)−131.35 pg·mL−1分别)。我们发现CCL2是由ASM细胞产生的,但这不是由CSE或TGF-β1诱导的,并且在非COPD组和COPD组之间没有差异(数据未显示)。
人气道平滑肌细胞CXCL8和CXCL1的释放。采用ELISA法检测慢性阻塞性肺疾病(COPD)患者(n=9)和非慢性阻塞性肺疾病(COPD)患者(n=9)的ASM细胞经香烟烟雾提取物(CSE)或转化生长因子(TGF)-β1刺激72 h后上清液中a、b) CXCL8和c、d) CXCL1的浓度。数据以平均值±表示扫描电镜。采用双因素方差分析加Bonferroni后验检验确定统计学显著性。**: p<0.01, ***: p<0.001。
CSE影响转录因子DNA结合活性
我们的研究结果显示,CSE和TGF-β1都没有增加转录因子NF-κB的活性(图S1a和b);然而,5%的CSE仅在非copd组中增加了转录因子AP-1的活性(图S1c和d)。
ECM及粘附分子相关基因的表达
为了研究CSE对气道重塑的潜在影响,我们使用基于pcr的阵列作为筛选工具。在CSE和TGF-β1刺激下,评估70个ECM蛋白、粘附分子和MMPs的基因表达(图S2)。与TGF-β1相比,CSE上调了更多的ECM-和粘附分子相关基因,而MMPs基因的表达在CSE和TGF-β1刺激下存在差异。COPD组和非COPD组之间采用≥2的断线和/或>1.5倍的差异,进一步研究MMP-1、-2、-3、-10和-12以及COL5、COL7和COL8A1。
CSE诱发MMPs
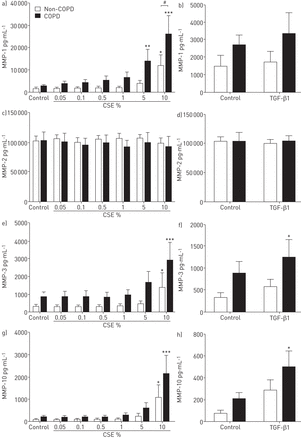
为了验证MMP的变化,我们测量了人ASM细胞中MMP-1、-2、-3、-10和-12的释放。在CSE或TGF-β1刺激后,人ASM细胞上清液中总MMP-12的浓度过低,无法检测到(数据未显示)。非COPD组总MMP-1浓度升高10%,COPD组升高5%和10% (图3a和b).CSE和TGF-β1均不影响MMP-2的产生(图3c、d).10% CSE增加两组MMP-3和MMP-10的释放,而TGF-β1仅在COPD组增加MMP-3和MMP-10的释放(图3情况).
从人气道平滑肌细胞中产生基质金属蛋白酶(MMPs)。采用ELISA法测定慢性阻塞性肺疾病(COPD)患者(n=8)和非慢性阻塞性肺疾病(COPD)患者(n=7)经香烟烟雾提取物(CSE)或转化生长因子(TGF-β1)刺激72 h后ASM细胞上清中a、b) MMP-1、c、d) MMP-2、e、f) MMP-3和g、h) MMP-10的浓度。数据以平均值±表示扫描电镜。采用双因素方差分析加Bonferroni后验检验确定统计学显著性。*: p < 0.05;* *: p < 0.01;***: p<0.001,与对照组比较。#: p<0.05,两组比较。
活性MMP-1的产生
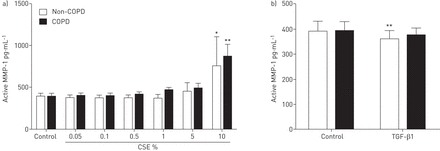
为了进一步研究CSE对MMP-1活性的影响,我们测量了人ASM细胞中MMP-1的活性形式。两组活性MMP-1浓度均升高10%,而TGF-β1仅在非copd组降低活性MMP-1的释放(图4).
人气道平滑肌细胞活性基质金属蛋白酶(MMP)-1的产生采用ELISA法测定慢性阻塞性肺疾病(COPD)患者(n=5)和非慢性阻塞性肺疾病(COPD)患者(n=5)经香烟烟雾提取物(CSE)或转化生长因子(TGF)-β1刺激72 h后ASM细胞上清液中活性MMP-1的浓度。数据以平均值±表示扫描电镜。采用双因素方差分析加Bonferroni后验检验确定统计学显著性。*: p < 0.05;**: p<0.01,与对照组比较。
ECM蛋白的沉积
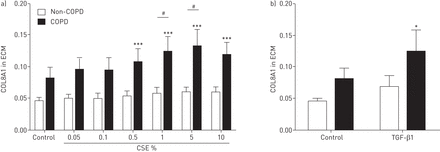
为了验证CSE或TGF-β1刺激后ECM蛋白的改变,我们评估了COL5、COL7和COL8A1在ECM中的沉积。COL7的沉积过低,无法检测到(数据未显示)。CSE没有改变COL5的沉积(图S3)。COL8A1的沉积仅在COPD组增加了0.5%、1%、5%和10%的CSE,并且与非COPD细胞相比,COPD细胞中1%和5% CSE诱导的COL8A1明显增加(图5).TGF-β1仅在COPD组增加COL8A1的沉积(图5 b).CSE没有改变两组纤维连接蛋白的沉积,这与之前在成纤维细胞中的发现形成鲜明对比[12], CSE抑制了两组人ASM细胞中perlecan的沉积(图S4)。
胶原VIII α 1 (COL8A1)在人气道平滑肌细胞中的沉积。采用ECM ELISA法测定慢性阻塞性肺疾病(COPD)患者(n=7)和非慢性阻塞性肺疾病(COPD)患者(n=7)的ASM细胞在香烟烟雾提取物(CSE)或转化生长因子(TGF)-β1刺激72 h后细胞外基质(ECM)中COL8A1的沉积,吸光值为450 nm/570 nm。数据以平均值±表示扫描电镜。采用双因素方差分析加Bonferroni后验检验确定统计学显著性。*: p < 0.05;***: p<0.001,与对照组比较。#: p<0.05,两组比较。
ECM蛋白的释放
为了验证CSE或TGF-β1刺激后可溶性ECM蛋白的改变,我们使用Western blots检测上清液中可溶性COL1和可溶性纤维连接蛋白。我们的结果显示,CSE和TGF-β1均未显著增加COL1的释放(图S5)。我们的结果还表明,CSE不诱导可溶性纤维连接蛋白的释放;而TGF-β1显著增加了纤维连接蛋白的释放(图S6)。
支气管COL8A1
由于我们发现慢性阻塞性肺病ASM细胞更大的cse诱导COL8A1,我们下一步研究是否我们的在体外结果反映了COPD在活的有机体内。免疫组织化学显示COL8A1在COPD患者(n=10)和非COPD患者(n=7)的气道组织中表达。在两组气道中,COL8A1似乎定位于基底膜、血管壁和ASM束。阳性染色采用阈值和同型对照染色。通过密度分析(定量染色面积),我们发现慢性阻塞性肺病组COL8A1的总体表达更高(图6).
胶原ⅰ(COL8A1)气道组织染色。a)采用免疫组织化学方法测定慢性阻塞性肺疾病(COPD)患者(n=10)和非COPD患者(n=7)气道支气管COL8A1的含量。使用化学发色团DAB(棕色)检测特异性染色,并用血红素(蓝色)对细胞核进行反染色。组织结构用苏木精和伊红染色。标尺=100 μm。b)用阳性染色面积定量非COPD组和COPD组COL8A1免疫染色,用同型对照校正。数据以中位数表示。采用Mann-Whitney检验确定统计学显著性。*: p < 0.05。
CSE抑制细胞附着和伤口愈合
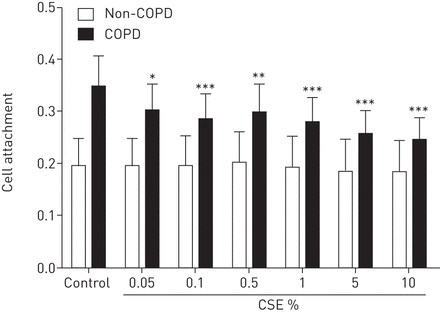
为了进一步研究CSE对人类ASM细胞功能的影响,我们评估了COPD患者(n=5)和非COPD患者(n=5) ASM细胞的细胞附着。CSE仅显著降低COPD组ASM细胞与培养板的附着(图7).伤口愈合实验显示,高浓度的CSE显著降低了人ASM细胞的伤口愈合速度(n=6)(图S7)。
香烟烟雾提取物(CSE)对595 nm吸光度下2小时细胞附着的影响。采用甲苯胺蓝法测定慢性阻塞性肺疾病(COPD)患者(n=5)和非慢性阻塞性肺疾病(COPD)患者(n=5)气道平滑肌细胞在CSE处理板上的附着情况。数据以平均值±表示扫描电镜。采用双因素方差分析加Bonferroni后验检验确定统计学显著性。*: p < 0.05;* *: p < 0.01;***: p<0.001,与对照组比较。
讨论
我们发现患有和不患有COPD的吸烟者的ASM细胞对CSE的不同反应。其中,慢性阻塞性肺病组ASM细胞中MMP-1和COL8A1的沉积增加,且COPD组增加幅度更大。我们的研究结果还显示,CSE降低了ASM细胞对培养板的附着,特别是在COPD吸烟者分离的细胞中减少了伤口愈合。这些发现表明,COPD吸烟者的ASM细胞对CSE刺激更敏感,这可能在一定程度上解释了一些吸烟者COPD的发展。
慢性阻塞性肺病是一种以中性粒细胞增多为特征的炎症性疾病[9]、[22],支气管肺泡灌洗液中中性粒细胞趋化因子(如CXCL8和CXCL1)含量升高[23]、[24]。CSE是ASM细胞中CXCL8的有效诱导剂[21]、[25];然而,从COPD患者分离的ASM细胞是否会像其他气道细胞一样出现CXCL8的高分泌尚不清楚[26]、[27]。因此,我们也测量了CSE诱导的CXCL8,发现CSE增加了ASM细胞中CXCL8的释放,但在COPD患者和非COPD患者的细胞中没有差异。我们还测量了CSE诱导的CXCL1,发现CSE增加了ASM细胞中CXCL1的释放。此外,COPD患者的ASM细胞对CSE刺激产生CXCL1更为敏感。CXCL8和CXCL1具有相似的生物学特性,它们都对中性粒细胞的募集有影响[28] - [30.]。在我们的研究中,我们使用了来自患有和不患有COPD的吸烟者的ASM细胞。CSE在两组ASM细胞中诱导CXCL8和CXCL1可能反映了观察到COPD患者中性粒细胞增加[31]和非慢性阻塞性肺病的吸烟者[32]。此外,由于低浓度的CSE仅在COPD细胞中诱导CXCL1,这表明这些细胞对CSE有高反应,这可能解释了为什么一些吸烟者患COPD,而另一些则没有。
我们的研究结果显示,高浓度的CSE增加了人类ASM细胞中proMMP-1和活性MMP-1(间质胶原酶)的释放,并且这在COPD吸烟者中比非COPD吸烟者更明显。当我们只测量活跃的MMP-1时,我们发现两组细胞之间的产量相似。这表明,ASM中活性MMP-1的产生可能不是COPD肺部病理的关键决定因素,但可能与患有和非COPD的吸烟者共同的过程有关。在其他细胞中,CSE增加了人上皮细胞和人肺成纤维细胞中MMP-1的产生,这似乎主要是通过细胞外调节的激酶-1/2丝裂原活化蛋白激酶途径驱动的[33]、[34]。我们还发现,人类ASM细胞组成性地产生高水平的MMP-2(明胶酶A),而CSE并没有增加这一水平,这与暴露于香烟烟雾的成纤维细胞的发现相反[35]。
与其他MMPs相比,MMP-3(基质溶解素1)和-10(基质溶解素2)迄今尚未得到广泛研究。我们的研究表明,CSE增加了人ASM细胞中MMP-3和-10的基因表达,10%的CSE增加了MMP-3和-10的产生。这些结果表明,MMP-3和-10可能导致吸烟者COPD的不同进展。两项基因分型研究表明,MMP-3多态性与COPD的疾病进展有关[36]、[37]。另一项研究显示,MMP-10基因在小气道和小气道周围实质中的表达增加与COPD的进展有关[38]。此外,我们的结果发现,MMP-12(巨噬细胞弹性酶)基因表达增加CSE在体外。然而,CSE刺激ASM的MMP-12蛋白释放量低于检测限(9.2 pg·mL)−1).
先前有研究表明,CSE增加了COPD成纤维细胞中纤维连接蛋白和perlecan的沉积[12],所以在这项研究中,我们也测量了它们在ASM细胞中的产生。然而,CSE不影响COPD ASM细胞中纤维连接蛋白的产生,并减少perlecan的产生,这表明对CSE的反应是细胞类型特异性的。我们的阵列数据显示,在CSE刺激下,几种胶原蛋白也发生了变化,因此我们选择对COL5、COL7和COL8进行评估。COL5的蛋白水平没有随着CSE的变化而变化,并且测量COL7的工具是不可靠的。然而,与对照ASM细胞相比,CSE诱导COPD细胞产生更多的COL8。目前对COL8在COPD中的作用知之甚少,特别是对COPD患者和非COPD患者气道中COL8的含量知之甚少。在这项研究中,我们发现COL8的表达在COPD气道中增加,特别是在平滑肌束内和周围,这表明平滑肌产生COL8原位提示慢性阻塞性肺病吸烟者COL8的沉积可能与气道病理有关。COL8具有短的三螺旋结构,含有α1和α2链,每个α链包含一个胶原结构域、一个短的n端非三螺旋结构域(NC2)和一个较长的c端非三螺旋结构域(NC1)。正如我们所知的其他胶原一样,COL8的不同区域可能具有相反的生物效应。例如,整个COL8分子增加了主动脉平滑肌细胞的增殖和迁移[39],而COL8A1的NC1结构域抑制牛主动脉内皮细胞的线粒体活性[40]。COL8先前未被报道为COPD中ECM的决定因素,但暴露于污染的怀孕小鼠会导致后代肾小管细胞COL8的增加[41]。这就提出了一个问题,即吸烟孕妇的后代是否也会受到类似的遗传影响。此外,这种暴露的功能和长期后果尚未得到检查。
我们没有研究过MMP-1和COL8之间是否存在相互作用,也没有在文献中找到具体的例子。人们很容易猜测,增加的MMP可能会降解胶原蛋白;然而,我们发现两者同时增加,表明净效应是胶原沉积。
慢性阻塞性肺病患者小气道壁和肺泡壁的修复受损[6]、[7]。我们的研究结果表明,CSE仅降低了COPD患者ASM细胞的细胞附着,高浓度的CSE还降低了ASM细胞的创面愈合率。这些结果可能表明,患有和不患有COPD的吸烟者的ASM细胞存在先天差异。一项关于CSE对人肺功能影响的研究表明,CSE降低了正常人支气管平滑肌细胞的迁移和收缩活性[42]。另一项研究表明,CSE损害牛支气管上皮细胞的伤口愈合通过活性氧依赖机制[43]。另一项研究显示,CSE抑制人肺成纤维细胞的增殖[44],但这些成纤维细胞是否来源于COPD患者尚不清楚。
为了研究转录因子活性的差异是否可以解释COPD ASM细胞对CSE的反应性增加,我们选择测量转录因子NF-κB和AP-1的活性,因为这些转录因子先前已被证明参与ASM细胞中MMPs和细胞因子的释放[45]、[46]。我们没有发现COPD ASM细胞中转录因子活性增加的证据。这表明慢性阻塞性肺病细胞对香烟烟雾的反应增加可能是由于表观遗传变化,正如我们在其他慢性阻塞性肺病细胞中发现的那样[47]。
总之,我们发现来自COPD患者和非COPD患者的ASM细胞在香烟烟雾刺激下产生趋化因子、MMPs和胶原的差异。从COPD受试者中分离的ASM细胞在释放炎症介质和与气道重塑和细胞行为相关的因子方面对香烟烟雾表现出更高的反应。我们的数据表明,慢性阻塞性肺病的ASM能够对香烟烟雾的可溶性成分做出反应。这可能会招募中性粒细胞(通过释放趋化因子),并可能通过改变ECM的沉积影响其他气道细胞。由于平滑肌的数量与COPD的严重程度正相关,这些影响可能在严重COPD中被放大。因此,我们的研究结果表明,来自吸烟者COPD患者的ASM细胞参与了该疾病的病理发展。
致谢
我们要感谢圣文森特医院(澳大利亚悉尼)的心肺移植团队和病理学家,以及皇家阿尔弗雷德王子医院(悉尼)和斯特拉斯菲尔德私立医院(澳大利亚斯特拉斯菲尔德)的胸科医生和病理学家的共同努力。
脚注
本文的补充资料来自www.qdcxjkg.com
利益冲突:可以在www.qdcxjkg.com网站上找到本文的在线版本
- 收到了2013年10月1日。
- 接受2014年5月4日。
- ©2014人队