抽象的
最近的研究表明,患有慢性阻塞性肺病(COPD)的男性比女性有更多的肺气肿。目前尚不清楚这些差异是否存在于COPD严重程度之间。我们的目的是根据COPD严重程度确定COPD亚组定量肺气肿的性别特异性差异。
我们包括来自Copdgene研究的非西班牙裔和非洲裔美国人科目,至少有10多年的吸烟和COPD全球血液测量级别II级或更高级别的吸烟和COPD全球倡议。我们检查了对数转化的肺气肿(Log%低衰减区域(%LAA)的性别特异性差异,黄金肺血管素级,早上的COPD(<55岁)和晚期肺气肿(> 25%肺气肿)。
与女性相比,男性LAA的log %更高:总体(1.97±1.4)与1.69±1.6,β=0.32 (0.04), p=1.34×10−14),以及非西班牙裔白人(p=8.37×10−14)和非洲裔美国受试者(P = 0.002)。雌性早盘COPD的女性,严重的肺气肿和黄金等级IV COPD患有类似的肺气肿,但少量吸烟(早盘,P = 0.01;严重的肺气肿和金级IV,P <0.001)。
本研究确定了具有普及的女性吸烟者的子集特别易于实质破坏。
抽象的
在重度COPD亚组中,女性更容易受到吸烟相关肺实质损伤/肺气肿的影响http://ow.ly/Stqyz
介绍
慢性阻塞性肺疾病(COPD)是美国第三大死亡原因,有1500万美国人受到影响[1].在过去几十年里,女性COPD患病率和死亡率迅速上升,现已与男性COPD患病率和死亡率相当[2那3.].多项研究表明,女性经历了比雄性相同的香烟曝光量大的肺功能下降[4.-7.].尽管COPD在非裔美国人中的患病率低于非西班牙裔白人[2],非裔美国人对吸烟的反应表现出更大的肺功能下降,一些研究表明非裔美国女性对吸烟特别敏感[4.].尽管越来越多的人认识到慢性阻塞性肺病不仅仅是一种男性疾病,但对慢性阻塞性肺病性别特征的研究一直受到限制,这是需要的[8.].
放射学肺气肿是一种临床相关的COPD表型,与肺功能丧失相关[9.那10],到期气流限制[11]减少扩散能力[12,减低运动能力[13那14]增加呼吸加剧[15]呼吸死亡率[16-18].识别肺气肿的性别差异可能导致对COPD易感性,严重程度,合并症和治疗的性别特异性差异有所了解。
一些先前的研究比较了横断面x线肺气肿在男性和女性之间。这些研究表明,作为一个群体,在气流阻塞程度相同的情况下,患COPD的男性比女性更容易出现肺气肿[19-22].基于这些研究,女性似乎对香烟烟雾造成的实质损害不像男性那么敏感。这与女性因吸烟而肺功能下降更严重的证据背道而驰[5.].然而,COPD是一种复杂的疾病,具有多种副题。这些研究受到鉴定雄性COPD受试者中较大肺气肿的趋势在严重的COPD亚型中,包括严重的肺气肿和先进或早期发病COPD。此外,这些趋势尚未在非洲裔美国人群中得到充分探索。Copdgene的主题子集中的一项研究表明,非洲裔美国人的整体肺气肿小于非西班牙语白人[23].进一步分析了这些亚组内的肺气肿差异,跨越不同的比赛是了解普及COPD如何通过性,见解可以提供可通知患者性别特异性临床护理的诊断。
这项研究响应了美国国立卫生研究院的呼吁,要求对疾病中的性别差异进行更多的调查[24尤其需要加强对COPD性别特异性特征的研究。本研究的目的是调查在肺功能范围广泛的大人群COPD受试者中肺气肿的性别特异性差异,并调查吸烟剂量和肺气肿之间的性别特异性关联。我们假设在重度COPD亚组中,男性肺气肿不会持续占优势。
材料和方法
主题
所有受试者签署知情同意书,并在布里格姆和妇女医院获得机构审查委员会批准(2007P000554;伙伴人类研究委员会)和所有研究站点(在线补充表S11)。所有研究对象都是非西班牙裔白人或非洲裔美国人,目前或曾经在COPDGene研究中吸烟[25].所有受试者都完成了修改过的美国胸部社会(ATS)呼吸问卷和标准化的肺功能测试。我们的主要分析是由ATS /欧洲呼吸道学协会标准的COPD主题(1 s中的支气管扩张剂强制呼气量(FEV)188bet官网地址1)/强迫肺活量(FVC) <70%, FEV1<80%预测)和全球慢性阻塞性肺疾病倡议(GOLD)肺测量分级II-IV级,基于GOLD 2006分类方案。我们检查了所有受试者的低衰减区百分比(%LAA)差异,并按种族、GOLD肺测量等级分层,在那些早发型COPD和严重肺气肿的受试者中。早发COPD受试者为<55岁,伴有FEV1< 50% (26].重度肺气肿定义为CT上>25%低衰减区(LAA) [27].我们另外调查了Copdgene(当前或前吸烟者> 10包吸烟历史和正常肺活量)的吸烟控制。
射线照相测量
使用在每个临床中心进行的吸气CT扫描测量定量肺气肿(%LAA),并用切片机进行分析[15那25].总肺气肿(%LAA)定义为LAAs小于- 950 Hounsfield单位(HU)的肺的百分比[28].我们还检测了- 910 HU时的LAA %。
统计分析
所有分析都使用R(2.15.1版)进行;https://www.r-project.org/).我们用t检验比较连续变量的均值,用皮尔森卡方分析比较二元变量的均值。我们使用皮尔森相关性来测量包年吸烟与肺气肿的相关性。我们将%LAA转换为自然对数尺度[29],并使用t检验对log %LAA进行单变量比较。我们对log %LAA进行了logistic回归,校正了年龄、吸烟包年、当前吸烟状况和体重指数(BMI)。包括非西班牙裔白人和非裔美国人的分析还根据种族进行了额外调整。我们使用COPDGene中包含的每个CT扫描仪模型的指标变量对CT扫描仪模型进行了调整[30.].对平均%LAA的Logistic回归在在线补充材料中另外提出。我们对使用单一扫描仪(Siemens Definition)扫描的受试者进行敏感性分析,按性别和种族比较男性和女性的log %LAA(见在线补充材料)。我们进行了另一项分析,以检查额外暴露的性别差异及其对肺气肿的影响,包括开始吸烟的年龄、成人二手烟暴露以及职业烟雾、粉尘和烟雾暴露。我们进行逆向选择以确定log %LAA相关的变量,并对结果log %LAA进行多元线性回归,另外对这些协变量进行调整。
结果
主题人口
共有3690名GOLD肺测量II-IV级COPD受试者被纳入分析(表格1).在这些受试者中,有836人是非裔美国人。非西班牙裔白人和非裔美国女性受试者的吸烟包年均少于男性(非西班牙裔白人:50.3±23.7)与60.7±30.2久,p < 0.001;非洲裔美国人:38.7±21.3与45.6±24.0久,p < 0.001)。
定量肺气肿
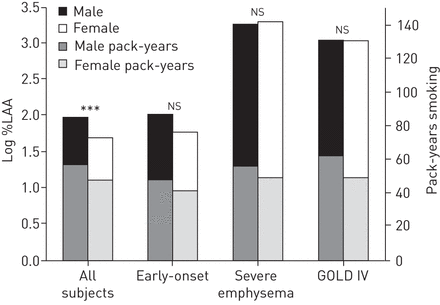
多因素分析比较COPD男性和女性的log %LAA,按种族分层,并根据年龄、BMI、包年、当前吸烟状况和CT扫描仪类型进行调整(图1和表2.),男性肺气肿明显大于女性,均为非西班牙裔白人(2.06±1.3)与1.79±1.5,β= 0.34±0.05,p = 8.37×10−14)和非洲裔(1.63±1.5)与1.31±1.7,β= 0.31±0.10,p = 0.002)。这一趋势随着LAA结果的平均%(在线补充表S1)和使用单一CT扫描仪类型扫描的受试者(在线补充表S2)而持续。当比较%LAA在- 910 HU时的结果时,观察到类似的趋势(在线补充表S3)。在4388例肺功能正常的当前或以前吸烟者中也观察到了log %LAA的性别特异性差异(在线补充)表S4和s5)。
在严重的慢性阻塞性肺疾病(COPD)表型上,对数为低衰减区域(%LAA)和包装岁月。所有科目:非西班牙裔和非洲裔美国人科目;早期出现:早期开放的COPD受试者;严重的肺气肿:COPD受试者> 25%LAA;金四:所有非西班牙裔和非洲裔美国人科目,具有全球慢性阻塞性肺病级IV的倡议。来自Age,Race,Body Mass Mass Index,Pack-Typs吸烟,当前吸烟状态和计算机断层扫描仪类型的推广线性模型的P值。***:P <0.001;ns:不重要的(p > 0.05)。P <0.01对于每个COPD亚型的性别差异的差异。
数年的吸烟和肺气肿
总体而言,男性的烟包年比女性多(表格1).男性和女性吸烟包年与log %LAA显著但弱相关(男性:r=0.12, p<0.001;女性:r = 0.08, p = 0.002)。在所有COPD受试者中,性别和包年的结果log %LAA之间没有显著的交互作用(非西班牙裔白人p=0.69,非裔美国人p=0.97,所有受试者p=0.78)。然而,在所有受试者(p=0.004)和非西班牙裔白人(p=0.01)中,性别和当前吸烟状况之间的交互作用对这一结果具有显著性,但在非裔美国人(p=0.06)中只有这种趋势。在吸烟对照组中,男性每包年吸烟的肺气肿比女性多(p<0.001),但COPD受试者中每包年吸烟的肺气肿数量没有差异(p=0.74)(在线补充表S6)。
定量CT特征及性别与肺功能的关系
为了评估肺气肿量与肺功能的关系是否因性别而异,我们通过GOLD肺测量分级(表3和图2).男性和女性的Log %LAA随GOLD肺测量等级的增加而增加。在GOLD II受试者中,log %LAA的性别差异最为明显(男性:1.39±1.3%)与女性:1.09±1.5%,β=0.36±0.05,p<0.001)。同样,对于IV级COPD,所有受试者的log %LAA在所有受试者中均无差异(3.05±0.85)与3.03±0.91,β= 0.12±0.06,p = 0.07)或非洲裔美国科目中。在非西班牙裔怀特对象中,具有金级IV COPD的雄性在统计学上显着但对数值LAA(男性:3.08±0.8)显示统计学显着但临床上最小差异与女性:3.02±1.0,β= 0.17±0.07,p = 0.02)。男性比整体的女性比女性更高的包装岁月(表格1)和所有GOLD阶段,包括GOLD IV(男性:61.8±31.4)与女性:49.2±24.3,β=11.1±2.3,p<0.001)。在比较各GOLD组按性别划分的LAA平均值时,也存在同样的趋势(在线补充表S7)。当基线FEV1被列入模型中检查了Log%Laa和性别之间的关系,雄性持续多于女性的肺气肿(β= 0.7±0.04,P <0.001)。
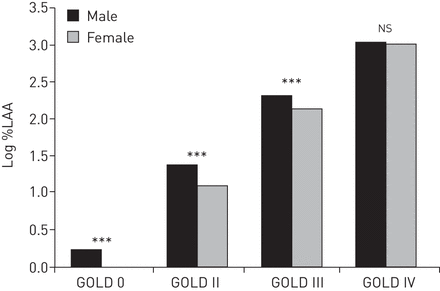
通过肺活动的全局慢性阻塞性肺病(金)等级来记录低衰减区域(%LAA)。广义线性型号的P值调整为年龄,竞赛,体重指数,包数吸烟,当前吸烟状态和计算机断层扫描仪类型。***:P <0.001;ns:不重要的(p > 0.05)。
COPD早期患者的性别特异性肺气肿模式
260例早发型COPD患者(表4.).女性早发型COPD患者的log %LAA与男性相似(女性:1.78±1.6)与男性:2.06±1.4,β=0.13±0.18,p=0.47)。如前所述[26],女性展示了通过FEV测量的类似肺功能1预测百分比(女性:35.52±10.6%与男性:35.52±9.8%,P = 0.99),但少量吸烟(女性:41.0±20.0)与男性:48.2±25.4包 - 年,P = 0.01)。性别与包装较少的互动(P = 0.42)。当比较平均值LAA时,这些趋势持续存在(在线补充表S8)。
以肺气肿为主的受试者的性别特异性肺气肿模式
627例患者胸部CT扫描>25% LAA (表4.).在这个组中,男性比女性多。以肺气肿为主的男性和女性在年龄和肺功能方面相似(表4.).然而,该组的女性比男性的包装较少(女性:49.1±22.1与雄性:56.3±25.8包组,P <0.001),尽管日志%LAA(女性:3.54±0.2与男性:3.54±0.2,p = 0.19)。在比较均值%LAA时也出现了同样的趋势(在线补充表S8)。
环境因素
我们研究了环境暴露与log %LAA之间的关系。总体而言,男性有更多的二手烟接触,包括在工作中接触烟雾,更有可能曾从事有灰尘或烟雾的工作,也更有可能目前从事有灰尘或烟雾的工作(在线补充表S9)。在多变量分析中,被动吸烟(β=0.003±0.001,p=0.02)和工作烟雾暴露(β=0.20±0.05,p<0.001)与log %LAA显著相关,工作中接触二手烟的年份显著(β=0.003±0.001,p<0.07)。将这些协变量加入到多元回归检验log %LAA中并没有改变我们主要分析中注意到的一般趋势。(在线补充表S10)。我们在模型中加入了母亲吸烟和母亲COPD病史,以检验所有受试者和早发受试者中性别与LAA %之间的关系;这些变量的加入并没有影响我们研究结果的总体趋势。
讨论
在对Copdgene受试者的这种分析中,我们证明,尽管雄性在整体上显示出比雌性更大的射线照相肺气肿,但是三种表型亚组(早盘COPD,严重肺气和黄金等级IV COPD)的女性尽管较少的包装数量较少,但仍有相当的射线照片肺气肿。吸烟。这些研究结果表明了一种特别容易受到实质肺部破坏的女性吸烟者的子集。我们的结果显着扩展到以前的研究表明,在聚集体中的COPD受试者中,雄性往往具有肺气肿 - 主要的表型,女性有气道受累[19那21那22那31].这些先前的研究受样本量或受试者确定的限制,因此对COPD受试者特定亚群的适用性有限。鉴于越来越多的人认识到影像学肺气肿是临床上有意义的COPD表型,即使在没有气流阻塞的情况下,我们的发现填补了肺病性别差异的重要知识空白。
早发性慢性阻塞性肺病是一种极端的慢性阻塞性肺病亚群,可能被证明对研究性别特异性遗传因素在慢性阻塞性肺病发展和进展中的作用特别有用。先前的研究表明,早发型慢性阻塞性肺病有一种独特的发病机制,包括性别特异性免疫反应、遗传或表观遗传效应[26].具有早盘COPD的受试者已被证明主要是女性[32,这一发现在对COPDGene的前2500名研究对象的分析中得到了重复[26].连锁和家族聚集研究已经确定了早发型慢性阻塞性肺病的潜在遗传风险因素[33-35];先证者早期COPD女性一级亲属肺功能明显下降[36建议女性可能特别易于这种COPD亚型。我们发现具有早盘COPD的女性具有相同的肺气肿,较少的肺部吸烟是与这些建议一致的。与我们的研究结果相比,campet al。[19]审查了来自国际COPD遗传学网络研究的COPD的证据和他们的兄弟姐妹。在那种人口中,他们发现更多的男性有肺气肿模式和女性气道主要模式。尽管在65岁之前选择了该研究的概念,但受试者的总体差别与此处包含的受试者不同,包括严重COPD的受试者。
我们在肺气肿主要亚组中的发现与来自国家肺气肿治疗审判(Nett)的肺部体积减少手术进行严重肺气肿的观察结果不同。martinezet al。[21研究表明,在这些受试者中,男性肺气肿比女性多,这是通过CT扫描全肺肺气肿百分比来测量的。然而,他们的研究在几个方面与COPDGene进行了对比。NETT研究对象定义为存在严重COPD (FEV)1<45%预测)和受试者被认为是肺粪减少手术的高风险,包括具有非常严重的COPD(FEV1< 20%)。NETT受试者有显著的烟包年吸烟史,男性为71包年,女性为55包年。在COPDGene研究对象中,我们观察到,在重度吸烟者以及肺功能下降最严重的人群中,肺气肿的性别特异性差异不太明显。
我们认为,性别差异在疾病的早期患者(金II)中最引人注目(金II),但对后期疾病相当,这是重要的,因为它可能表明,基于性的肺气肿模式在疾病过程中早期开始,但后来根据额外的易感因素,在雄性和女性中不同的进展。结果与来自国家肺筛查试验的COPD金II-IV的396名受试者的先前研究形成鲜明对比[31].在那项研究中,男性总体而言,他们的肺气肿大于女性。然而,贱民和女性与黄金II COPD之间的疾病和女性之间的差异没有显着差异,而是用于黄金III / IV男性和女性。Copdgene包括更多具有严重COPD的受试者,并且更好地供动力检查该科目子集中的肺气肿差异。此外,本研究当前的研究估计在比较性别之间的肺气肿时占用岁月和吸烟状况。
我们的研究还表明,与非西班牙裔白人的性别差异相比,非洲裔美国人受试者COPD的性别差异类似,但不太明显。在之前对COPDGene研究的前2500名受试者的分析中,HAnsel.et al。[23]观察到非洲裔美国受试者的整体肺气肿较少,而且比非西班牙裔人民更低的低叶片肺气肿。我们证明,非洲裔美国人科目的肺气肿差异较小,但趋势仍然存在。值得注意的是,在我们的研究中,非洲裔美国女性比非洲裔美国男性更高,而非西班牙裔美国人在非西班牙裔美国人看到。这一趋势镜子在美国成年人中看到的一个整体[37].理论上,BMI增加会导致有效辐射剂量降低,人为增加LAA测量值% [30.那38];但是,我们在我们的模型中调整了BMI。
我们选择使用log%laa作为我们的肺气肿的衡量标准。这种终点是通过计算低于一定限度的胸部CT上的体素的百分比,在这种情况下小于-950胡。Slicer方法是计算机算法,因此不受Interobserver变异性的影响。然而,虽然它提供了对整体肺气肿的定量评估,但它尚未解析亚型,例如胰腺,探针和肢体肺气肿。已经开发了几种用于计算肺气肿的方法[39那40]这是一个积极研究的领域。在分析所有这些结果中的性别差异,而且是未来工作的领域,对于此目前的分析,我们选择了既定和验证的方法。
我们的研究有几个局限性。首先,由于%LAA是一个高度倾斜的变量,我们对这个结果进行了对数变换[29];但是,我们认识到,日志变换的值不太简单。我们已经包括对未转化的平均肺气肿的分析进行主要分析(见在线补充材料)。其次,我们试图识别与吸烟史有关的肺气肿的性别特异性差异。我们的研究结果混合了,这可能反映了定量肺气肿与软禁历史的包装或包装年份不存在,或者包装是表征香烟烟雾暴露的最佳度量。包数变量是先前卷烟烟雾暴露的最佳估计;然而,这种变量的能力有限于评估烟雾暴露的影响,因为它假定持续暴露和线性剂量关系。此外,一包香烟可以代表男性和女性的不同剂量,因为女性具有较小的肺部尺寸。雄性和女性之间的肺气肿差异可能与对香烟烟雾的反应的性别特异性差异有关:%LAA与肺功量下降相关[9.],女性慢性阻塞性肺病患者每吸一支烟的肺功能下降幅度大于男性[4.那5.].虽然香烟烟雾显然是工业化国家COPD发展的最重要因素,但其他接触可能影响肺气肿的进展。我们试图研究这些额外暴露的作用,包括二手烟、职业性粉尘和烟雾。尽管暴露于生物质燃料的女性与因吸烟导致肺功能下降的女性表现出不同的肺气肿模式[41]我们的队列被确定,强调当前和前吸烟者。这些结果对于生物质燃料暴露更普遍的区域可能不太稳定。虽然我们研究中的男性对二手烟的暴露有更大的曝光,而职业粉尘和烟雾,我们主要分析的一般趋势在调整额外的曝光后仍然显着。第三,我们不能排除选择偏见的可能性,即。肺病的女性患有肺病和较少的吸烟历史,可能更愿意参加Copdgene研究。最后,身体组成可以影响肺气肿和皮下组织的性别差异的放射线评估可能会影响我们的研究结果;为了克服这一点,正如在先前的研究中所做的那样,我们在我们的回归模型中调整了BMI作为协变量。乳房组织的差异衰减的可能性仍然存在。目前CT扫描技术不考虑乳房组织衰减,这是一种方法开发的一个区域。
放射学肺气肿中明显的性别二型性可能与吸烟剂量对生物学影响的性别特异性差异有关。研究发现,在早发性和以肺气肿为主的人群中,尽管吸烟的包年较少,但女性肺气肿的发生率相当,这表明这些人群中女性对与吸烟相关的实质损伤的易感性增加。慢性阻塞性肺病是一种受不同易感性因素影响的复杂疾病。在不同表型亚群中识别易感性因素是了解COPD总体易感性和性别特异性特征的重要进展。在肺气肿变化后进行纵向研究将是必要的,以澄清吸烟对肺气肿发展和进展的性别特异性影响,并可能确定额外的性别特异性因素导致不可逆的肺实质破坏。
结论
在非西班牙裔白人和非裔美国烟民亚组中,包括COPD晚期、早发型COPD和严重肺气肿患者,男性和女性的肺气肿相当,尽管女性吸烟的包年明显更少。COPD是一种异质性疾病,识别表型不同的亚群仍然是我们理解疾病发病机制的性别二型特征的重要一步。继续对COPD的性别差异进行研究是强制性的,希望能朝着性别特异性一级预防、诊断和治疗的方向前进。
确认
作者要感谢COPDGene的参与者和实地调查人员,感谢他们愿意为医学研究做出贡献。
COPDGENE调查人员:核心单位。行政核心:詹姆斯·克拉皮(主要调查员),Edwin Silverman(主要调查员),Barry Make,Elizabeth Regan。遗传分析的核心:Terri Beaty, Nan Laird, Christoph Lange, Michael Cho, Stephanie Santorico, John Hokanson, Dawn DeMeo, Nadia Hansel, Craig Hersh, Peter Castaldi, Merry-Lynn McDonald, Emily Wan, Megan Hardin, Jacqueline Hetmanski, Margaret Parker, Marilyn Foreman, Brian Hobbs, Robert Busch, Adel El-Bouiez, Peter Castaldi, Megan Hardin, Dandi Qiao, Elizabeth Regan,Eitan Halper-Stromberg, Ferdouse Begum, Sungho Won, Brittney Fredericksen, Sharon Lutz。成像的核心:大卫·a·林奇,哈维o . Coxson美兰k .汉埃里克·a·霍夫曼斯蒂芬·汉弗莱斯,弗朗辛·l·雅各布森,菲利普·f·朱蒂埃拉a . Kazerooni小约翰·d·纽厄尔,伊丽莎白·里根詹姆斯·c·罗斯,劳尔圣何塞Estepar Berend c·斯托尔Juerg Tschirren,伊娃·范·Rikxoort Bram van Ginneken,乔治•Washko卡拉·g·威尔逊,穆斯塔法Al Qaisi Teresa灰色Alex Kluiber, Tanya Mann, Jered Sieren, Douglas Stinson, Joyce Schroeder, Edwin Van Beek。PFT QA核心,美国犹他州盐湖城:罗伯特詹森。数据协调中心和生物统计数据那国家犹太健康,丹佛,美国:Douglas Everett,Anna Faino,Matt Strand,Carla Wilson。流行病学的核心那美国科罗拉多州大学安舒茨医学院John E. Hokanson, Jennifer Black-Shinn, Gregory Kinney, Sharon Lutz, Katherine Pratte。
COPDGene调查者:临床中心。Ann Arbor Va,Mi,USAJeffrey Curtis, Carlos Martinez, Perry G. Pernicano。贝勒医学院,休斯顿,德克萨斯州,美国:尼古拉·哈纳尼亚,菲利普阿拉帕,Venkata Bandi,Mustafa atik,阿拉丁·鲍伊克,卡尔帕··格尔费普......伊丽莎白家伙,Amit Parulekar,Arun Nachiappan。Brigham和女子医院,波士顿,马,美国:Dawn Demeo,Craig Hersh,George Washko,Francine Jacobson。哥伦比亚大学,美国纽约: R. Graham Barr, Byron Thomashow, John Austin, Belinda D'Souza, Gregory D.N. Pearson, Anna Rozenshtein。杜克大学医学中心,达勒姆,NC,美国:小尼尔·麦金太尔、莱西·华盛顿、h·佩奇·麦克亚当斯。卫生伙伴研究基金会,明尼阿波利斯,明尼苏达州,美国: Charlene McEvoy, Joseph Tashjian。约翰霍普金斯大学,美国博尔的摩,美国:Robert Wise,Nadia Hansel,Robert Brown,Karen Horton,Nirupama Putcha。洛杉矶生物医学研究所港口UCLA医疗中心,洛杉矶,加州,美国,美国:Richard Casaburi,Alessandra Adami,Janos Porszasz,Hans Fischer,Matthew Budoff,Dan Cannon,Harry Rossiter。Michael E. DeBakey VAMC,休斯顿,德克萨斯州,美国:Amir Sharlafkhaneh,Charlie Lan。美国明尼苏达州明尼阿波利斯市:Brian Bell Christine Wendt。美国乔治亚州亚特兰大莫尔豪斯医学院Marilyn Foreman, Gloria Westney, Eugene Berkowitz。国家犹太健康,丹佛,美国:罗素·鲍勒,大卫·林奇。美国马萨诸塞州伍斯特的Reliant医疗集团: Richard Rosiello, David Pace。美国费城天普大学:Gerard Criner,David Cicchella,Francis Cordova,Chandra Dass,Robert D'Alonzo,Parage Desai,Michael Jacobs,Steven Kelsen,Victor Kim,A. James Mamary,Nathaniel Marketti,Aditti Satti,Kartik Shenoy,Roberti M. Steiner,AlexSwift,Irene Swift,Gloria Vega-Sanchez。阿拉巴马大学,伯明翰,美国,美国: Mark Dransfield, William Bailey, J. Michael Wells, Surya Bhatt, Hrudaya Nath。加利福尼亚大学,圣地亚哥,加州,美国:Joe Ramsdell,Paul Friedman,Xavier Soler,Andrew Yen。爱荷华大学大学,爱荷华州,IA,美国:Alejandro Cornellas,John Newell Jr,Brad Thompson。Michigan大学,Ann Arbor,MI,USA:韩美兰,艾拉卡泽罗尼,费尔南多马丁内斯。明尼苏达大学,明尼阿波利斯,美国: Joanne Billings, Tadashi Allen。匹兹堡大学,匹兹堡,帕,美国: Frank Sciurba, Divay Chandra, Joel Weissfeld, Carl Fuhrman, Jessica Bon。美国德克萨斯州圣安东尼奥的德克萨斯大学健康科学中心:安东尼奥·安祖托,桑德拉·亚当斯,迭戈·马塞利-卡塞雷斯,马里奥·e·鲁伊斯。
脚注
对于编辑评论看EUR RESPIR J.2016;47: 19 - 22日(DOI:10.1183/13993003.01781 -2015].
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:R01 HL089438,K12 HL120004,R01 HL089856,R01 HL089897,R01 HL089897,P01 HL105339,2013HL105339,2013 Sheila J. Goodnight,MD,女性肺部健康中的FCCP临床研究授予。所描述的COPDGENE项目由奖励号码R01 HL089897和国家心脏,肺和血液研究所获得奖励号码R01 HL089856。内容完全是作者的责任,并不一定代表国家心脏,肺和血液研究所的官方意见或国家卫生研究所。COPDGENE项目也得到了COPD基金会,通过对由Astazeneca,Boehringer Ingelheim,Novartis,Pufire,Siemens,Sunovion和Glaxosmithkline的行业咨询委员会所作的捐款提供支持。本文的资助信息已存入乐趣。
利益冲突:披露可以在本文的在线版本旁边找到www.qdcxjkg.com
- 收到了2015年6月23日。
- 公认2015年9月5日。
- 这项工作的内容是作者或其雇主的版权。设计和品牌的版权所有©ers 2016