摘要
四端粒相关基因的杂合突变已与肺间质纤维化,但鲜为人知的是,相似或受影响的个体差异。
115例端粒酶逆转录酶突变(TERT)(N = 75),端粒酶RNA组分(TERC) (n=7),端粒延伸解旋酶1 (RTEL1) (n=14)和poly(A)特异性核糖核酸酶(PARN) (n=19),并对临床资料进行分析。
大约二分之一(46%)有特发性肺纤维化(IPF)的多学科诊断;他人已经分类的肺纤维化(20%),慢性过敏性肺炎(12%),pleuroparenchymal弹力纤维增生症(10%),与自身免疫特征(7%),特发性间质性肺炎(4%)间质性肺炎和结缔组织疾病相关间质性纤维化(3%)。不和谐的间质性肺疾病诊断患病个体中发现,从家庭的80%。患者TERC突变比那些有突变的人在更早的年龄被诊断出来PARN突变(51±11年与64±8年;p=0.03)和较高的发病率血液学共病。平均肺活量下降速率为300毫升·年-1死亡或移植的平均时间是2.87年。基因突变组和诊断为IPF的患者在死亡或移植时间上没有显著差异与non-IPF诊断。
在端粒相关基因的遗传突变导致多种间质性肺病(ILD)是普遍渐进诊断。
摘要
四端粒相关基因的突变导致进行性肺纤维化,无论ILD诊断http://ow.ly/TH2B300Yjvt
介绍
肺间质疾病是一种异质性疾病的集合,其特征是细胞外基质在肺间质内沉积,导致咳嗽、呼吸急促和缺氧。特发性肺纤维化(idiopathic pulmonary fibrosis, IPF)是一种独特的慢性肺纤维化,表现为肺功能的破坏性进行性下降,通常导致呼吸衰竭[1,2]。IPF的原因仍不清楚,但最近的研究牵连端粒缩短的主要贡献者其发病机制与生存特性[3-五]。
端粒酶是一种反转录酶,其细胞复制过程中添加TTAGGG重复染色体末端。在端粒酶的蛋白成分突变(TERT)和酶的RNA成分(TERC)导致短端粒长度和家族性肺纤维化[6,7]。TERT突变是家族性肺纤维化患者中最常见的突变,约有15%的家族性肺纤维化患者发生突变[8]。dyskerin突变(DKC1)和TRF1相互作用蛋白2(TINF2)也已经在患者的家族间质性肺炎发现[9,10]。最近,其他两个基因,RTEL1和PARN已经具有缩短的端粒长度和家族性肺纤维化相关联11-13]。因此,六端粒相关的基因都与这种疾病。RTEL1编码含有a的蛋白质ñ末端解旋酶DNA复制过程中卷出端粒T环结构。PARN有助于poly(A)的特异性成熟TERCRNA与端粒长度的维持[14]。基因剂量的证据以两份有害副本的形式存在TERT[15],RTEL1[16-18),PARN[14,19,20.]已经在幼儿先天性角化不良和多脏器疾病,包括肺纤维化被发现的突变。
在临床上,与非IPF肺间质疾病相比,IPF的诊断可预测更快的疾病进展和更短的预期寿命[21]。端粒长度也被证明与IPF患者较短的预期寿命有关[五,22]和肺纤维化的患者的之前描述TERT突变已经表明,许多具有IPF [临床诊断6-⇓⇓8]。我们试图测试的假设肺纤维化患者由于杂合基因突变TERT,TERC,RTEL1或PARN共有一个共同的临床表现型(IPF)和一个渐进的临床过程。
方法
研究设计和参与者
在这项观察性队列研究中,德克萨斯大学西南医学中心(UTSW;达拉斯,TX,美国)或被推荐从不同的学术医疗中心参与。该研究得到了新南威尔士大学机构审查委员会的批准,并获得了所有受试者的书面知情同意。64个家系中有38个(59%)曾被报道;本研究对每个病例的临床资料进行了独立回顾。在28例病例中,可以从系谱结构和活的家庭成员的基因分型推断出受影响个体中是否存在基因突变。在所有这些病例中,突变的存在仅被认为是基于个体在具有已确认的变异的受试者之间的系谱中的位置而必须携带的个体。收集受试者的临床资料,包括人口学资料、实验室结果、肺功能测试、影像学研究和肺组织病理学标本。种族是自我报告或家庭报告。来自19-89岁健康对照组参与者的基因组DNA样本[3,五,8)是从来自美国德克萨斯州达拉斯的一组不相关的多种族个体中获得的。
程序
基因组DNA从循环的白细胞中分离出使用自定位LS (Qiagen, Valencia, CA, USA)。循环白血病细胞基因组DNA的端粒长度使用先前描述的定量PCR测定[3,五,8和端粒与单个复制基因(T/S)或年龄调整端粒长度的对数转换相对比。测序的叔,TERC RTEL1和PARN基因的表现如前所述[7,11]。没有突变DKC1[9] 要么TINF2[10]是在这个队列中。临床检查和管理是由当地医生指导。为了考虑行为的变化,所有数据均采用目前临床指南,建立一个多学科的诊断[独立审查2,23,24]。
现有的胸部计算机断层(CT)图像(n=73)由一名胸部放射科医生(K. Batra)进行复查,他对临床病史、突变分析、端粒长度和组织病理学均不知情。扫描分为31种不同的影像学特征,并分为三种影像学类型之一:明确的常见间质性肺炎(UIP)、可能的UIP和与UIP不一致的UIP [2]。
可用的肺组织病理标本(n = 42)用谁是失明的临床病史,突变分析,端粒长度和放射线照相特性的肺病理学家(J.托雷亚尔瓦)进行分析。可用的标本,包括外科肺活检和肺外植体,进行分级为15个不同的组织病理学特征。每个试样按照制定的准则中给出一个组织病理学诊断23]。
统计分析
使用单因素方差分析(用于连续变量)或Fisher精确检验(用于分类变量)比较患者组的特征。诊断年龄的差异用线性回归测试,包括基因和世代作为预测因素(或用t检验,当只有两代时)。端粒长度相对T/S比采用对数变换,确保残差为正态分布,方差恒定。我们使用对照组参与者的线性回归估计了端粒长度和年龄之间的关系,如前所述[五]。估计的回归系数被用来计算观察减去预期的,或年龄调整,每个受试者的端粒长度。
肺功能测试的变化(PFT)的特性,使用线性混合效应模型患者至少有两个单独的PFT测量进行分析。我们包括年龄和性别作为协考虑到年龄和第一PFT测量的时间差异和性别比例的各种基因。为了测试在PFT变化率是否取决于年龄和性别,我们最初包含在模型中的年龄×时间和性别×时间相互作用项。在单独的模型,我们测试了平均PFT特性或在PFT变化率是否依赖于端粒长度或诊断,通过包括用于端粒长度(>第10百分位或<第10百分位)的固定效应或诊断的术语(IPF或非IPF)和模型时间依赖性相互作用项。该无统计学显著(p-值> 0.05)条款被排除在最终模型。使用受限制的最大似然过程的参数估计。需要随机效应,使用似然比测试评估。
平均无移植存活时间(从诊断到移植或死亡)和总生存率采用Kaplan-Meier曲线计算。Cox比例风险模型被用来评估的年龄,性别的影响,临床参数(用力肺活量(FVC)%预计一氧化碳弥散肺容量(dLCO)、基因突变载体群、端粒长度、诊断(IPF)与非IPF)上无移植存活时间。所有分析,使用R版本3.2.2统计分析软件(执行www.R-project.org)。
结果
患者特征
我们确定了来自64个家族的115名肺纤维化患者,他们的四种与端粒缩短相关的基因中有一种发生了突变:TERT,TERC,RTEL1和PARN(N = 75,图7,分别为14和19)。每个基因突变是罕见和独特的在它被发现的家庭。38个(60%)的家庭只有一个患病个体被列入(补充表S1)。与单基因肺纤维化主题特征描述表1和2。大多数受影响的人是白种人。更多受影响的女性被发现患有TERC(86%)或PARN(53%)的突变,虽然这个结果没有达到在所有基因组比较有统计学意义。While the mean age at diagnosis for all mutation carriers was 58 years old, individuals withTERC突变were diagnosed at a younger mean age (51±11 years) andPARN突变携带者的平均年龄较晚(64±8岁,p=0.03)。我们没有发现吸烟对诊断年龄有影响的证据。与受试者相比TERT突变,年龄调整的端粒长度PARN突变携带者较长(- 0.36±0.14)与−0.58±0.27;p = 0.013)。同样,更高的百分比PARN突变携带者的血白细胞端粒长度为>的十分之一(40%)与13%;p值= 0.049)。
贫血和大细胞增多症是最常见的血液学异常,分别占总队列的28%和24%。TERC肺纤维化突变携带者白细胞减少、血小板减少、再生障碍性贫血或骨髓增生异常综合征的发生率较高(p<0.05) (表2)。两名受试者RTEL1突变(14%)有肺癌,当与其它基团(P = 0.017)相比,在统计学上是显著。癌症总发生率为9.7%。附加comordid条件在补充表S2呈现。
临床诊断ILD
在有足够数据进行多学科诊断的77名受试者中,35名(46%)诊断为IPF (表1)。最常见的非ipf诊断包括无法归类的肺纤维化(20%)、慢性过敏性肺炎(12%)和胸膜实质纤维弹性变性(10%)(图1a-F)。两名结缔组织病相关的ILD患者被诊断为硬皮病。基因组间的ILD诊断分布差异无统计学意义。
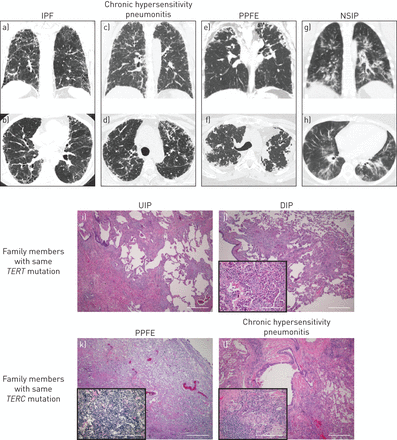
在杂合子受试者间质性肺疾病诊断的光谱叔,TERC RTEL1或PARN突变。代表日冕(a、c、e, g)和轴向(b、d、f、h)胸部电脑断层扫描的图像诊断患者的a和b)特发性肺纤维化(IPF), c和d)慢性过敏性肺炎、e和f) pleuroparenchymal fibroelastosis (PPFE)和g和h)非特异性间质性肺炎(NSIP)。来自i和j)相同的相关ILD受试者的代表性的苏木精和伊红染色肺切片TERTc。2594G>A (R865H) mutation and k and l) the sameTERCr。182g>c mutation. i) Usual interstitial pneumonia (UIP) pattern with temporal and spatial heterogeneity and fibroblastic foci at the interface between normal and fibrotic lung in a 53-year-old man who underwent lung transplantation. j) Desquamative interstitial pneumonia (DIP) with organising pneumonia, thickened interstitial septi and presence of intra-alveolar pigmented macrophages (inset) in a 68-year-old never-smoker (scale bar=500 µm; inset scale bar=200 µm). k) Pleuroparenchymal fibroelastosis (PPFE) with diffuse elastic fibre deposition (inset) near the pleural edge in a lung explant from a 60-year-old female at the time of lung transplantation (scale bar=500 µm; inset scale bar=500 µm). l) Features of chronic hypersensitivity pneumonitis with bronchiolocentric fibrosis, patchy lymphoid aggregates, bridging fibrosis and loosely formed granulomas (inset) in a lung explant from her 57-year-old sister (scale bar=500 µm; inset scale bar=500 µm).
同一家庭受影响的成员经常有不和谐的诊断,尽管他们相同的种系基因突变的继承。对他们来说,多学科的ILD诊断为≥2受影响的家庭成员提出的15个不同的家庭(表3),在12个(80%)家庭中发现了不一致的诊断,在3个(20%)家庭中发现了一致的IPF诊断。图1I-升显示肺部有来自两个家庭不和谐诊断个体的组织病理学。
胸部CT与组织病理学的相关性
73箱子了胸部CT扫描供审查。这些被分为三种影像学模式之一:明确UIP,可能UIP,不符合UIP(补充表S3)。所有CT扫描的近二分之一(47%)所表示的一定的UIP图案。总体来看,三分之一的扫描用可能UIP一致和扫描的20%,被认为是与UIP模式不一致。
我们发现肺气肿和基因组(p = 0.032)之间的显著关联。与其他基因组,较高比例的比较RTEL1突变携带者(40%)和TERT突变携带者(40%)有肺气肿的放射学证据(p=0.026和p=0.028;补充表S4)。我们还发现了肺气肿和吸烟之间的联系(p=0.015)。
42例手术肺标本可供复查(补充)表S5)。UIP的组织病理学诊断有21例(50%)。镜下见33例(78%)人出现蜂窝,34例(80.9%)人出现纤维母细胞灶。具有不同基因突变的受试者的组织病理学模式没有统计学上的显著差异。
我们评估了34名同时拥有胸部CT和组织病理学标本的受试者的影像学和组织病理学诊断之间的相关性。在明确的UIP和可能的UIP的x线诊断病例中,分别有61%和38%的UIP的病理诊断(补充)表S6)。这被认为是与UIP不符合胸部CT扫描的情况下一半了UIP的组织病理学诊断。
基因预测
在这个队列中,有九个家庭(四连TERT,两个RTEL1和三连PARN突变)与来自不止一代人。我们发现了在携带者遗传早TERT和RTEL1突变(p=0.003和p=0.018),但没有突变PARN突变(图2a)。
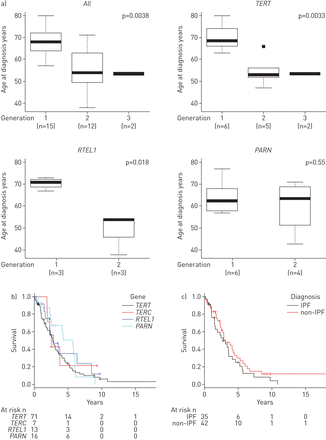
间质性肺病(ILD)杂合子受试者的临床特征叔,TERC RTEL1和PARN突变。一)遗传早的证据与ILD诊断的患者中九家系后代较早的年龄,其中包括四连TERT突变,两RTEL1突变和三连PARN突变。分析中包含的个体数量列在x轴上。b) ILD患者无移植存活叔,TERC RTEL1和PARNKaplan-Meier生存图中描述的突变。不同基因组的生存特征无显著差异。c)患者无移植存活叔,TERC RTEL1和PARN突变和特发性肺纤维化(IPF)或如在Kaplan-Meier存活曲线图所示的非IPF诊断的诊断。有跨越两个诊断组的生存特性之间没有显著差异。
疾病进展与生存
平均下降FVC was 300 mL·year-1(范围260-350毫升·年-1跨基因组)(表4)。平均下降dLCO1.7毫升·敏吗-1每毫米汞柱·年-1。两组间的植被覆盖度无显著性差异dLCO基因或诊断的差异。值得注意的是,FVC的平均下降速率为299 mL·年-1和296毫升·-1分别适用于诊断为IPF或非IPF的患者。
在随访期间,59(51%)名患者死亡,34(30%)名患者接受了肺移植(表5)。总体而言,所有患者死亡或移植的中位时间为2.87年(95% CI 2.40-3.80)。不同基因组、IPF患者和非IPF患者死亡或移植的中位时间没有显著差异。4个基因组的ILD患者的无移植性生存率无显著性差异(p=0.63),差异有统计学意义(p=0.63)图2b。四组患者的总体生存率也没有显著差异(p=0.86,数据未显示)。对于诊断为IPF或非IPF诊断的患者,这四个基因之一发生突变的患者的无移植生存期无显著差异(p=0.25),并显示在图2c。
在未经调整的Cox分析中,预测的基线FVC %与患者的无移植存活密切相关(每10个百分点FVC差异的HR 0.65 (95% CI 0.53-0.79), p<0.0001) (表6)。无移植生存的其他未调整的预测因素包括:诊断时年龄(HR 1.02(1-1.04),P = 0.046)和男性(HR 1.6(1.04-2.44),P = 0.031)的时间。的各种基因的突变,端粒长度和诊断亚型(IPF与在未经调整的分析中,非指规数与生存率无显著相关性。在对相关的个体协变量进行调整后,FVC %预测仍然是无移植存活时间的独立预测因子(HR 0.93 (0.89-0.98), p=0.004),而端粒长度没有。
讨论
基因突变的叔,TERC RTEL1和PARN端粒病与短端粒综合征或“端粒病”的发展有关,其特征是全身异常,包括肺纤维化、骨髓功能障碍、肝硬化和早期变灰。到目前为止,对这些基因中遗传突变个体的表型描述一直局限于有先天性角化障碍的儿童患者和有各种该疾病表现的成人患者的报告。总的来说,肺纤维化似乎是与端粒酶突变相关的最常见的表型[25]。在这里,我们研究了大量年龄较大的端粒罕见杂合子相关突变的成年患者,这些患者是根据家族性肺纤维化表型收集的。我们发现,该队列在血液学、胃肠和肺气肿表型的临床表达方面表现出相似性和差异性,这在其他队列中已经得到了注意[26-28]。例如,我们发现中发现多发于那些具有严重的血液疾病TERC突变。我们在该队列中观察到的肝脏表型似乎比其他人所描述的要温和[27,29]。放射学上的肺气肿表型不仅与吸烟有关TERT突变组作为最近已有描述[28],而且还与相关联的RTEL1基因。
77个科目在这个队列对他们来说,多学科的诊断成立,我们发现,46%符合诊断标准的IPF。其他诊断包括原因不明(非特异性间质性肺炎,脱屑性间质性肺炎,pleuroparenchymal弹力纤维增生症),以及其他特发性间质性肺炎如ILD归因于已知的原因(慢性过敏性肺炎和结缔组织疾病相关的ILD)。超过50%的受影响的个人的有比其他IPF诊断。ILD患者端粒短长度的其他研究也发现非IPF诊断的高比例,其中包括过敏性肺炎,未分类的间质性肺炎和合并肺纤维化和肺气肿[30.,31]。我们发现,在亲缘族中有80%相同的遗传性罕见突变的影响个体间的不和谐诊断。这在同一个家庭程度的表型异质性是高于原来的S发现teele等。[32]在一个家族性间质性肺炎的队列(45%)。
有跨越患者差基因型 - 表型ILD相关性不同的端粒相关的基因突变。肺纤维化的位置(下叶,上叶,外周气道为中心的),肺破坏的图案(微囊与大囊性蜂窝状结构,细胞外基质在肺内沉积的性质(胶原蛋白、弹力蛋白、染色蛋白的同质性)和重塑的时间范围(同质性)与多相)很可能受其它因素,遗传和环境来控制。例如,公共MUC5B风险多态性(rs35705950)与射线照相和组织病理学UIP图案相关联33]。性别可能是另一个因素,因为我们发现,患者pleuroparenchymal弹力纤维增生症的群主要是女性(88%)。其它因素可包括纤维化环境暴露的持续时间和程度,以及在某些肺细胞的端粒缩短的后生或随机效应。例如,有气道为中心的纤维化诊断为慢性过敏性肺炎的个体空气滞留的证据;在这些情况下,吸入纤维化环境用药可能导致更多轮细胞分裂和周围小气道肺上皮细胞气道的更极端的端粒缩短的。
然而,在所有的基因突变看到了一个一致的表型进行性恶化。在这些单基因ILD患者看到的PFT平均下降率比一般的还要快。We find a mean change in FVC of −300 mL·year-1,-7.4 FVC%每年和预测-5.8dLCO预测有端粒杂合相关基因突变的受试者每年的百分比。相比之下,在多个IPF临床试验安慰剂组的患者中,FVC下降的中位数为每年130-210 mL-1[34在肺硬皮病研究的安慰剂组中,受试者的年下降率为预测的2.6±0.9 FVC %和3.5±1.0dLCO每年%的人预测[35]。患有这些突变代表了一种极端的表型,类似于那些已经被归类为快速进展性疾病[36,37]。
We found that there was no difference in survival of patients categorised by diagnosis, as those with a diagnosis of IPF have a median survival of 2.75 years (95% CI 1.64–4.61) and those with a non-IPF diagnosis have a nearly equivalent survival of 3.11 years (2.56–4.82). This finding is different from historic studies demonstrating a worse survival for IPF patients with a UIP histopathology [21并提出,与特定的临床诊断或组织病理学模式相比,遗传的端粒相关突变的效果更能预测加速进展。由于缺乏预后意义的组织病理学和发病率与手术肺活检,手术肺活检的风险和利益,应仔细考虑这些端粒相关基因突变的患者。提高警惕和早期转诊进行肺移植评估是必要的,即使是非ipf诊断。
四个基因突变群体,我们发现在ILD科目最长的白细胞端粒长度与PARN突变,其与先前的报告一致[11]。不同基因突变组患者的平均端粒长度依次为:<叔,TERC < RTEL1 < PARN。这些不同基因突变组的ILD患者的平均诊断年龄差异有统计学意义,且均符合上述顺序TERCmutation carriers diagnosed at the earliest age (51 years), followed byTERT突变携带者(58岁)RTEL1mutation carriers (60 years) andPARNmutation carriers (64 years). Similarly, there was a statistically significant higher prevalence of severe haematological comorbid conditions such as leukopenia, thrombocytopenia and aplastic anaemia/myelodysplastic syndrome in theTERC突变组和在这些血液学条件低流行RTEL1和PARN突变组。虽然没有统计显著,平均死亡时间或移植遵循相同的趋势。
本研究是一项观察队列研究,因此,在确定成人肺纤维化表型的基础上存在一定的偏差。病人在不同的地点接受治疗,医生的执业模式也大不相同。尽管我们尽了最大努力通过回顾所有的主要临床数据来提供一致的多学科诊断方法,但由于缺少或无法获得胸部CTs、外科肺活组织检查或肺外植体,我们无法确定38例患者的诊断。该研究还受到缺乏对照队列控制的地区和时间临床实践以及遗传特征的限制。考虑到具有某些非ipf诊断的少数患者,如无法分类的肺纤维化和慢性过敏性肺炎,我们无法直接评估这些个体组的PFT进展率或移植无存活率。大量接受肺移植的患者可能影响了与生存相关的研究结果。然而,敏感性分析审查移植或把它作为一个竞争风险证明了定性相似的结果(数据未显示)。由于不同的做法,我们不能很容易地评估IPF患者在fda批准的药物或慢性过敏性肺炎,结缔组织疾病相关的ILD或免疫抑制药物的IPAF患者的疾病进展。
综上所述,突变的端粒维持机制的基因叔,TERC RTEL1和PARN导致可变间质性肺疾病的表型和诊断。虽然具体的ILD诊断可能是在治疗方法和预后例散发性疾病而言重要的是,这项研究表明,突变的四个不同的端粒相关基因的影响预测类似的致病机制,表现为进行性肺纤维化和生存率下降。另外的研究将是需要的确定端粒长度的相对效用和基因突变作为生物标志物用于在患者的家族性肺纤维化预测治疗性治疗和结果。
确认
作者感谢向患者及他们在这项研究和阿什利·扬(德克萨斯大学达拉斯西南医学中心,达拉斯,德克萨斯州,美国)为她的技术专长参与的家庭。
脚注
在编辑点评:欧元和J2016年48:1556年至1558年。
这篇文章有提供补充材料www.qdcxjkg.com
支持声明:在作者承认资金来源如下支持:美国国立卫生研究院,美国国家心脏,肺和血液研究所:5T32HL098040(C.A.牛顿),UL1TR001105和R01HL093096(C.K.加西亚);中心和全国推进转化科学。本文资金的信息已交存资助者打开注册表。
利益冲突:披露可以这篇文章在旁边找到www.qdcxjkg.com
- 收到了2016年2月10日。
- 公认2016年5月31日。
- 版权©2016人队