摘要
目前估计阻塞性睡眠呼吸暂停(OSA)严重程度的诊断参数与OSA患者的精神运动警觉性关系不佳。因此,我们旨在研究呼吸暂停、低通气和间歇性低氧血症的严重程度与警觉性受损的关系。
我们回顾性检查了743名连续OSA患者(呼吸暂停-低通气指数(AHI)≥5个事件·h)的I型多导睡眠记录仪数据和相应的精神运动警戒任务(pts)−1).常规诊断参数(如。AHI和氧去饱和指数(ODI))和新参数(如。评估去饱和严重程度和梗阻严重程度),包括呼吸暂停和低通气的持续时间以及去饱和的深度和持续时间。根据PVT结局变量将患者分组为四分位数。评估了属于表现最差的四分之一的几率。所有PVT结果变量均采用二项逻辑回归分析。
去饱和的中位深度相对增加10%,会增加患病几率(OR范围1.20 ~ 1.37, p<0.05),平均反应时间和中位反应时间延长,延迟计数增加。类似地,去饱和严重程度(OR范围1.26 ~ 1.52, p<0.05)与中位反应时间延长有关。女性(或范围2.21 ~ 6.02, p<0.01), Epworth嗜睡量表得分(OR范围1.05 ~ 1.07, p<0.01)范围1.01 ~ 1.05, p<0.05)均为显著危险因素。相比之下,常规AHI、ODI和唤醒指数的增加与PVT性能恶化无关。
这些结果表明,我们描述间歇性低氧血症严重程度的新参数与PVT性能受损的风险增加显著相关,而传统的OSA严重程度和睡眠碎片指标则不是这样。这些结果强调了在AHI之外发展OSA严重程度评估的重要性。
摘要
考虑去饱和特征的参数与警觉性受损有显著关联,突出了开发AHI之外的方法以更详细地评估OSA严重程度的重要性http://bit.ly/2veqxD9
简介
由于睡眠障碍和睡眠时间缩短而导致的睡眠不足,在西方国家被广泛认为是一个重大的公共卫生负担[1].良好的睡眠质量对于维持神经认知能力至关重要。1].相反,越来越多的职业事故和缺勤,以及交通事故,都是由睡眠质量下降的因素造成的。1].仅在澳大利亚,2016-2017年期间,睡眠不足造成的医疗和社会成本估计为450亿美元[1].阻塞性睡眠呼吸暂停(OSA)是最常见的睡眠障碍之一,在西方国家影响了≥20%的成年人[2- - - - - -4].阻塞性睡眠呼吸暂停症是由于白天睡眠潜伏期缩短,以及慢性疲劳和嗜睡[5- - - - - -7].此外,阻塞性睡眠呼吸暂停与神经认知能力差和无法保持注意力有关[8- - - - - -10].
《精神疾病诊断与统计手册》定义的神经认知障碍涵盖学习和记忆、语言、执行功能和复杂注意力等领域[11].精神运动警戒任务(PVT)评估复杂注意领域,通过测量对视觉刺激的重复反应来评估受试者维持注意力的能力[8,12].PVT是一种快速、客观、易于解释的测试,学习效果很小[13].PVT被认为是高度可靠和敏感的睡眠剥夺对认知表现的影响,并清楚地表明,当一个人无法保持注意力时,在任务期间表现的累积恶化[14].由于用于客观评估困倦的临床资源有限,主观问卷不可靠,PVT可用于,例如,作为驾驶适能的初步评估[15,但限制条件是,驾驶除了需要持续的注意力外,还涉及其他复杂的技能。
研究发现,急性睡眠剥夺会损害PVT的表现[16]和长期睡眠不足[9],但个体间的反应也有很大差异[17].此外,PVT结果恶化与描述OSA严重程度的常见临床参数之间的关联(即。呼吸暂停-低通气指数(AHI))或睡眠破碎程度(即。唤醒指数)是模棱两可的[9,18- - - - - -22].先前的研究表明AHI的增加与警觉性受损没有直接联系[9,22].尽管与健康个体相比,严重OSA患者的PVT表现平均较差,但据报道,OSA严重组之间PVT表现没有显著差异[9,22,23].然而,OSA患者缺乏差异可能与AHI的任意、过时和次优严重程度分类阈值有关[24,25].
尽管AHI与PVT性能降低没有很好的相关性,P消等.[9]报道了PVT患者的表现受损似乎是由于长期睡眠剥夺和睡眠时间不足造成的。此外,先前的研究表明,夜间间歇性低氧血症水平对OSA患者的PVT表现有负面影响[10,18].年代加油等.[18]表明,错误次数与最低血氧饱和度和平均血氧饱和度适度相关(r分别=−0.454和−0.421),但这是在1000 ms的非典型长反应时间限制下实现的。此外,我们最近证明,不论AHI如何,时间更长、饱和度更深的去饱和会显著增加客观测量的白天过度嗜睡的风险[7].
基于间歇性低氧血症与OSA患者日间功能受损之间的这种明显联系,我们假设考虑呼吸事件持续时间以及去饱和的深度和持续时间的新颖、更复杂的诊断参数与PVT性能受损的关联比传统的严重程度指标(如AHI和氧去饱和指数(ODI))更强。在这项研究中,我们在一个大的患者队列中调查了哪些OSA严重程度指标与PVT表现不佳相关。此外,我们还研究了去饱和的严重程度如何独立于呼吸事件的次数和总持续时间而影响PVT性能。
患者与方法
这是一项对912名因怀疑OSA而在亚历山德拉公主医院(布里斯班,澳大利亚)睡眠障碍中心接受多导睡眠描摹(PSG)的连续患者的回顾性分析。亚历山德拉公主医院机构人类研究伦理委员会批准了回顾性数据收集(HREC/16/QPAH/021, LNR/2019/QMS/54313)。未能完成pvt的患者(n=32) AHI <5次·h−1(n=134)或人口统计信息缺失(n=3)被排除。因此,研究的患者群体包括743人,他们成功地接受了1型诊断PSG, AHI≥5次·h−1PVT于PSG前19:00 - 21:00 h进行。整个患者群体的人口统计信息显示在表1.2015-2017年期间,使用Compumedics Grael采集系统和Compumedics ProFusion PSG 4软件(Compumedics, Abbotsford, Australia)进行PSG录音并进行评分。
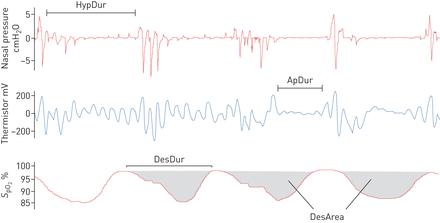
所有的PSG录音都由经验丰富的睡眠技术人员手动评分,他们定期参加评分协调活动。根据美国睡眠医学学会2012年指南,对所有呼吸暂停、低通气和去饱和进行手动评分[26].如果观察到鼻压振幅降低≥30%且持续≥10 s,并伴有≥3%的去饱和和/或觉醒,则为低通气(推荐低通气规则4A [26])。如果观察到热敏电阻信号在≥10秒内振幅降低≥90%,则为呼吸暂停。如果氧饱和度信号下降≥3%,则手动评分为氧饱和度降低事件(年代阿宝2)用脉搏血氧计测量,观察。从去饱和开始前的最后一个采样点到恢复达到基线点(图1).如果未达到基线,则在降饱和后的平台期开始时确定终点(图1).
与新参数相关的变量的示意图表示。HypDur:低通气持续时间(秒);ApDur:呼吸暂停持续时间(s);DesDur:去饱和持续时间(s);DesArea:去饱和区域。
对于PVT,使用ASUS变压器垫(台北,台湾)上的心理实验建筑语言PVT程序,并附带键盘[27].PVT采用10分钟方案进行,每隔2 - 10秒进行120次视觉刺激。患者被指示监视平板显示器,并在屏幕上出现粉色刺激时立即用惯用手的食指或拇指按下响应按钮。记录标准PVT结果:中位反应时间(RT)、平均互反反应时间(RRT)、最慢10% RT的平均值、最快10% RT的平均值和失效次数(RT >500 ms)。
生年代阿宝2信号、催眠图和信息(如。将评分的呼吸暂停、低呼吸、觉醒和去饱和事件的持续时间、开始时间和结束时间)从ProFusion导出到MatLab(版本R2018b;MathWorks, Natick, MA,美国)。总睡眠时间(TST)以及TST中非快速眼动睡眠和快速眼动睡眠的百分比基于手动睡眠分期结果。AHI,氧饱和度指数(ODI),觉醒指数,夜间平均氧饱和度(mean年代阿宝2),夜间最低氧饱和度(min年代阿宝2),与年代阿宝2< 90% (t90%),计算去饱和深度的平均值和中位数。此外,新的参数(梗阻持续时间、去饱和持续时间、去饱和严重程度和梗阻严重程度)(表2)中所描述的[28- - - - - -30.],根据呼吸和去饱和事件信息和原始数据计算年代阿宝2信号与定制MatLab函数。分析中考虑了所有类型的呼吸暂停(阻塞性、混合性、中心性),没有患者患有中枢性睡眠呼吸暂停。即。中心事件的百分比<所有事件的50%。生理上不相关的年代阿宝2数值(≤50%)在减饱和度范围内或在最小值内年代阿宝2被认为是人工制品,未用于分析。
梗阻持续时间参数表示呼吸暂停总持续时间的百分比(图1而且表2)和低通气(图1而且表2)。类似地,去饱和持续时间参数表示去饱和总持续时间的百分比(图1而且表2)。去饱和严重程度参数表示去饱和事件的严重程度(即。减饱和区)(图1而且表2)由TST标准化。通过使用每个单独的去饱和事件的开始和结束时间,并对相应的去饱和区域(图1).此外,梗阻严重程度参数定义为呼吸暂停或低通气持续时间与相应去饱和面积(表2).
为了进行统计学分析,患者根据PVT五个结局变量(表1而且3.).分组后,采用多元二项逻辑回归研究哪些参数与PVT性能受损有关。选择多元二项逻辑回归是因为假设OSA严重指数与PVT不良表现之间的联系是非线性和多变量的,并且因为该方法不需要对PVT结果变量进行任何转换。将表现最差的患者与表现最好的患者进行比较。模型首先根据性别、年龄、身体质量指数(BMI)、爱普沃斯嗜睡量表(ESS)评分、吸烟状况和现有共病(抑郁症、高血压和COPD)进行调整。根据病史或在睡眠诊所的访谈报告抑郁症和所有其他共病的共存情况。对于每个研究参数和调整因素,分别计算属于最差PVT四分位数的β系数的部分最大似然估计。其次,对模型进行TST、AHI、唤醒指数和梗阻持续时间的调整,以检验去饱和严重程度如何独立地影响PVT性能。使用这个经过额外调整的模型有两个原因。首先,通过控制呼吸事件的次数和持续时间,更详细地检验低氧血症假说。 Second, we wanted to avoid the use of predefined limits for OSA severity classes, and rather treat AHI as a continuous variable. After computing the β-coefficients for all models, the coefficients were converted to odds ratios according to the logit-function. As examined parameters differ substantially in the order of magnitude, their values were normalised by the maximum value of each parameter in question before the analyses. However, the normalised 1% increase,如。将产生1.7个事件·h的增加−1去饱和深度的中位数增加了0.29%。因此,参数值进一步缩放到等于10%的相对变化,以实现可比较的和临床更有意义的增加。
结果
最差和最佳PVT四分位数之间的比较
用两种不同的多元逻辑回归模型对每一个被检查的OSA严重程度指标分别进行Q1和Q4的比较。当模型根据人口统计学、主观嗜睡和共病进行调整时,无论是t90%、去饱和严重程度参数、平均去饱和深度或中位去饱和深度显著提高中位RT延长的几率(or 1.17-1.26)。慢速RRT (OR 1.24-1.26) (表4)与平均和中位去饱和深度的增加显著相关。只是t的增加90%(OR 1.18, p=0.04)和中位去饱和深度(OR 1.20, p=0.02)显著提高了发生更多次失误的几率。基于失效,去饱和严重程度参数(p=0.06)和平均去饱和深度(p=0.09)的增加处于显著提高属于Q4的几率的边缘。此外,基于最快的10% RT,中位去饱和深度的增加表明属于Q4的几率显著增加(OR 1.25, p=0.04)。
在对TST、唤醒指数、AHI和梗阻持续时间参数进行额外调整的模型中,所有检查的低氧血症参数的恶化均显著增加了基于失效次数的属于Q4的几率;然而,在平均值下降年代阿宝2(p=0.10)和平均去饱和深度的增加(p=0.12)与其他低氧血症参数相比,没有显著影响中位RT更长的几率(表4).根据RRT,去饱和严重程度参数(OR 1.43, p=0.01)或中位去饱和深度(OR 1.36, p=0.02)的增加显著增加了属于Q4的几率。此外,对最慢的10% RT四分位数的调查显示,梗阻严重程度参数增加(OR 1.39, p=0.04), t90%(OR 1.19, p=0.04)或中位深度(OR 1.27, p=0.02)增加了属于Q4的几率。基于最快的10% rt,没有任何参数与属于Q4的几率显著相关。将Q4与所有其他四分位数进行比较的类似分析结果显示在补充表S1.
人口统计学变量是PVT表现受损的危险因素
当评估人口统计学风险因素、主观嗜睡(ESS)和共病风险时,只有女性、ESS评分较高和年龄较大与PVT表现受损的几率升高显著相关。女性(或范围2.21 ~ 6.02, p<0.01), ESS (OR范围1.05-1.07, p<0.01)是所有PVT结局变量的显著危险因素,而在所有基于RRT、中位RT和失效(OR)的四分位数分析中,年龄的增加是显著的范围1.01 - -1.05, p < 0.05)。BMI、吸烟和抑郁症、COPD或高血压并存与PVT性能受损无关。
讨论
在这项研究中,我们调查了743例OSA患者的常规和新型PSG参数在预测PVT表现中的作用。我们发现,描述间歇性低氧血症严重程度的新参数与PVT性能受损的风险增加显著相关,而传统的OSA严重程度和睡眠碎片性指标(即。AHI, ODI和唤醒指数)则不是。这一发现得到了我们之前研究的支持[7],表明osa相关的客观日间嗜睡与个体低饱和度严重程度的相关性比与呼吸暂停和低通气次数的相关性更强。此外,目前的结果与以往的研究相一致[8,9,18- - - - - -22],通过表明传统的基于ahi的OSA评估与不良PVT表现几乎没有联系。这些发现,连同最近的研究[7,24,29,31,在评估OSA严重程度、症状和日间功能时,更详细地分析PSG记录的临床重要性。由于所提出的新参数是基于常规的PSG人工评分,因此诊所可轻松实施,无需技术或医务人员额外工作[32].
基于我们的结果,夜间间歇性低氧血症的严重程度是PVT表现不佳的psg相关最强指标。在每个亚组分析中,更严重的去饱和导致更长的中位反应时间和更多的失效次数是一致的(表4),并与以往的研究一致[10,18].我们的研究结果表明,较大的去饱和区域和较深的去饱和对OSA患者的警觉性和保持注意力的能力有负面影响。有趣的是,去饱和的持续时间并不是提高PVT性能受损几率的重要因素(表4).已有研究表明,osa相关的间歇性低氧血症可引起神经元脑损伤和与缺血性损伤相似的变化[33].此外,最近的一项研究表明,在健康个体中,全身间歇性低氧血症很容易转化为脑低氧血症,这表明自我调节系统在预防脑血管低氧血症方面有一定的限制[34].我们的研究结果与这些发现相结合,表明去饱和的深度,以及大脑自动调节系统的重复失效,可能会导致OSA患者的认知障碍。
在所有分析中,最高和最显著的优势比是由去饱和严重程度参数、中位去饱和深度和平均去饱和深度引起的。经人口统计调整的模型与经额外调整的模型的比较(表4)表明,当呼吸暂停和低呼吸的数量和持续时间不变时,去饱和深度和面积的增加将提高反应时间延长的几率。先前已有研究表明,AHI值相似的患者外周血氧合反应差异很大[29].这些发现表明,患者在外周氧合下降的速度和再氧合到基线的速度方面存在实质性差异。因此,有必要进一步研究去饱和的形态,以及降低和回收率年代阿宝2以及这些因素与OSA患者心血管结局和日间症状的关系。
正如我们所假设的那样,与AHI或其他常规PSG参数相比,更详细的诊断参数与PVT性能受损有明显更强的联系。与这一假设相反,我们的研究结果表明,呼吸暂停、低呼吸和去饱和的持续时间似乎并不像去饱和的深度那样影响PVT性能。梗阻严重程度参数定义为相应呼吸事件的去饱和面积和持续时间的乘积,而去饱和严重程度与呼吸事件持续时间无关。因此,阻塞严重程度参数的重要性低于去饱和严重程度参数是合理的,因为事件的持续时间是不显著的。值得注意的是,梗阻严重程度是为家庭睡眠呼吸暂停测试而开发的,因此,不可能考虑与觉醒相关的低通气。这对于psg修正梗阻严重程度参数的开发是有说服力的,其中唤醒的严重程度可以用如。唤醒的频率、内容和持续时间与去饱和区域相似。根据两种调整方案对详细低氧血症参数的结果,可以推测警惕性恶化更依赖于呼吸暂停和低通气引起的生理后果,而不是事件的数量或持续时间本身.此外,由于本研究的重点是评估间歇性低氧血症在警惕性失效中的作用,本研究只调查了有限数量的脑电图(EEG)和睡眠碎片化指标。因此,有必要进一步研究详细的脑电图分析及其与PVT表现受损的关系,以更全面地了解警觉性恶化的原因。
本研究基于一个相对较大的、平衡的临床患者样本,其人口统计学、症状和共病很好地反映了一般OSA人群(表1),使所得结果可推广至临床人群。然而,临床和流行病学人群可能包括其他共病性睡眠障碍,如失眠和不宁腿综合征等,这可能会对与PVT结果相关的发现产生令人困惑的影响。此外,目前的结果表明,女性、主观嗜睡和年龄较大以及OSA是PVT表现不佳的显著预测因素。在其他调查阻塞性睡眠呼吸暂停患者和健康个体认知障碍的研究中也报道了类似的发现[9,19,20.,22,35].此外,在我们最近的研究中,我们报道了更大的去饱和区域是客观白天嗜睡和OSA最有害健康后果的重要预测因素[7,29,31].与这些发现一起,本研究强调了迫切需要开发超出AHI的OSA诊断方法。应通过人口统计学信息和更详细的参数来描述OSA的严重程度,从而使诊断更加全面,这些参数与OSA的症状、日间功能以及(例如)心血管合并症更好地相关。为了支持在正常临床工作流程中使用这些新指标的想法,我们已经为RemLogic (Natus Medical, Middleton, WI, USA)发布了一个插件,该插件可以根据睡眠记录的常规手动评分自动计算这些新指标[32].这些指标也可以以类似的方式在其他临床软件中实现。
本研究有一定的局限性。首先,本研究中使用的PVT结果变量是来自120次反应时间系列的标准统计参数。个体在重复反应时间上存在天然差异,因此PVT分析可以从利用完整的时间序列中受益。然而,本研究中使用的标准参数使我们能够与现有文献中关于OSA与PVT结果的联系进行比较。其次,患者在PSG前完成PVT。患有阻塞性睡眠呼吸暂停(OSA)的个体在PSG中的TST往往比正常情况下短[36],这会影响TST的概率。公认TST在很大程度上调节AHI和ODI值;然而,所有新参数也都通过TST归一化。此外,在最近的一项研究中,据报道,个人呼吸暂停、低通气和饱和度下降的严重程度在早晨增加[37].因此,假设均值和最小值是合理的年代阿宝2会减少,并且t90%以及去饱和的平均深度和中位数深度,将随着TST的增加而增加。因此,我们认为PVT的时间不会减少所获得的结果。第三,虽然模型根据合并症进行了调整,但没有PSG和PVT时患者用药的完整记录。精神药物和镇静药物尤其会影响反应时间,从而影响PVT表现,从而在一定程度上影响计算的优势比。第四,这项研究没有纳入健康个体的对照组。然而,本研究的目的是调查哪些是与OSA患者PVT表现受损相关的最重要PSG参数。因此,没有OSA的患者被排除在外,因为他们的警觉性受损与OSA患者相比不是由相同的因素引起的。第五,没有患者的习惯性睡眠数据(如。采用问卷调查、睡眠日记或长期活动记录仪)。睡眠时间短和长期睡眠不足与嗜睡显著相关,因此会影响神经认知表现[38];因此,缺乏这方面的信息是本研究的一个局限性。
总之,我们已经证明,基于特征属性量化去饱和的参数与警惕性受损和维持注意力的能力有显著关联。此外,AHI或ODI的增加不会显著增加PVT性能受损的几率。这些结果强调了开发更详细地评估OSA严重程度和全面分析psg的方法的重要性。这将加强对OSA严重程度的评估,并改善对相关日间症状的风险和严重程度的估计。
补充材料
可共享的PDF
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:J. Töyräs, A. Kulkas, S. Myllymaa, A. Oksenberg和T. Leppänen设计了该项目和分析的主要概念思想。S. Kainulainen, H. Korkalainen和B. Duce进行了数据收集和准备。S. Kainulainen, H. Korkalainen, A. Leino, B. Duce和E.S. Arnardottir进行了分析和解释。S. Kainulainen起草了手稿并准备了图表。所有作者都严格地修改了手稿,批准了提交出版的版本,并同意对工作的各个方面负责。
利益冲突:S. Kainulainen报告了芬兰科学院(资助号313697)、库奥皮奥大学医院集水区研究委员会(项目号5041779和5041768)、坦佩雷大学医院专家责任区的竞争性国家研究资助(资助VTR3221、VTR3228和EVO2089)、Päivikki以及Sakari Sohlberg基金会和肺部疾病研究基金会在进行研究期间的资助。
利益冲突:b,首领没什么可透露的。
利益冲突:H. Korkalainen报告了芬兰科学院(资助号313697),库奥皮奥大学医院集水区研究委员会(项目号5041780和5041767),库奥皮奥地区呼吸基金会,Päivikki和Sakari Sohlberg基金会,肺部疾病研究基金会,芬兰抗结核协会基金会在研究期间的资助。
利益冲突:A.奥克森伯格没有什么可透露的。
利益冲突:A. Leino报告了库奥皮奥大学医院集水区研究委员会(项目号5041776)、Päivikki和Sakari Sohlberg基金会、肺病研究基金会、芬兰文化基金会和库奥皮奥地区呼吸基金会在进行研究期间的资助。
利益冲突:E.S. Arnardottir报告了诺克斯医疗的赠款、个人费用和非经济支持,飞利浦和ResMed的个人费用,在提交的工作之外。
利益冲突:A. Kulkas报告了Seinäjoki中心医院、坦佩雷大学医院专家责任领域竞争性国家研究资助(VTR3221和VTR3228以及坦佩雷结核病基金会)在研究进行期间的资助。
利益冲突:S. Myllymaa在研究期间报告了芬兰科学院(资助号313697)、库奥皮奥大学医院集水区研究委员会(项目号5041770)、保罗基金会和坦佩雷结核病基金会的资助。
利益冲突:J. Töyräs报告了芬兰科学院(决定号313697)、库奥皮奥大学医院(项目号5041767)和芬兰商业(决定号5133/31/2018)在研究期间的资助。
利益冲突:T. Leppänen报告了库奥皮奥大学医院集水区研究委员会的国家研究基金(项目号5041767)、芬兰科学院(决定号313697和323536)、坦佩雷结核病基金会和库奥皮奥地区呼吸基金会在进行研究期间的拨款。
支持声明:在本研究进行期间,获得了库奥皮奥大学医院集水区研究委员会的国家研究基金(项目5041767、5041768、5041770、5041776、5041779和5041780)、芬兰科学院(决定号313697和323536)、Seinäjoki中央医院、坦佩雷大学医院专家责任区的竞争性国家研究基金(资助VTR3221和VTR3228)、商业芬兰(第5133/31/2018号决定)、保罗基金会、Päivikki和Sakari Sohlberg基金会、肺部疾病研究基金会、芬兰文化基金会、坦佩雷结核病基金会、芬兰抗结核病基金会和库奥皮奥地区呼吸基金会。本文的资助信息已存入交叉参考基金注册.
- 收到了2019年9月18日。
- 接受2020年1月17日。
- 版权所有©ERS 2020
本文是开放获取的,并根据创作共用188滚球软件署名非商业许可4.0的条款发布。