摘要
全身硬化(SSC)是一种影响多器官系统的全身自身免疫病,包括肺部。间质肺病(ILD)是SSC中死亡的主要原因。
虽然抗拓扑异构酶I的自身抗体和一些炎症标志物是需要进一步评估的候选生物标志物,但目前还没有有效的生物标志物来预测SSc-ILD的发生。胸部听诊、呼吸急促和肺功能检查是重要的诊断工具,但对发现早期ILD缺乏敏感性。因此,高分辨率计算机断层扫描(HRCT)基线筛查是必要的,以确认SSc-ILD诊断。一旦诊断为SSc-ILD,患者的临床病程是可变的和难以预测的,尽管某些患者特征和生物标志物与疾病进展相关。监测SSc-ILD患者的疾病进展迹象是很重要的,尽管对于使用哪种诊断工具或监测的频率没有共识。在这篇文章中,我们回顾了用于定义和预测SSc-ILD疾病进展的方法。
SSC-ILD疾病进展没有有效的定义,但我们建议从基线≥10%的基线下降,或者与扩散的下降,FVC下降5-9%的FVC下降一氧化碳的肺部容量≥15%表示进展。HRCT成像对ILD的放射线照相程度的增加也将意味着进展。通常用于该定义的1-2岁的时间段,但在较长时间内的下降也可能反映临床相关的疾病进展。
摘要
肺功能测试和胸部成像帮助预测谁具有SSC相关的ILD以及它是否会进展。在没有医生的标准化方法的情况下,我们建议使用肺功能测试和胸部成像的策略。http://bit.ly/2uk9zd2.
介绍
系统性硬化(SSc)是一种系统性自身免疫性疾病,其特征是内皮功能障碍,导致小血管病变、免疫失调、成纤维细胞功能障碍和随后的纤维化;然而,其具体发病机制尚不清楚[1].由于疾病的异质性,SSC代表了医生和患者的主要临床挑战[2].除了损害皮肤外,SSc还可影响多个器官系统,包括肺[3.].临床课程是可变的,但器官表现经常在疾病早期发生[4.].与健康对照组相比,SSc与死亡风险增加250%相关,总的来说,这在过去40年没有显著变化[5.].死亡率主要是由肺部并发症引起的:在迄今进行的最大的观察性研究中,主要死亡原因是间质性肺疾病(ILD;17%),其中肺动脉高压(PAH)占死亡的15% [6.那7.].此外,在一项挪威队列研究中,SSc患者的死亡率与肺纤维化程度相关[8.].
在1972年至2002年期间,由于硬皮病肾脏危机导致的死亡比例从42%下降到SSC相关死亡的42%至6%,可能是由于危险因素,预防,使用血管紧张素转换酶抑制剂来治疗该维度的危险性对疾病的疾病,更大的对MILD SSC案件不太可能发展肾危机的意识。相反,在同一时期,SSC死亡的比例由于ILD增加增加到6%至33%[9.],而在最近的介入研究中,据报道,由ILD引起的呼吸衰竭占死亡的43% [10.].由于ILD导致的死亡比例的增加可能会反映其他死亡原因的减少。总体10年生存从1972年至2002年的54%提高到66%[9.].
根据皮肤纤维化程度,SSc患者通常分为有限皮肤(lcSSc)和弥漫性皮肤(dcSSc)亚群[11.那12.].肺受累可发生在这两种疾病的亚群中,它可影响呼吸道的所有方面,包括实质、血管和肌肉组织[8.那13.].ILD是SSC中的早期并发症,在一些患者(〜4%)SSC的第一个临床症状与ILD直接相关[2那14].大多数发展为严重限制性肺病的患者是在SSc症状出现后的头5年发生的[2].
尽管SSC相关的ILD(SSC-ILD)与发病率和死亡率之间建立的关系,但仍然没有对ILD的筛查达成共识,也没有疾病进展监测。这个问题因缺乏验证的生物标志物而缺乏SSC-ILD和缺乏临床建议,以通知诊断SSC-ILD的患者的方法和时间,并确定进展风险的患者[15].
在这个透视片中,我们总结了目前对SSC患者患者患者的疾病发病机制和危险因素的理解,讨论筛选,早期检测进展的危险因素,并提出了监测疾病进展的指导和对这用于治疗SSC-ILD。
SSC-ILD的发病机制
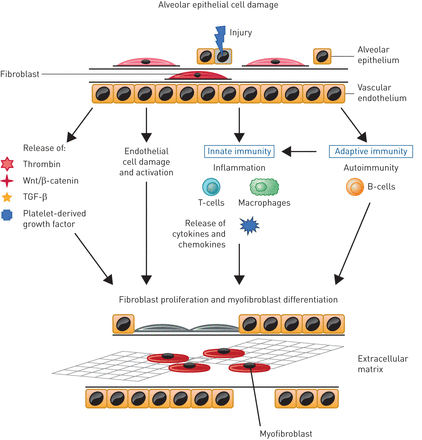
SSC可能会影响多个器官和系统,最具不可逆的损伤,可归因于渐进式纤维化[2那16].基于迄今为止的研究,先天性和自适应免疫,内皮功能障碍,小血管异常,炎症和纤维化之间存在复杂相互作用[17].涉及SSC-ILD的关键路径总结在图1.SSc-ILD发病最常见的启动因子是肺泡上皮细胞和血管内皮细胞的损伤,炎症途径导致促纤维化刺激,诱导肺成纤维细胞分化为肌成纤维细胞表型[6.那18].纤维化是由于异常愈合过程与骨髓、周细胞、上皮细胞和内皮细胞等来源的间充质细胞的异常扩张,以及固有成纤维细胞向肌成纤维细胞分化所致[16那18].转化生长因子-β被认为在SSc-ILD纤维化的发展和进展中发挥核心作用[6.那16[血小板衍生的生长因子,WNT-β-catenin和刺猬信号还驱动纤维化[18那19].SSc成纤维细胞已被证明对细胞因子(如干扰素-γ)的纤维化抑制潜能更有抵抗力[20.].此外,SSC-ILD的患者可以增加促炎细胞因子的水平,例如白细胞介素(IL)-8,IL-6,肿瘤坏死因子-α和巨噬细胞炎症蛋白-1α中的支气管肺泡灌洗(BAL)流体和血清[21-23].此外,已被假设可以涉及B细胞,因为SSC-ILD更常见的患者用抗拓扑异构酶I抗体和抗细纤维细胞抗体存在[24].抗成纤维细胞抗体的功能作用尚不明确,但它们可能通过与成纤维细胞结合,增加胶原蛋白的分解和基质金属蛋白酶-1的产生,直接影响细胞外基质重塑[25].这些细胞因子的释放增加,生长因子和生物活性蛋白有助于纤维化过程的刺激的自我延续循环[16那18].对潜在机制的更大理解可以鉴定可用于筛查风险患者的生物标志物,并促进目标和个性化治疗的发展。例如,高循环的混合M1(经典活化)/ m 2(或者活化)单核细胞/巨噬细胞百分比与ILL有关,表明需要研究其可能的作用作为生物标志物或用于SSC肺参与的病原体元素[26].
风险因素存在于ILD
SSC中ILD普遍性的估计因ILD如何定义而异;使用高分辨率计算断层扫描(HRCT),估计率为47-84%。在加拿大硬皮病研究小组注册处,65%的患者在HRCT扫描上有ILD的证据,26%通过体检鉴定,22%通过胸部射线照相鉴定[27].在一项挪威队列研究中,50%的患者HRCT诊断为ILD [8.].依赖肺功能测试(预测的强迫肺活量(FVC) %或至少一项肺功能测试(PFT)的下降),导致对ILD患病率的估计较低[28].在尸检中,74%的SSc患者发现间质纤维化[29].
许多患者特征与SSC中发育ILD的风险较高有关(表1).在EUSTAR (euular硬皮病试验和研究)数据库中,ILD在dcSSc(53.4%)中比lcSSc(34.7%)更常见[30.].此外,性和种族似乎是ILD发展的重要决定因素。尽管SSC(女性:男性比例4.7:1)报告的雌性优势强劲,但SSC的男性比具有SSC的雌性更容易发生,相对风险1.24; 95%CI 1.01-1.52)[31那32].在普遍医疗保健系统的环境中进行了一个大型多民族观测研究,发现与欧洲血统患者相比,患有SSC的非洲加勒比血症患者更频繁地具有ILD(31%与53%;p = 0.007)[33].
SSC-ILD的发展的危险因素还包括抗拓扑异构酶I阳性,降低FVC和肺部的肺部延长用于一氧化碳(D.LCO)[34]但虽然FVC和D.LCO变化可能是由ILD引起的,并且在发病之前不存在。多变量分析表明,与DCSSC的抗拓甲异构酶I阳性更密切地与DCSSC相比更密切与LCSSC [30.].
许多研究也支持SSc中胃食管反流与ILD的相关性,如Christmann等.[35].
ILD的诊断和筛查
SSC-ILD的最常见的初始症状是嗜好的呼吸困难和干咳,但早期SSC-ILD可以相对无症状[6.].随着肺参与可能影响呼吸道的所有方面,当患有SSC的患者患有呼吸困难症状时,差异诊断可能相当宽泛,可包括PAH,脱墨,慢性贫血[13.[左心中参与减少或保存的射血分数。
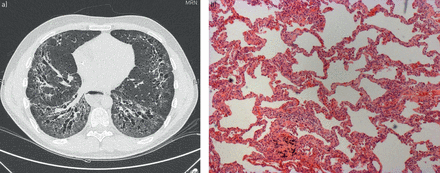
使用HRCT诊断SSC-ILD以检测实质肺病[36].典型的非特异性间质性肺炎(NSIP)在HRCT上表现为双侧磨玻璃影、网状和牵引性支气管扩张,最突出的是下叶(图2A)[36].一般而言,HRCT表现可区分NSIP和通常的间质性肺炎(UIP)模式[37].虽然肺活检极少用于诊断SSc-ILD,但如果进行活检,间质纤维化伴颞部均匀性和轻度炎症细胞浸润(IE。纤维化NSIP)通常可视化(图2B.).在少数病例中,观察到细胞NSIP或UIP [13.].虽然计算断层扫描(CT)扫描是诊断所必需的,但它们将患者暴露于辐射[38].减少剂量的HRCT协议可以可靠地检测SSC-ILD,比全胸部HRCT更低的辐射曝光[38那39].虽然这些减少剂量的方案在一些中心已经成为常规,但还需要在更大的队列中进一步验证。
a)来自系统性硬化(SSc)相关间质性肺疾病患者的高分辨率计算机断层扫描(疾病范围>20%);b) SSc患者的肺组织学表现为非特异性间质性肺炎。
SSc-ILD患者的pft通常表现为限制性通气缺损,FVC和/或总肺容量下降,1秒内强迫呼气量(FEV)保留1), FEV正常或增加1/FVC比率,以及单次呼吸减少D.LCO[6.].值得注意的是,尽管HRCT对结构肺病的明确证据表明,患有早期SSC-ILD的患者可能已经保存了肺量[28那40],并减少D.LCO.两项研究发现,>60% HRCT诊断的SSc和ILD患者肺功能正常[28那40].因此,虽然pft是SSc-ILD诊断的重要组成部分,但它们不够敏感,不能可靠地检测早期ILD [28那40那41].在SSc诊断后的前5年定期进行pft(至少每年一次)可能有助于检测指示ILD的肺功能变化。
目前,当SSC-ILD变得临床显着并且指示治疗时,没有广泛接受的共识。
挑战诊断
与SSC-ILD的诊断有很多挑战。一个潜在的诊断障碍是在SSC的初级护理中缺乏意识,这可能导致推荐[42].在建立SSc- ild诊断过程中,临床专科的参与程度也存在差异,而且缺乏正式指定的SSc专科中心[42].
早期发现ILD
有必要对患者进行早期系统筛查,以确定肺部并发症,尽管在筛查和随访中对应使用哪些检测缺乏共识[2那42].在一项研究中,使用HRCT诊断SSC的ILD筛查,鉴定了35%的受试者,其中51%的受试者,其受试者有限(1-20%纤维化)和13%的受试者,涉及涉及> 20%的受试者> 20%肺 [43].
CT扫描检测到的亚临床间质性肺异常(ILAs)为早期发现ILD提供了一种可能的方法[44那45].ilas已经在类风湿性关节炎相关的ILD中进行了研究,其中它们与咳嗽和呼吸困难增加以及PFT结果下降相关[46];然而,很少有证据表明他们在SSc-ILD。一项早期SSc-ILD的研究表明,毛玻璃不透明后来发展为NSIP模式[47].
未来的SSC-ILD诊断和筛查方向
未来,肺超声可能与其他方法结合筛查ILD [48-51].正电子发射断层扫描的临床前研究表明,ILD疾病过程组分的靶向核成像(如整联蛋白αvβ3和生长抑素受体2)可以与ILD的筛选和评估中的其他方法集成[52那53].然而,这种方法受到与该技术相关的高水平辐射照射的限制。
另一种帮助识别ILD患者的另一种潜在方法是钉子录像机(NVC)。NVC是一种安全验证的工具,NVC模式与不同的SSC临床并发症相关[54那55].在287例SSC患者中测试了NVC,以评估它是否可以改善心肺患者的高风险患者的检测。在该分析中,NVC模式与ILD和心脏/肺参与的存在有关,与特定的抗萃取核抗原抗体无关[56].这可能表明微血管病变是器官受累的重要原因。在未来,NVC可能与其他参数一起被纳入高性能算法中,用于早期检测SSc肺受累性[57].
然而,尽管发现了SSc患者发生ILD的危险因素,以及更新的技术可能有助于识别发生ILD风险增加的亚群体,但目前除了CT外,没有任何技术能够以适当的敏感性和特异性检测ILD。因此,胸部CT仍是筛查和诊断SSc-ILD的金标准。
ILD进展的危险因素
一旦ILD被诊断为SSC患者,重要的是要确定哪些患者可能正在进行,因为SSC-ILD的自然历史是可变的。有些患者经历肺功能丧失的损失,其他患者进展缓慢或表现出稳定的疾病[58那59].
目前,没有生物标志物预测跨多个临床队列的SSC-ILD过程[60].初步报道BAL细胞数量可预测死亡率、免疫抑制治疗获益、进展或无进展生存[61那62尚未在更大规模的队列研究中得到证实[63].然而,有几种策略可以帮助识别有发展和进展SSc- ild风险的患者,这些策略应被视为治疗SSc患者的第一步(表2).
在临床实践中,SSc-ILD的严重程度可根据“Goh标准”进行分级,根据HRCT(明显<20%或明显>20%),患者有“局限性”或“广泛”疾病,在不确定病例中使用FVC阈值为70% [41].基线HRCT范围与FVC % pred下降相关[64在最近的一项研究中,广泛疾病(>20%)与恶化或死亡增加三倍相关[65].
基于证据的预测模型,结合外围毛细管氧饱和度(S.宝2)和关节炎史(SPAR)已被研究用于预测轻度ILD的进展[66].在215例SSC和温和的患者中,降低S.宝26分钟步行试验后,任何时间点存在关节炎是ILD进展的独立预测因子(定义为FVC≥15%,或FVC≥10%联合D.LCO随访1年≥15%)[66].通过组合两个预测因子,衍生的SPAR模型能够将预测率从25.5%提高至91.7%,最终可使患者的风险分层,轻度SSC-ILD [66].
已经确定了许多用于SSC-ILD疾病进展的危险因素。大型SSC-ILD队列研究证明FVC(危险比(HR)0.97; P = 0.0009),D.LCO(HR 0.97;p=0.0004)和年龄增加(HR 1.03;P =0.04)与性别、体重指数、吸烟状况、血清学、疾病亚型和免疫抑制剂使用等因素校正后的死亡率显著相关[67].最近的一个分析表明,FVC或下降D.LCO超过2年是一个比基线FVC更好的死亡率预测因素D.LCO[10.].
对DNA改性酶拓扑异构酶I的自身抗体经常存在于DCSSC的患者中,并且可能与SSC-ILD的更快进展相关[34那68那69].由于趋化因子受体CXCR3和CXCR4在纤维化中的致病作用,已经研究了SSC的患者对它们的自身抗体[70].抗cxcr3和抗cxcr4抗体水平在SSc亚组中与健康受试者相比存在差异,弥漫性SSc患者中最高。SSc-ILD患者的抗体水平高于无ILD者;而肺功能恶化(FVC <70% pred)患者的抗cxcr3 /4抗体水平较病情稳定者低[70].但是,这些生物标志物不是常规可用的。
我们对几种炎症标志物进行了研究。血清趋化因子配体18升高预测FVC下降[71那72]是SSC-ILD死亡或进展的危险因素[72-74].基线C反应蛋白水平预测SSC-ILD的长期进展,较高的水平与较短的存活相关[75]和pft的下降[76].Krebs Von Den Lungen(KL)-6和表面活性剂蛋白-D是主要在肺部表达的蛋白质,与肺部损伤,纤维化和炎症有关[72那77].血清KL-6水平呈负相关D.LCO%pred和升高的水平与终级肺病相关,更快的FVC下降[72那77-79],即使在存在免疫抑制的情况下[80].需要进一步的研究来验证这些生物标志物。
监测疾病进展
SSc-ILD疾病进展的可变率意味着在SSc诊断为ILD后对患者进行适当监测是很重要的,尽管目前对疾病进展没有确定的定义。一系列症状测量(如。呼吸困难,咳嗽和/或疲劳的外观或加重),体检和PFT在常规诊所访问时评估疾病进展非常重要[6.那21],最近的研究强调PFT变化对死亡率的影响[10.那81].
此外,患者报告的结果可能对测量疾病进展很重要;在ILD患者中,较低的肺活量与St George’s Respiratory Questionnaire (SGRQ)评分恶化之间存在关联,SGRQ是一种呼吸相关健康状况的测量方法[82].应注意,本研究主要评估了特发性肺纤维化,过敏肺炎和NSIP的患者;SSC中的SGRQ分数可能受到同血症的影响,包括肌肉骨骼问题。
仍然有关使用重复的HRCT的突出问题,包括如何经常进行(例如,每年或每隔一年)的频率,以及PFT或其他工具是否应用于监控,仅在必要时使用HRCT(如。意外恶化或怀疑感染)[38那83].此外,对于在第一次检查时,在患有SSC的患者中,CT扫描是否应重复何种辩论。
SSc-ILD专家小组
欧洲和北美的国际小组国际专家组专家组被组装讨论该领域的发展。面板椅子选择兴趣的主题,并以团体讨论。所选脉管和风湿病学家确定了SSC-ILD作为未满足的面积的预测因素。我们审查了SSC-ILD临床进程的证据,审查了诊断所涉及的挑战,并为SSC-ILD患者的分期和风险分层提供了指导。
我们支持单个患者疾病进展的定义,作为肺功能的持续变化,其特征在于≥10%的基线的FVC下降,或与A相关联的FVC下降5-9%D.LCO下降≥15% (图3)[81].如果串行CTS在HRCT成像上显示ILD的程度,则也将考虑到这一点。此定义是进展最常用的定义之一,尽管它尚未在SSC-ILD中正式验证。研究人员通常使用这一定义,时间为1年,但没有关于如何在较长时间内定义疾病进展的协议。它应该承认FVC和/或D.LCO在较长一段时间内的观察仍然显示出潜在的临床相关疾病进展,尽管速度较慢。
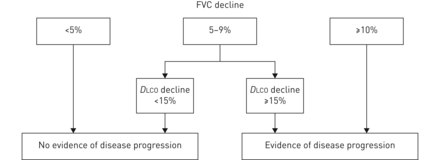
疾病进展的建议定义。FVC:强迫肺活量;D.LCO:肺对一氧化碳的扩散能力。
无干预时,肺功能的年自然损失为15-25 mL(由[84])。肺功能的昼夜变异性为8-9%,临床试验中的测量误差是~1%[85].在最坏的情况下,这增加了10%。因此,对于FVC的相对5-9%的损失,我们同意应该伴随着下降D.LCO确认疾病进展
对治疗的影响
在最近发表的Nintedanib治疗系统性硬化(SENSCIS)的安全性和有效性试验中,接受Nintedanib治疗的SSc-ILD患者的年FVC下降率低于接受安慰剂的患者(治疗差异41 mL) [86].基于这些数据,尼丁尼布最近被美国食品和药物管理局批准,减缓了SSC-ILD患者肺功能下降率[87].2017年欧洲抗风湿病联盟(European League Against Rheumatism)和EUSTAR集团发布的指南建议考虑对SSc- ild患者进行量身定制的环磷酰胺(CYC)治疗,并在选定的快速进展SSc患者中使用造血干细胞移植[88].遵循硬皮病肺部研究(SLS)II试验[10.],倡导与霉酚酸酯MOFETIL(MMF)进行第一线治疗SSC-ILD的Delphi共识处理算法。二线治疗包括Cyc或Rituximab作为感应治疗,其次是MMF作为维护治疗[89].
但是,目前没有关于治疗开始或升级的共识[90].大多数SSc专家利用他们的临床经验,并考虑SSc- ild进展的危险因素,以决定何时在逐个病例的基础上开始治疗[91].更好地识别进展风险最大的患者将有助于识别哪些患者能从早期治疗中获益最大[6.].有明确需要新的治疗方法。随着我们对SSC-ILD的发病机制的理解,希望将引入特定疗法,以治疗受影响的器官系统,改善患者阱,功能和生存[92-95].瞄准自我蠕虫纤维化可能会在未来提供治疗选择[16]但虽然它仍然未知是否在修饰疾病进展和预防不可逆的肺部损伤方面是有益的。在不久的将来,希望疾病的分子检测将为SSC患者提供免疫调节治疗[96].
结论
通过提高医生对SSc-ILD相关的频率、进展和死亡率的认识,有可能改善患者的预后。更好地识别哪些患者有进展的风险也将是有益的。ILD是SSc的早期并发症,有必要对患者进行早期和系统的筛查,以便在疾病进展高风险的受试者肺功能恶化之前进行治疗。肺功能检查仍是一项重要的诊断工具,但在SSc诊断后可能需要定期进行检查,以发现提示ILD的变化。作为包括肺功能检测在内的更广泛临床检查的一部分,HRCT基线筛查对于确认SSc-ILD诊断是必要的。我们倾向于将疾病进展定义为肺功能的持续改变,其特征是肺活量从基线下降≥10%,或与a相关的肺活量下降5-9%D.LCO下降≥15%。FVC或D.LCO即使只在12个月内观察到它,也应该被视为疾病进展。患者报告的成果工具专注于呼吸困难和成像可以提供有价值的支持信息。未来,希望新的成像技术和诊断和预测生物标志物将在定义SSC-ILD进展方面发挥越来越重要的作用。
可分享的PDF.
确认
编辑,编辑支持和格式援助是由核心全球的汤姆普利德尔和克莱尔Scofield提供,由Boehringer Ingelheim International GmbH合同和资助。Boehringer Ingelheim International GmbH有机会审查医疗和科学准确性以及知识产权考虑的稿件。
脚注
作者贡献:作者根据医学期刊编辑国际委员会建议符合作者的标准。188bet手机版188bet手机版他们对稿件有关的范围,方向,内容和编辑决策的全部责任参与了所有发展阶段,并批准了提交的稿件。作者收到了与稿件的发展有关的赔偿。Boehringer Ingelheim International GmbH支持国际专家委员会会议。
利益冲突:O. Distler报告在研究进行期间,勃林格咨询公司的个人费用;来自Actelion的讲座拨款和个人费用,来自AbbVie的顾问委员会工作的个人费用,来自Acceleron Pharma、Anamar、Amgen、Catenion、CSL Behring、ChemomAb、Ergonex、GSK、Inventiva、Italfarmaco、iQvia、Medac、礼来、赛诺菲、Target BioScience、UCB、Baecon Discovery、Blade Therapeutics、Curzion制药和Glenmark制药、赠款和个人费用咨询和讲座从拜耳和勃林格殷格翰的发言,个人费用从iQone讲座,Menarini, Mepha和诺华,个人费用从起到咨询和讲座,并和罗氏,赠款和个人费用从三菱咨询公司,咨询和讲座的个人费用和辉瑞非金融(旅行)支持,在提交的工作之外;已发布专利US8247389、EP2331143。
利益冲突:S. assassi在研究期间报告了Boehringer Ingelheim的非财务(书面)支持;来自Biegen Idec和Bayer,Beehringer Ingelheim的授权和个人费用在提交的工作之外。
利益冲突:V. Cottin报告了咨询委员会工作和讲座和非金融(旅行)支持的个人费用,咨询,咨询委员会工作和讲座的非财务(旅行)支持,以及Boehringer Ingelheim和Roche,咨询委员会工作和数据监测委员会的个人费用来自拜耳/ MSD和加拉帕戈斯,数据监测委员会的个人费用从Gilead,Celgene和Galecto工作,咨询委员会的个人费用和诺特里斯的讲座,讲座的个人费用Sanofi,指导委员会工作和数据监测委员会的个人费用来自ProMEDIOR,在提交的工作之外。
兴趣冲突:M. Cutolo报告来自Cantelion,Boehringer Ingelheim,Horizo n,BMS和Celgene的赠款,在提交的工作之外。
利益冲突:S.K.在研究期间,Danentch / Roche和Bristol Myers Squibb的赠款和个人费用来自Boehringer Ingelheim,Genentech / Roche和Bristol Myers Squibb的个人费用,在研究期间,Galapagos和Galectic的个人费用。
利益冲突:C.P. Denton报告了Actelion、拜耳、赛诺菲、勃林格殷格翰和Corbus的个人费用,以及葛兰素史克、Inventiva、CSL Behring和领先生物科学在进行研究期间的拨款和个人费用。
利益冲突:J.H.W.Distler报告了Boehringer Ingelheim的发言和咨询委员会工作的个人费用。
利益冲突:a.m.。Hoffmann-Vold报告了勃林格殷格翰在研究进行期间提供的非财政支持;勃林格殷格翰(Boehringer Ingelheim)的拨款、个人费用和非经济支持、Actelion的个人费用和非经济支持、罗氏(Roche)的个人费用。
利益冲突:S.R. Johnson报告了勃林格殷格翰(Boehringer Ingelheim)、Corbus、拜耳、罗氏(Roche)和加拿大卫生研究院(Canadian Institutes of Health Research)在提交工作之外的拨款。
利益冲突:U.MüllerLadner向提交的工作之外向Boehringer Ingelheim提供咨询委员会工作和讲座的个人费用。
兴趣冲突:V.史密斯在研究期间向Boehringer Ingelheim报告了发言者费用;来自Boehringer Ingelheim的Grants,Contelion Pharmaceuticals Ltd,Bayer AG,Hoffman-La Roche AG,Galapagos NV和Sanofi,外部的研究资金。
利益冲突:E.R. Volkmann报告了勃林格殷格翰(Boehringer Ingelheim)在提交作品之外的个人费用。
利益冲突:下午Maher从GSK和Astrazeneca报道赠款和个人费用,从UCB,Boehringer Ingelheim,Roche,拜耳,普通,苏比,加拉帕戈斯,Celgene,Indalo,Planiant,Blade Therapeutics,Arthivent,诺华和布里斯托尔 - 迈尔斯Squibb,Apellis的股票期权,在提交的工作之外。
支持声明:S.R. Johnson被授予加拿大卫生研究所新研究员奖;由关节炎研究基金会的奥斯卡和埃莉诺·马科维茨硬皮病研究基金支持。V. Smith是弗兰德斯(比利时)研究基金会(FWO) (1.8.029.15N)的高级临床研究员。FWO没有参与研究设计、数据收集、分析和解释、报告的撰写,也没有参与决定将文章提交出版。T.M. Maher是由国家健康研究临床医生科学家协会(NIHR参考:CS-2013-13-017)支持的,也是英国肺基金会呼吸研究主席(C17-3)。勃林格殷格翰国际有限公司签约并资助了写作、编辑支持和格式协助。本文的资金信息已存入Crossref资助者注册表.
- 已收到2019年10月15日。
- 公认2020年2月9日。
- 版权©2020人队
此版本在Creative Commons归因非商业许可证4.0的条款下分发。