抽象
促使大流行的新型疗法急需的冠状病毒病2019(COVID-19)的严重呼吸后果。基于细胞的方法,主要是使用间充质干(基质)细胞(MSCs),已经证明,在急性呼吸窘迫综合征(ARDS)的安全性和有效性可能,尽管他们还没有很好的呼吸道病毒引起的急性呼吸窘迫综合征的研究。有限的临床前数据表明,全身MSC管理可以显著减少呼吸道病毒(流感病毒株H5N1和H9N2)引起的肺损伤;但是,也有在冠状病毒呼吸道感染的模型没有可用的数据。
有一个快速增长的数量COVID-19的基于细胞的治疗方法临床研究的。这些利用了各种不同的细胞来源,剂量,给药的策略和目标患者群体。为了提供一个合理的策略,最大限度潜在治疗用途,这是非常重要的,了解相关的临床前研究和呼吸道病毒引起的肺损伤MSC行动的假设机制。本文综述了这些,并考虑目前临床调查的一起。
抽象
当务之急是要更好地理解基本原理和基本数据,在呼吸道病毒感染MSC的支持,也有人反驳有效性,并确定目标患者群和潜在的细胞治疗COVID-19方法https://bit.ly/2VbmYXs
介绍
该冠状病毒病2019(COVID-19)的流行,对原产于中国武汉,迅速和持续全球范围内传播,并可能导致严重的呼吸显著发病率和死亡率[1]。负责代理,严重急性呼吸综合征冠状病毒2(SARS-CoV的-2),是的有包膜RNA病毒冠状病毒病毒家族。人对人通过飞沫或污染的表面[发生传输1]。Ťhe average incubation period is 5 days, but ranges from 1 to 14 days. Most patients present with mild respiratory tract infection, most commonly characterised by fever (82%) and cough (81%). Severe pneumonia and acute respiratory distress syndrome (ARDS) have been described in 14% of the reported cases, and the overall mortality is around 2% [2]。然而,这些数字演变为大流行蔓延,并取决于所涉及的国家。
谁开发ARDS需要插管和机械通气,休克和多器官功能衰竭也可以发展,但是这是否是病毒感染的直接后果,或因重大疾病的并发症COVID-19的患者,目前尚不清楚。目前的治疗方法包括大规模的标准的支持护理和治疗其他合并感染。抗病毒药物,包括remdesivir,洛匹那韦,利托那韦,洛匹那韦或-利托那韦和干扰素(IFN)-β1,正在研究,但是安全性和潜在功效仍有待确定。Remdesivir和IFN-β1β似乎有优越的抗病毒活性,洛匹那韦和remdesivir体外中东呼吸综合征(MERS)冠状病毒,但是这是否是要确定用于SARS-CoV的-2遗体的情况下[2]。美国食品和药物管理局(FDA)近日批准使用羟氯喹的COVID-19例,但效果仍有待确定。增长的信息还表明在肺中的是病毒诱导的细胞因子风暴可驱动严重发病机制和提供潜在的治疗靶标,例如抗白介素(IL)-6或抗IL-1的方法[3]。
最近,越来越多的基于细胞疗法的临床研究,主要涉及骨髓间充质干细胞(基质)细胞(MSCs),而且利用MSC衍生的条件培养基或细胞外囊泡和其他几种类型的细胞,在中国已经启动了COVID的-19呼吸系统疾病。由于这些涵盖范围广泛的方法和目标患者群,就必须更好地了解和研究,对呼吸道病毒感染MSC行动的潜在机制的基本原理。在呼吸道病毒感染和MSC管理的有关相关的临床研究中ARDS患者的机型最近的临床前数据有助于对他们来说,潜在的基于MSC的细胞治疗方法可能会被认为是患者群体的更加清晰。
在呼吸道病毒引起的肺损伤MSC行动的可能机制
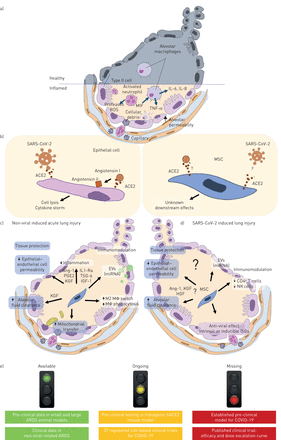
全身给药后,大部分的MSCs在肺血管床通过提出与毛细血管内皮细胞尚不清楚相互作用。Ťracking studies using labelled MSCs demonstrate that most are cleared within 24–48 h, although there can be longer persistence in injured or inflamed lungs [4]。的清除机制仍然被阐明,但通过居民炎性和免疫细胞,尤其是巨噬细胞[包括凋亡和随后的胞葬作用和吞噬作用五]。骨髓间充质干细胞驻留在肺部时,能够释放多种可溶性介质,包括抗炎细胞因子[6],抗微生物肽[7],血管生成生长因子和胞外囊泡[8(图1)。从MSCs向呼吸道上皮细胞和免疫细胞[线粒体的直接细胞 - 细胞传递10]也已经被描述[11]。
在呼吸的肺损伤的间充质干细胞(基质)细胞(MSC)的潜在的治疗作用是由不同的机制介导的,包括但不限于分泌的旁分泌因子,细胞外囊泡(电动汽车),以及可能的线粒体传递,促进组织保护,免疫调节和可能的病毒抵抗性。一个)健康的齿槽(顶部)和发炎/肺泡水肿(底部)和涉及急性呼吸窘迫综合征(ARDS)发病机制的示意图。b)中严重急性呼吸综合征冠状病毒的示意图2(SARS-CoV的-2)感染肺上皮细胞,随后裂解和细胞因子风暴(左),和潜在的MSC感染SARS-CoV的-2的,具有未知下游后果(对)。c)部分,通过它的MSC改善非病毒急性肺损伤已知机制。从L-改编阿菲和Matthay[9]。d)对机制的限制信息,通过该间充质干可能改善SARS-CoV的-2的肺损害的基础上,在流感病毒感染的模型有限的临床前数据。E)当前状态的最先进的在冠状病2019(COVID-19),基于临床前和临床研究的基于细胞的疗法。MIF:巨噬细胞迁移抑制因子;TNF:肿瘤坏死因子;IL:白细胞介素;ROS:活性氧;ACE2:血管紧张素转化酶2;的Ang-1:血管生成素1;PGE2:前列腺素E2; KGF: keratinocyte growth factor; IL1-Ra: IL-1 receptor antagonist; TSG-6: TNF-stimulated gene 6; IGF-1: insulin-like growth factor 1; miRNAs: microRNAs; MΦ: macrophage; M2 MΦ: macrophage type 2; HGF: hepatocyte growth factor; NK cells: natural killer cells; ISGs: interferon-stimulated genes; hACE2: human ACE2.
越来越多的文献证明,抗炎症介质释放的模式是特异于所遇到的炎性肺环境,并通过上表面MSC表达损害是与病原体相关的分子病原体受体的差动活化介导[12]。这包括Toll样受体(TLR),其是由病毒RNA激活(如。TLR3)(如在COVID-19)和病毒非甲基化CpG-DNA(如。TLR9),导致导致MSC活化下游细胞信号传导途径[13]。MSC分泌的血管生成素-1(ANG-1)和角质形成细胞生长因子(KGF)有助于肺泡 - 毛细血管屏障恢复破坏,如ARDS发病的一部分[14,而细胞外囊泡中的特异性抑制microRNAs也被描述为介导间充质干细胞在细菌或非感染性急性肺损伤临床前模型中的保护作用[15]。
然而,改善呼吸道病毒所致肺损伤的介质尚不清楚。在动物模型中,流感H9N2病毒感染增加血清和肺趋化因子负责肺白细胞浸润,包括集落刺激因子(gm - csf)、单核细胞化学引诱物蛋白1 (MCP-1)、巨噬细胞炎性蛋白1α(MIP-1α)等,由静脉明显减少msc(管理16]。IFN-γ水平的增加,与其它促炎性细胞因子,提示MSC活化,包括抗炎介质的释放典型的抗病毒免疫应答,单独或一起。这种干扰素的免疫调节作用“牌”的重要性已在移植模型先前证实与宿主病(GVHD),其中IFN-γ的MSC治疗的接受者- / -t细胞移植物对细胞治疗没有反应,演变成致命的移植物抗宿主病[17]。从COVID-19例患者在意大利未发表的数据表明,高水平的IFN-γ被发现,从而可能影响全身给药的MSC(马西莫Dominici,摩德纳大学医院和雷焦艾米利亚,意大利摩德纳;个人通信)。然而,“行货”的MSCs也可以抑制同种抗原诱导T细胞功能体外,可能损害所需的疾病控制抗病毒应答。例如,间充质干抑制响应于流感特异性的T细胞的活化淋巴细胞增殖体外[18]。脐带衍生的MSC(UC-MSC的)也已显示出抑制特异性T细胞的针对H1N1流感病毒细胞毒性体外[19],也许导致长期感染收件人。这是相反的报告,其中,例如,巨细胞病毒的型号(CMV)感染,间充质干会对同种抗原和病毒特异性T细胞保留的能力,增殖,产生IFN-γ和杀死巨细胞病毒感染的细胞的不同影响体外[20]。
有待解决的一个重要的问题在呼吸道病毒感染防护MSC行动是否直接与病毒性感染,抗病毒t细胞可能通过刺激行动,或者他们是否将整体抗炎行动已经证明在其他急性肺损伤模型9]。后者可以是用于细胞因子风暴特别相关,这是可能的动作的组合将负责。
在MSC行动的呼吸道病毒影响
相比,他们的分化后代的MSC一般对病毒感染抗性[21]。这部分反映IFN刺激基因(ISG)的固有表达该抢先病毒感染[21]。MSC ISG表达包括,除其他外,IFITM家族蛋白,IFI6,ISG15,SAT1,PMAIP1,P21 / CDKN1A和CCL2。其中抗病毒蛋白,因为它们防止感染之前病毒能够穿过细胞的脂质双层的IFITM家庭成员是唯一的。这些活动由许多病毒,包括登革病毒,埃博拉病毒,A型流感病毒和严重急性呼吸综合征(SARS)冠状病毒[限制感染培养的细胞22]。MSC中最高度表达的ISG中的一个(P21 / CDKN1A)的沉默的易感性特别提高到基孔肯雅病毒(CHIKV),而IFITM3击倒由多种病毒呈现的MSC易受感染,包括黄热病病毒和寨卡病毒[21]。
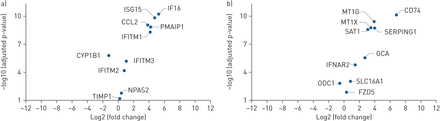
通过定量逆转录PCR [使用RNA测序(GEO数据集GSE97987)和验证21],我们建立了人类胚胎干细胞源性MSC组成型表达的ISG名单。的在下面的人MSC固有的ISG(3骨髓来源的MSC(BM-MSC的),一个UC-MSC和一个脂肪组织源性MSC的不同促炎症细胞因子的刺激五个独立GEO数据库的表达改变生物信息学分析(AD-的MSC),与相应的数据集GEO GSE68610,GSE77814,GSE46019,GSE46019和GSE18662;图2)的研究表明,IFN- wt等促炎细胞因子诱导的非组成性ISGs包括MT1X、MT1G、SERPING1、SAT1、IFNAR2和CD74,同时显著增加了组成性抗病毒基因IFI6、ISG15、CCL2、SAT1、PMAIP1和IFITM1的表达。
干扰素刺激的基因的基因表达(的ISG)的人骨髓间充质干(基质)细胞(BM-MSC的)与促炎细胞因子(白介素1β,肿瘤坏死因子α和活化的代表性火山图分析干扰素(IFN)-γ),与控制,在GEO数据集GSE68610。的基因表达分析)组成,和b)非组成的ISG。ISG15:泛素样蛋白;CCL2:C-C基序趋化因子2;IFI6:IFN-α诱导蛋白6;PMAIP1:佛波醇-12-肉豆蔻酸酯-13-乙酸酯诱导的蛋白1;IFITM:IFN诱导的跨膜蛋白;CYP1B1:细胞色素P450 1B1;NPAS2:神经元PAS蛋白2结构域的;TIMP-1:金属蛋白酶抑制剂1; MT1G/MT1X: metallothionein 1G/X; SERPING1: serpin family G member 1 (plasma protease C1 inhibitor); SAT1: sulfate anion transporter 1; GCA: grancalcin; IFNAR2: IFN-α/β receptor 2; SLC16A1: monocarboxylate transporter 1; ODC1: ornithine decarboxylase 1; FZD-5: Frizzled-5.
因此,在呼吸道病毒感染的上下文中,包括COVID-19,的MSC可以呈现两种不同的抗病毒机制:组成性水平升高MSC-特定ISG的以功能作为抗病毒保护的介质,以及IFN的次级反应,导致ISG的诱导和广泛的病毒抗性。相反,间充质干可提出内在和诱导抗病毒先天防御可能导致治疗效果COVID-19在患者的混合。
相反,一些文献表明,人类的BM-MSC是宽容的禽流感A(H5N1)感染,失去活力和免疫调节活性[16]。这可能发生的未感染的MSC的快速暴露[23],和病毒感染的MSC可以因而不会在停止病毒复制和肺部炎症[功能上有效的24-27]。的BM-MSC上表达它们的细胞表面流感病毒的α-2,3和α-2,6唾液酸受体和可以同时支持禽类H1N1和H9N5的流感病毒株的复制[24,25]。一世nfluenza-infected MSCs undergo cell lysis apoptosis within 18 h post exposure, with corresponding production of pro-inflammatory cytokines and chemokines [24]潜在颠覆它们的保护免疫调节性质[26]。呼吸道合胞病毒也能传染的MSCs,修改免疫细胞增殖及活性[27]。因此,取决于病毒的类型和表达或表达病毒受体的MSCs的百分比的水平,MSC可以得到,如果注入与正在进行的呼吸道病毒感染的患者感染。这将如何影响潜在的有利影响仍有待确定。
做的MSCs表达ACE2,SARS-COV-2的功能性受体?
血管紧张素转化酶2(ACE2)已被报道是SARS-CoV的-2条目中的主宿主细胞受体,和病毒利用宿主细胞丝氨酸蛋白酶TMPRSS2为S蛋白启动[28]。ACE2在呼吸道上皮细胞中高度表达,从而起到在病毒进入了至关重要的作用向这些细胞[29]。ACE2最近也被证明是鼻上皮细胞中的ISG [三十]。因此,SARS-CoV的-2可以利用ACE2的IFN-驱动上调,肺损伤中的关键组织保护介体,以增强感染。相反地,ACE2报道通过降解纤维化肽血管紧张素II [以防止非病毒肺损伤31]。体内ACE2的基因沉默增强了在小鼠中博来霉素诱导的肺胶原沉积,而纯化的ACE2的全身给药抑制纤维化反应[32]。鼠BM-MSC的过表达ACE2基因,下面的慢病毒载体转导,对内毒素诱发的肺损伤提供额外的抗炎和内皮保护作用在小鼠中33,34]。然而,也有可能是一个缺点,如果这种表达ACE2导致感染并在随后的MSCs有害影响。作为基因表达的水平是SARS-CoV的-2传递的一个关键因素[28],它是相关的,以评估任何来源的间充质干是否组成性或诱导表达ACE2或TMPRSS2。
临床前证据:在呼吸道病毒相关的急性肺损伤的MSCs
有大量文献证明在临床前模型中的呼吸系统疾病的,包括细菌或细菌产物(内毒素)或其他手段[诱导那些涉及急性肺损伤全身性或直接气管内施用MSC的功效的35]。该模型包括啮齿动物和大型动物(猪牛羊),以及移植的人体肺部。的途径和方法范围已被用于剂量,正在研究给药和MSC来源,从骨髓,脂肪组织,脐带,脐带血和胎盘的MSC。最近的一项系统评价表明,BM-MSC和UC-MSC的在临床前急性肺损伤模型降低死亡率[比AD-MSC的更有效36]。
然而,只有临床前研究调查呼吸道病毒感染的临床前模型MSC管理的影响的一个小数目。这些都被进一步限制到流感病毒,已经产生矛盾的结果,并没有尚未直接涉及冠状病毒呼吸道感染(表格1)。值得注意的是,前两次研究发现的MSCs不被对小鼠流感呼吸道感染的保护。darwish等。[37]评估单个全身给药的任一同源的鼠BM-MSC或异种人的BM-MSC上由小鼠适应性H1N1或猪源H1N1流感引起的肺损伤的免疫活性小鼠的影响。两种不同剂量的MSC(2.5×10五或5×10五 cells·mouse-1)在病毒施用后不同时间点给药(天-2,0,2和5感染后(p.i.时))。Using survival and different measures of lung inflammation as outcome end-points on day 7 p.i., neither syngeneic nor xenogeneic MSC administration, either alone or as an adjuvant therapy with oseltamivir, was effective either when administered prophylactically prior to virus inoculation, or when therapeutically administered. Similarly, Gotts等。[38]评估人类和小鼠的MSCs(5×10的全身和气管内给药的效果五 cells·mouse-1),施用两个剂量,无论是前面(2和3天注射后)或更高(天5和6注射后),在免疫活性小鼠的小鼠适应性H1N1引起的肺损伤。然而,MSC不提高流感介导的肺损伤,不管给药途径。
相比之下,最近的研究表明,全身MSC给药对流感呼吸道感染的啮齿动物和猪模型具有保护作用。C韩等。[39]研究发现,通过体外测定法,该间充质干通过释放可溶性介质即上调钠和氯转运改善由H5N1和H7N9的流感病毒诱导的失调肺泡液体清除和蛋白渗透性,部分。5全身给药×10五每只小鼠的人BM-MSC的一天感染后5一世n immunocompetent mice aged 8–12 months infected with influenza A (H5N1) reduced virus-induced mortality (until day 18 p.i.), weight loss (days 6–10 p.i.), lung oedema (day 7 p.i.), bronchoalveolar lavage fluid (BALF) CD4+Ť-cells and natural killer (NK) cells (day 7 p.i.), lung histopathological lesions (day 18 p.i.), and pro-inflammatory cytokines and chemokines (day 7 p.i.), without reducing lung virus titres (days 7 and 10 p.i.). They further found that Ang-1 and KGF released by MSCs were important, but not enough to attenuate the effects of viral infection on alveolar fluid clearance and permeability. However, in young mice (aged 6–8 weeks), no effects were observed in mortality and body weight loss. Thus, the data suggest that systemic MSC administration may provide benefit in older patients who are at higher risk for severe pulmonary illness caused by H5N1. Why this was less effective in younger mice is not clear at present.
大号一世等。[16]调查了低剂量的影响(10五 cells·mouse-1禽流感病毒(H9N2)诱导免疫小鼠肺损伤的小鼠BM-MSCs的研究。第3天,一次静脉注射。,to reduction in mortality, lung oedema and histological injury, as well as in BALF and serum chemokines and cytokines, and to improved gas exchange and levels of anti-inflammatory mediators, although it did not reduce lung virus titration when administered either 30 min or 24 h after infection induction. Differences between early and later administration of MSCs were only observed in some BALF and serum inflammatory mediators. Only early administration reduced BALF levels of GM-CSF, reduced BALF and serum monokine induced by IFN-γ (MIG), IL-1α and IFN-γ, and increased levels of BALF and serum IL-10. Both early and later administration led to reduction of BALF and serum IL-6 and tumour necrosis factor-α. This might reflect that early administration seems more geared towards prevention of cell infection and inflammation, rather than dealing with more clinically relevant sequelae of epithelial infection. Avian influenza virus infection can trigger a very intense pro-inflammatory response compared to other influenza viruses; thus, L一世等。[16]推测,有益的影响可能是不同的致病性特征的具体结果,相比于猪源H1N1病毒感染。
大号OY等。[41]发现UC-MSC的比人类的BM-MSC更有效的在恢复受损的肺泡液体清除和渗透性,在体外气道上皮细胞模型。这些作用被部分地穿过的的Ang-1和肝细胞生长因子分泌MSC介导的。UC-MSC的作者随后相比给予的BM-MSC(5×10五 cells·mouse-1,day 5 p.i.) in experimental lung injury induced by influenza A (H5N1) infection in female immunocompetent mice aged 6–8 weeks. Despite failure to reduce virus titre and increase survival rate, a single dose of UC-MSCs decreased body weight loss (days 16 and 17 p.i.), lung oedema (days 10 and 14 p.i.) and inflammation (day 7 p.i.) in H5N1-induced lung injury.
MSC衍生的细胞外囊泡已经被证明有类似的结果,并且在某些情况下比的MSC本身在一定范围的临床前肺损伤模型[改善炎症和损伤更有效42,43]。ķhatri等。[40]found that systemic administration of extracellular vesicles isolated from pig BM-MSCs was safe and reduced virus shedding in nasal swabs, influenza replication in the lungs, BALF pro-inflammatory cytokines and chemokines, and histopathological changes, when administered 12 h after viral inoculation in a mixed swine (H3N2, H1N1) and avian (H9N5, H7N2) influenza-induced pig lung injury model. These findings suggest systemic extracellular vesicle administration as a potential cell-free strategy for use in respiratory virus-induced lung injuries.
有还无的临床前研究的数据管理MSC的影响冠状病毒呼吸道感染的车型,主要是由于缺乏一个建立的动物模型。SARS-COV-2在一些非人类的灵长类动物和小鼠的近交系鼻内感染中观察到的复制,但这些模型没有显示肺部疾病的临床症状在人类[可见44]。转基因小鼠人ACE2,感染SARS-CoV的-2,在肺中表现出病毒的复制,以及间质性肺炎与淋巴细胞和单核细胞浸润到在肺泡空间巨噬细胞[肺泡间质和积累45]。虽然这种模式需要进一步评估,这可能有助于治疗包括COVID-19细胞疗法的测试。最近,SARS-COV-2的非人灵长类动物模型能够反映相同的临床症状,在人体观察到病毒复制和病理,与死亡率相当的水平,并可能进行进一步评估一个有价值的模型[46]。
总体而言,目前还不清楚不同的结果是否反映每种方法的不同功能,包括在主机(年龄)不同,相应的MSCs(来源,数量,给药途径),并在病毒特异性炎症模式。由病毒,特别是禽流感病毒,施用的MSC的感染可以解释一些观察到的缺乏有效性体内研究,但他们的给药后MSC感染体内尚未调查。为了绕过病毒对MSCs的影响,外囊可能是进一步研究的选项。很明显,进一步的临床前研究必须做评估的MSCs由冠状病毒的infectiveness和MSCS的冠状病毒引起的肺损伤模型的影响。
MSC管理的临床研究患者的冠状病毒或其它呼吸道病毒引起的肺损伤
尽管最近暗示流感呼吸道病毒性肺部感染的临床前模型MSC管理的潜在效力的证据,有限的发表的临床数据可用。最近发表的单中心的开放标签试验从佑安医院在北京(中国)调查给予BM-MSCs向7例COVID-19的肺炎具有不同的严重程度,其中包括1例危重严重的疾病,需要照顾的重症监护单元(ICU)[47]。所述的MSC,剂量为10作为单次静脉内给药6 cells·kg-1body weight in 100 mL saline at various times after initial symptomatic presentation. The MSCs were assessed by RNA sequencing for expression of ACE2 or TMPRSS2 prior to administration and each was found to be minimally expressed (in one out of 12 500 cells and seven out of 12 500 cells, respectively), although the RNA sequencing results were not validated for gene (quantitative reverse transcription PCR) or protein expression.
7名患者被归类为严重严重(N = 1),重度(N = 4)和普通型(n = 2)。另外三个病人列为严重的接受安慰剂(车辆)管理进行比较。Patients were followed for 14 days after MSC or placebo administration and a range of safety and efficacy end-points were assessed. No infusional toxicities, allergic reactions, secondary infections or severe attributable adverse events were observed, and patients, including the one categorised as critically severe, apparently demonstrated clinical improvements within 2–4 days after MSC administration. However, while detailed information is provided for the critically severe patient, there is a lack of corresponding information for the other six patients or for the three placebo patients. Analyses of viral titres, circulating pro- and anti-inflammatory mediators, and lymphocyte numbers and populations were presented in detail for the critically severe patient and to a lesser degree for the other patients.
更详细的信息,以纳入和排除标准,给药相对于疾病,合并症,每个患者的临床过程的发作MSC的定时,和炎症介质的评价和细胞群两个治疗组和安慰剂的患者都需要更好地确定潜在MSC功效和作用机制。重要的是,没有讨论是否接近在只有极为严重和/或严重的患者或用于更广泛的范围COVID-19呼吸道感染的临床表现的进一步研究。
在中国[2013 - 2014年爆发期间的第二个最近发表的研究评估MSC管理患者的H7N9流感病毒呼吸道感染48]。在这项研究中,17名危重患者H7N9引起的ARDS接收经血衍生的单元的多个静脉内给药(106从单个健康供体获得的结果和在勃每输注细胞)进行比较,以44名同等危重患者接受标准的抗病毒和支持疗法。所述治疗的患者中,三个被描述为早期感染期间接收三个分开的输注,六名患者接受三次输注在晚期感染和八个患者接受4个输注在晚期感染。然而,关于输注之间或是否所接收的控制患者车辆输注的定时被提供的任何信息。的MSC治疗和对照患者否则相当良好匹配为合并症和度多器官衰竭和用于使用其它支持疗法,除了休克的MSC治疗组中发生率较高(P <0.03)。没有明显的静脉滴注毒性或严重不良事件指出。三名患者的MSC治疗组中死亡(82.4%存活),而对照24死亡(45.5%存活)。但是,没有具体细节提供的死亡,包括原因和相关要么注入或整体临床病程时间,或其他标准的评估,包括呼吸机的天,ICU住院或住院时间上。全血计数和肾,肝,心脏,和凝血功能的措施是可比较的,除了在对照组中更高的循环亲降钙素水平,可能暗示仲或共细菌感染,虽然提供了关于其它感染没有信息。作者的结论是MSC管理是H7N9引起的急性呼吸窘迫综合征,而这可能是潜在的适用COVID-19在患者使用一种可行的方法。
这两项研究,同时暗示,凸显了一些问题,相对于潜在用途的冠状病毒和其他病毒性呼吸道感染的MSCs。这些包括但不限于的MSC,剂量和给药策略,包括给药的次数和时间源。这些研究还强调与呼吸系统疾病,包括那些在危重患者的临床试验的行为问题。对入选和排除标准,病程,合并症,合并感染和实验室评价,包括调查评估机制的全部信息,必须以全面的方式来提供。
正在进行的基于细胞的临床试验评估COVID-19爆发期间注册
在本次审查的时间,基于细胞的临床研究的数量,探讨细胞治疗SARS-COV-2感染的健康(NIH)ClinicalTrials.gov数据库的美国国立卫生研究院自1月下旬2020注册患者的治疗潜力和中国临床试验注册中心(www.chictr.org.cn),也从世界卫生组织国际临床试验注册平台(WHO-ICTRP),已经达到了27项,共约1287名被认为入学(访问表2)。有三种主要的干预:的MSC(N = 17; 781例患者),MSC衍生物(条件培养基或细胞外囊泡; N = 4; 176例患者),或其它细胞来源(N = 6; 330例)。调查的一般常见的功能包括:1)全身给药,联合或随后由推荐常规支持治疗严重或临界SARS-CoV的-2感染[49]。2) age range 18–80 years with no sex restrictions; 3) follow-up for at least 3 months; and 4) clinical samples collected will be throat secretions and/or blood. For the MSC investigations, 10 out of 17 will utilise UC-MSCs, one out of 17 will utilise menstrual blood-origin MSCs, and six out of 17 do not disclose the MSC tissue source. Notably, no apparent MSCs of bone marrow origin are being utilised, despite the majority of pre-clinical investigations for non-viral-induced acute lung injuries having utilised BM-MSCs. There is little clarification of use of cryopreserved与连续培养细胞[五]。只有六个16的公开预期的细胞注射的剂量,其中只有四个与患者体重相关。在静脉内给药的范围内变化0.4之间和42×106 cells·kg-1。相比较而言,MSC的最高剂量在非病毒ARDS在已发表的文献用于临床试验为10×106 cells·kg-1(START试验)50]。给药策略为单剂量至五剂量,平均频率为每2天。
试验的四个将利用任一MSC衍生的条件培养基或细胞外囊泡。这两种提议MSC衍生的细胞外囊泡,从AD-MSC的一个,对于其中不存在临床前支持数据的气溶胶吸入。六次调查将利用其它细胞,包括脐带血来源的单核细胞,细胞毒性T细胞,树突细胞,NK细胞,脐带血干细胞和细胞因子诱导的杀伤细胞,其中只有后者的调查描述给药和注射的频率。作为最好的,我们可以确定,有支持的理由对任何这些方法没有明显的临床前数据。
对于考虑呼吸道病毒感染的细胞为基础的方法中的伦理问题
传染病暴发,包括临床试验期间的医疗保健提供者和研究人员的活动,目的是为了争取找到的感染患者的治疗快速,有效的反应。这些动作需要在适当的道德准则发生。世界卫生组织有一个嵌入集成全球警报和反应系统中的伦理方法和注意事项传染病及其它突发公共卫生事件[指南51]。这些都是适用于基于细胞的临床研究,包括保证,这些都是科学有效的和潜在的风险是相对于预期收益合理。随着危重病人,包括那些与其他病因导致ARDS对于MSC管理的安全性,无显著问题已经在发表的文章中描述的最新[51]。相对于功效,目前并平衡力,因为只有一个尚未MSC施用未发表的探索性试验表明有益的结果[52]。
此外,还必须使临床调查以透明的方式,根据用于严重疾病潜在新疗法的临床研究[既定先例进行53]。这包括公认的端点,包括但不限于总死亡率,ICU和住院和机械通气天的长度。我们还大力提倡使用临床样品,如适当的临床护理部分所获得的或用于监测下面的单元格管理的不良事件,以获得机械的信息,包括但不限于循环支持和反对炎症介质和炎性细胞群的分析。鉴于COVID-19蔓延和细胞治疗研究的越来越多的快速性,一个中央协调中心,以加快全等试验设计和相应的数据发布将是显著的好处。
进一步显著的问题是COVID-19的患者人群为目标,以及何时启动MSC管理。危重病人需要支持性措施,包括气管插管,机械通气ARDS是一个合乎逻辑的人口目标。赞赏有治疗方法在这个人口正在考虑其他潜在的,它似乎合理的目标,这些患者尽快下面气管插管,机械通气。参数也可以与目前公认的危险因素,如年龄增加,糖尿病和/或心血管疾病,谁在临床恶化的风险潜在的更高的目标严重感染的患者做。在这种情况下,在临床和实验室指示,诸如氧合水平新出现的数据,在氧合的变化和在升高的全身细胞因子风暴的指标,可以是用于发起MSC管理标准。由于这些指标是不断发展的,我们主张在考虑时要考虑的MSC使用旷达的方法。无论是中度或轻度疾病的患者应临床研究仍不明朗的一部分。可用的临床前数据和临床试验,非病毒性急性呼吸窘迫综合征最好的支持潜在使用的安全性数据。由于这是为时过早是否会出现在COVID-19 ARDS幸存者任何下游呼吸效应,这似乎是一个不那么紧迫的人口目标。同样,针对恢复轻度或中度影响病人计数器作为对肺未知下游的影响也似乎是一个不那么紧迫的考虑。 Overall, to date there has been a limited understanding of the pathogenesis of COVID-19, which currently hinders the development of an optimal study design.
是否利用遗传修饰的MSCs目前还不清楚。这部分反映了当前的缺乏了解哪个动作,即分泌介体通过的MSC组成性或诱导产生的,可能是最有效的SARS-CoV的-2呼吸道感染。这也反映了目前缺乏明确的证据,以任何其他潜在的治疗剂是否有证明有效,例如IL-6或IL-1受体拮抗剂,所述的MSC可被工程化以产生。因为目前的治疗研究发展,这可能迅速改变,涉及这些代理等。此外,由于转基因细胞产品需要更长时间的监管部门的批准,这可能不是选择的策略,以面对当前的爆发。
挑战和前景
COVID-19呼吸道感染的全球大流行已经促使新疗法的迫切需要。临床和基础科学调查人员需要通过促进和坚持严格设计的调查逻辑基于现有的临床前数据带头。关于在临床前的呼吸系统疾病损伤模型MSC管理和肺损伤模型MSC行动的潜在机制目前了解的有限的可用数据可以是谨慎,谨慎使用,以支持合理设计并进行临床研究。然而,更多的临床前数据是必要的,特别是在冠状病毒引起的肺损伤的模型。虽然同情使用未经验证的基于MSC的疗法可以在不同的情况下可以考虑,我们敦促,只要有可能,这发生在临床研究的大背景下。由于本次审查的原始写作,许多基于MSC-调查的学术界和工业界赞助的试验已经开始在全球范围内除了这里回顾了中国的人。我们敦促所有这些坚持理性和合理设计调查的最高标准。只有在这些方面可以为潜在的治疗用细胞疗法的合理的证据为基础的平台上进行开发。
我们还必须采取对干细胞临床行业,它已经开始提供未经证实的疗法COVID-19强大的立场。国际社会为细胞和基因治疗,国际社会为干细胞研究等一批专业和科学组织已经在这方面采取领导职务[54-56]。滥用的可能性很高,鉴于COVID-19大流行,并擅自使用未经证实的疗法的走投无路的情况下是一个明显的危险。
可共享PDF
致谢
我们承认莫妮卡Kurte(安第斯大学,圣地亚哥,智利),用于执行对GEO数据库的生物信息学分析。
脚注
利益冲突:M.扈利在研究进行期间报告从CONICYT(FONDEF 2016年,IT16I10084),补助金;助学金从细胞中的细胞接受,提交作品之外;具有WO2014135924A1未决,WO2017064670A2未决,WO2017064672A1未决和WO / 2019/051623申请中的专利;并为细胞的细胞CSO,一个大学分拆开发骨关节炎,牙髓炎和心脏衰竭,并Regenero,智利再生医学(公共和私人资金),用于皮肤溃疡和狼疮财团疗法。
利益冲突:J.昆卡在研究进行期间报告从CONICYT(FONDEF 2016年,IT16I10084),补助金;助学金从细胞中的细胞接受,提交作品之外;并且是为细胞细胞研究科学家,大学分拆开发治疗骨关节炎,牙髓炎和心脏衰竭,并Regenero,智利再生医学(公共和私人资金)的财团,为皮肤溃疡和狼疮。
利益冲突:F,F克鲁兹没有透露。
Conflict of interest: F.E. Figueroa has a patent WO/2019/051623 pending and is a board member of Cells for Cells, as the director of the programme of translational cell therapy at Universidad de los Andes, the academic institution that originated the Consorcio Corfo Regenero and the Cells for Cells biotechnological spin-off.
利益冲突:罗科没有什么可透露的。
利益冲突:D.J.魏斯从NIH,囊性纤维化基金会和美国国防部,外界提交的工作报告补助。
支持声明:该作品部分被从通讯社国立InvestigaciónŸDESARROLLO,ANID,原名CONICYT补助(FONDEF 2016年,IT16I10084)的支持。本文资金的信息已交存交叉引用出资者注册。
- 收到2020年3月25日。
- 公认2020年4月3日。
- 版权所有©ERS 2020
该版本采用知识共享署名非商业许可证4.0的条款分发。