摘要
COVID-19的高细胞动力学免疫失调被称为细胞因子风暴综合征。白细胞介素-6水平≥80 pg·mL−1预测呼吸衰竭和死亡的风险增加,免疫调节治疗是一个紧急调查领域。https://bit.ly/3jq3uJ4
介绍
2019年冠状病毒病(COVID-19)相关细胞因子风暴综合征(COVID-CSS)的概念出现在严重急性呼吸综合征冠状病毒2(SARS-CoV-2)大流行的早期,以解释为什么一些接触该病毒的患者会患上严重急性呼吸窘迫综合征、多器官衰竭和死亡。来自中国武汉的一项开创性研究报告称,与病情较轻的患者相比,需要重症监护的患者血清中炎性细胞因子浓度较高,作者推测“细胞因子风暴与疾病严重程度相关”[1].COVID-19高细胞运动血症最初被拿来与其他导致免疫反应失调的呼吸道病毒感染,即严重急性呼吸综合征(SARS)和中东呼吸综合征(MERS)进行比较。随后,COVID-CSS与其他细胞因子风暴综合征(如噬血细胞淋巴组织细胞增多症(HLH))之间的相似性[2]、自身炎症综合征和嵌合抗原- t细胞治疗细胞因子释放综合征(CAR - T-cell therapy cytokine release syndrome, CAR - T-cell CRS)变得明显[3.- - - - - -5].在一些COVID-19患者中,高细胞运动血症是病理性的主张促使了大量免疫调节和细胞因子抑制剂治疗的临床试验。然而,批评人士认为,在COVID-19中,CSS是一个误导的概念框架,两篇著名的社论对COVID-19 -CSS提出了严重的质疑[6,7]简言之,这些作者主张:
细胞因子风暴综合征没有定义;
中位IL-6水平在新冠病毒-19中相对较低;
COVID-19应以低炎症性血管病变而不是高炎症性细胞运动综合征为特征;
因此,免疫调节疗法可能在COVID-19的治疗中发挥很小或没有作用。
在这篇社论中,我们讨论了这些争议,并证明细胞因子风暴综合征可能在COVID-19导致的严重呼吸衰竭和死亡中发挥重要作用。
细胞因子风暴综合征的定义
新冠病毒CSS概念的批评者声称“细胞因子风暴没有定义”[6而且“没有证据表明COVID患者会出现细胞因子风暴”[7]事实上,专家将细胞因子风暴综合征定义为[8]:
以淋巴细胞和巨噬细胞持续活化为特征的免疫失调;
导致大量细胞因子的分泌;
导致严重的全身炎症和多器官衰竭,死亡率高。
CSS一词最初是用来描述移植物中的高细胞激肽血症与异基因干细胞移植后的宿主病[9].最近,CAR - t细胞CRS的IL-6水平显著升高,经常超过1000 pg·mL−1(正常<7 pg·mL−1),并对IL-6的阻断有反应,已被列入CSS的总称[3.].许多病毒、细菌和寄生虫感染都能导致CSS。传染性病原体如eb病毒(EBV)和结核分枝杆菌在遗传性和获得性免疫缺陷患者中,引起病理性免疫激活,其特征是细胞因子和细胞因子受体,如干扰素-γ (IFN-γ)和可溶性IL-2受体(sIL-2r)显著升高,导致HLH临床综合征[10,11].
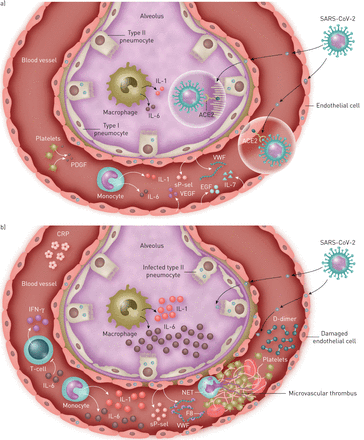
详细的免疫学研究明确表明,部分重症COVID-19患者确实符合细胞因子风暴综合征的一般标准,这与其他传染性CSS不同。最近一项纵向研究对中度与严重COVID-19在重症患者中显示了“免疫失火”的三个明显特征[5].中度疾病患者(存活且无需重症监护病房(ICU)入院的患者)炎症细胞因子表达较低,组织修复性生长因子(如表皮生长因子、血小板衍生生长因子和血管内皮生长因子)增加(图1一个)相比之下,重症患者(死亡或需要ICU入院的患者)的促炎细胞因子(包括IL-1α、IL-1β、IL-6、IL-18和TNF-α)高度升高(图1 b) [5]另一项研究发现,虽然细菌脓毒症诱导的免疫麻痹以单核细胞缺乏和不能产生细胞因子为特征,但在严重的新冠病毒-19中,外周血单个核细胞在LPS刺激下表现出持续的TNF-α和IL-6产生体外IL-6和c反应蛋白(CRP)浓度显著升高体内[4]。与其他呼吸道病毒(如SARS-CoV-1、MERS-CoV、人副流感病毒和呼吸道合胞病毒)相比,SARS-CoV-2中的转录过度炎症反应具有独特的不平衡性,IFN-I和-III水平较低,伴有炎症趋化因子和细胞因子(IL-1、IL-6)的高表达以及严重的淋巴细胞减少,导致“高促炎症、低天然抗病毒防御”状态[12].
新型严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)在一些患者中导致轻病,在另一些患者中导致严重疾病的机制示意图。在这两种情况下,病毒都会进入人体细胞通过血管紧张素转换酶2 (ACE2)是一种广泛表达于II型肺细胞、巨噬细胞、内皮细胞和其他肺细胞的跨膜受体[24,25].a)轻度疾病(凝血病和血栓发生率低,住院时间短,危重症和死亡率低):这些患者血清炎症因子水平低,组织修复生长因子水平高,如表皮生长因子(EGF)、血小板衍生生长因子(PDGF)和白介素(IL)-7 [5].血管内皮生长因子。b)严重疾病(微、大血管血栓形成发生率高、住院时间长、危重症高、死亡率高):其中许多患者出现细胞因子风暴,伴有高血清炎症因子(如IL-6、IL-1、IFN-γ)和内皮激活标志物,如von Willebrand因子(vWF)、因子8凝血剂(F8)和可溶性p -选择素(sP-sel),导致内皮炎和微血管血栓形成[5,15,27].IL-6显著升高导致淋巴细胞减少和免疫麻痹,免疫麻痹可通过IL-6阻断部分恢复[4,32].NET:中性粒细胞细胞外陷阱;CRP: c反应蛋白。
虽然COVID-CSS还没有标准的诊断标准,但这一术语通常用于指表现出过度免疫激活的患者子集,其特征是炎症标志物(如CRP、IL-6和铁蛋白)显著升高,以及淋巴细胞减少和一系列末端器官损伤,从孤立的呼吸功能障碍到多器官衰竭。IL-6的临床测量目前还不广泛,但对许多临床实验室来说是一种相对简单和廉价的分析方法。在我们中心的COVID-19早期,当IL-6被用于研究目的而不是临床护理时,我们对COVID-CSS采用了以下标准:1)需要机械通气的COVID-19肺炎;2)发热(最高体温>38°C);3) CRP >100 mg·L−1;4)血清铁蛋白峰值>1000 μg·L−1[13].符合这些标准的患者研究血清IL-6水平显著升高:中位数为91 pg·mL−1,四分位间距(IQR)54–696 pg·mL−1(n = 15)。然而,IL-6并不总是与CRP(由肝细胞在对IL-6反应时产生)或铁蛋白(巨噬细胞活性的标志)相对应[14].最近,至少有两项大型研究表明,血清IL-6在预测呼吸衰竭和死亡等临床结局方面优于CRP、铁蛋白、肝酶等简单临床实验室指标,其最佳临界值分别为80和86 pg·L−1分别为(15,16]综上所述,这些数据表明IL-6阈值≥80 pg·mL−1在COVID-CSS的未来定义中具有预后价值。最终,多变量预后模型纳入简单、广泛可用的参数,如外周血氧饱和度(年代阿宝2)/吸入氧含量(FIO2)、中性粒细胞/淋巴细胞比率、CRP和铁蛋白,以及细胞因子/趋化因子,如IL-1、IL-6、IFN-γ诱导蛋白(IP)-10和IL-10,可能导致预后评分系统,而不是HLH采用的二元“是/否”诊断模型[16,17].
白细胞介素- 6和COVID-CSS
在COVID-19早期研究中报告的血清IL-6适度升高被引用为反对CSS在该疾病中的相关性的论据[6,7]。例如,中位数(7-45 pg·mL−1)和血清IL-6水平的IQR在四项针对轻至重COVID-19患者的大型研究中相对较低[6].然而,中位数和IQR是集中趋势的估计,在细胞因子风暴中,感兴趣的人群位于患者的前四分之一。此外,这些研究中细胞因子分析的时间异质性可能忽略了一些患者细胞因子水平的快速增加。重要的是,细胞因子风暴并不适用于大多数表现出a生理对特定暴露的反应,但对少数人的痛苦病理免疫激活或功能障碍。我们可以做一些类比,暴露于EBV的患者中只有很小的比例会发展成HLH,而接受CAR - t细胞治疗的患者中不到15%的人会发展成需要IL-6阻断的3-4级严重CRS。同样,暴露于COVID-19的人群中,一小部分但高度相关的人会发展成CSS。
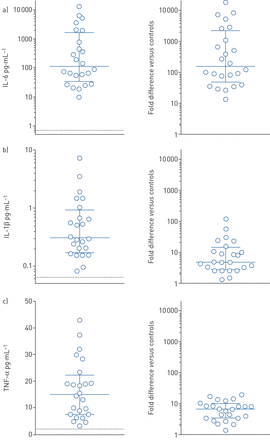
在COVID-CSS中,许多炎性细胞因子,如IL-1、IL-10和TNF-α,比正常值升高约2-100倍,而IL-6的升高幅度更大,在某些情况下,比正常值高出1000倍以上。图2图中显示了24例重症COVID-19患者IL-1β、IL-6和TNF-α的炎症因子水平,包括绝对值和高于正常值的“fold elevation”。其他几项大型研究也报道了血清IL-6水平在100-10 000 pg·mL显著升高−1严重疾病患者的范围[12,15,17,18]这些显著升高的白介素-6水平与严重的CAR T细胞CRS相似[19,高于其他IL-6高综合征,如多中心Castleman病,IL-6水平升高,但通常<100 pg·mL−1[3.,20].HLH据说包含多种“具有共同终末途径但有不同致病根源的高铁贫血高炎症综合征”[21]类似地,在COVID-CSS中,免疫失调的不同“根”特征越来越可能导致共同的末端炎症途径,其特征是IL-6显著升高、严重T细胞淋巴细胞减少和呼吸衰竭[4,5,17].
高细胞运动血症、血管病变和内皮炎
一些作者提出,与中度升高的IL-6水平相比,D-二聚体水平显著升高,微血管和大血管血栓形成率较高,这意味着新冠病毒-19的病理生理后遗症与低炎症性血管病变有关,而不是与炎性细胞因子有关[7].受体血管紧张素转换酶2 (ACE2)在病毒细胞进入和复杂的血管变化(包括尸检研究中看到的肠套纳血管生成和弥漫内皮膜破坏)中的中心作用,确实支持covid -19相关发病率中血管病变的中心作用[22]然而,最近的研究表明,高细胞激肽血症和血管病变不是一个非此即彼的命题。肺血管系统是新冠病毒-19血管内凝血和血栓并发症的关键部位[23,24].早期对SARS-CoV刺突(S)蛋白和ACE2的研究表明,S蛋白与ACE2结合导致炎症细胞因子的产生,包括IL-1和IL-6 [25,26].
这种高炎症反应导致内皮屏障破坏和高凝。弥漫性闭塞肺血管床微循环可引起肺动脉高压、死腔通气增加,最终导致右心衰竭。血清内皮因子,如可溶性血栓调节蛋白、可溶性p -选择素和von Willebrand因子在急性呼吸窘迫综合征的疾病进展中起主要作用[27].综上所述,这些发现建议了一个模型,在该模型中,COVID-19最好被视为一种炎症性内皮炎,肺细胞、内皮细胞和上皮细胞产生炎症细胞因子,并对血管系统和周围组织产生免疫介导的损伤[25,27) (图1 b).
新冠病毒-19中的细胞因子、呼吸衰竭和免疫调节治疗
CSS的批评者认为,COVID-19中出现的高细胞活性血症可能是病毒清除的必要生理反应,并警告在这种情况下使用免疫调节疗法[6,7]在更为成熟的CSS中,特定细胞因子的中心作用不仅通过将细胞因子升高与特征性器官损伤联系起来的研究来确定,而且还通过临床试验证明细胞因子阻断可带来临床益处。原发性HLH可能是该模型的范例,因为IFN-γ/CXCL-9轴是该疾病病理生理学的中心[28],用emapalumab阻断该轴产生深度和持续的缓解[29].同样,IL-1已被证明在自身炎症综合征和继发性HLH中发挥了类似的作用,用anakinra或canakinumab进行阻断可获得临床益处[30,31].
白细胞介素-6导致新冠肺炎患者免疫失调和呼吸衰竭的证据正在迅速积累。血清白细胞介素-6升高与淋巴细胞减少、淋巴细胞毒性受损和内皮细胞活化有关(图1 b)这些免疫缺陷可通过用托昔单抗阻断IL-6治疗部分恢复[4,32].德国一项研究显示IL-6 >为80 pg·mL−1结合CRP>97 mg·L−1高度预示呼吸衰竭[15].在我们的研究中心,IL-6被发现与动脉氧张力的比值呈负相关FIO2及静态肺顺应性[33].此外,从一个大的前瞻性队列(n=501)生成的多变量模型显示,早期全身炎症预测死亡率。在入院时测量的15个变量中,CRP的临界值为87.5 mg·L−1是最敏感的(0.97),IL-6的临界值为86 pg·mL−1是预测死亡最具体的(0.89)[16].
RECOVERY试验显示每日6mg地塞米松治疗的死亡率受益,特别是在重症患者中,是第一个明确显示免疫调节治疗受益的随机对照试验(RCT) [34]尽管许多细胞因子阻断的回顾性研究(如anakinra和tocilizumab)和JAK抑制(如baricitinib)显示出了希望,但最终还是需要RCT。其中一些研究正在进行或最近完成,其结果令人期待[3.].表现出CSS表型的新冠病毒-19患者肯定处于疾病谱的严重末端。因此,试验应以免疫反应失调的患者为目标,以确定免疫调节疗法的真正疗效。2020年7月29日,新冠病毒RCT的新闻稿(NCT04320615)比较了托西珠单抗和安慰剂在COVID-19中的主要结果(临床状态和死亡率)没有差异。然而,在住院时间和无呼吸机天数方面出现了积极的趋势,但由于未能达到主要终点而被认为不显著。COVACTA试验的纳入标准非常广泛,只需要明确诊断氧饱和度为93%或更低或的COVID-19肺炎年代阿宝2/FIO2<300 mmHg,未提及全身炎症标志物,如CRP或IL-6。考虑到在RECOVERY试验中地塞米松治疗对重症患者更有利的梯度,COVACTA试验的亚组分析以及正在进行的免疫调节rct将会引起极大的兴趣。
可共享的PDF
确认
作者感谢凯瑟琳·比格斯对手稿的批判性评论。
脚注
作者贡献:所有作者贡献了文章的概念和起草,并为重要的知识内容提供了关键的修改和最终批准。
利益冲突:陈立昌没有什么可披露的。
利益冲突:霍伊兰没有什么可披露的。
利益冲突:斯图卡斯没有什么可披露的。
利益冲突:C.L.威灵顿没有什么可透露的。
利益冲突:ms . s . Sekhon没有什么可披露的。
支持声明:陈立春是UBC血液学研究项目的资助人。M.S. Sekhon得到了温哥华海岸健康研究所临床科学家奖的支持。惠灵顿学院得到了加拿大健康研究所、国家健康研究所、韦斯顿大脑研究所和治愈阿尔茨海默病基金的资助。本文的资金信息已存入交叉参考基金登记处.
- 收到了2020年8月2日。
- 接受2020年8月24日。
- 版权所有©ERS 2020
这个版本是在知识共享署名非商业许可4.0的条款下发布的。