摘要
原发性睫状体运动障碍的诊断通常通过标准的,尽管复杂和昂贵的测试来确认。然而,在许多情况下,尽管有一系列复杂的诊断测试,诊断仍然困难。没有“黄金标准”的参考测试。因此,由欧洲呼吸学会支持的一个工作组制定了本指南,以提供关于诊断测试的循证188bet官网地址建议,特别是鉴于此类测试的新发展,以及对可能进入随机对照治疗试验的患者进行可靠诊断的需求。该指南基于与临床护理相关的预先定义的问题,对文献的系统回顾,以及使用GRADE(建议分级、评估、发展和评估)方法对证据进行评估。重点介绍临床表现、鼻一氧化氮、高速视频显微镜分析、透射电镜、基因分型和免疫荧光分析睫状搏动频率和模式。然后使用改进的德尔菲调查开发了一种算法,用于使用诊断测试,以明确确认和排除原发性纤毛运动障碍的诊断;并在诊断不确定时提供建议。最后,本指南为未来原发性睫状体运动障碍诊断方法有效性的研究提出了一套质量标准。
摘要
国际ERS指南建议联合检查诊断原发性纤毛运动障碍http://ow.ly/sJhH304InBN
简介
原发性纤毛运动障碍(PCD)是一种临床和遗传异质性的呼吸道纤毛病,气道粘液纤毛清除减少。不同的突变导致不同的临床和病理模式,增加了诊断的挑战。PCD没有单一的金标准诊断测试[1].目前的诊断需要结合技术要求高的调查,包括鼻一氧化氮(nNO),高速视频显微镜分析(HSVA)和透射电子显微镜(TEM)。历史上,临床医生使用糖精试验来筛查PCD,但这已不再被提倡。2].此外,可能提高诊断准确性的更复杂的诊断测试(基因分型、纤毛蛋白免疫荧光和电子显微镜断层扫描)正变得越来越容易获得。
测试的可获得性在欧洲各地各不相同[3.].最近,由于包括欧洲呼吸学会(ERS)前工作组(2006-2009)在内的合作,这一情况有了部分改善[188bet官网地址2- - - - - -4]和框架计划(FP -7)资助的BESTCILIA。ERS专责小组于2009年发表共识声明[2BESTCILIA最近在三个以前没有诊断测试服务的国家引入了诊断测试。自2009年发表声明以来,一些团体和财团对PCD各种诊断检测的准确性进行了调查,为通过制定循证指南来推进诊断状况提供了机会。因此,2014年成立了一个新的PCD ERS工作组,由肺科和耳鼻喉科学科的成人和儿科医生以及诊断科学家组成。它旨在为PCD的诊断制定基于证据的指南。这对于可疑或最终确诊的PCD患者的适当临床管理和预后非常重要,以确保PCD患者得到正确诊断,同时避免假阳性诊断的问题。它还应确保PCD患者在纳入随机对照临床试验治疗之前得到明确的诊断。
方法
这些方法在补充材料中有详细的描述。
专责小组的组成
简而言之,该小组由在PCD诊断方面具有公认专业知识的临床医生和科学家组成的多学科小组;隶属于欧洲PCD中心的初级成员/学员是委员会的积极成员(表S1)。ERS的方法学家根据诊断测试的GRADE(建议、评估、发展和评估的分级)方法,在制定指南方面提供了专业知识[5].小组成员在工作组开始时和本手稿发表之前,根据ERS政策披露了潜在的利益冲突。
Patient-important结果
GRADE方法强调基于对患者重要结果影响的建议的重要性[6].工作队的病人代表完全赞同,准确的诊断是一项重要的结果,因为它能使医生更好地认识到他们的问题,并得到更有效的治疗,从而改善他们的健康和生活质量。我们对来自25个国家的352例PCD患者的问卷调查和20次深度访谈证实了这一点[7].然而,诊断准确性研究并没有为改善患者重要结果提供直接证据;因此,对测试准确性研究结果的置信度充其量可以判断为中等。
主题和问题的制定
工作组成员一致认为应评估PCD诊断的六个方面:临床症状、nNO、HSVA、TEM、基因型和纤毛蛋白的免疫荧光标记。我们评估了每个测试,看看它是否应该包括在PCD的诊断途径中,使用“PICO”结构化问题:P怀疑患有PCD的患者我通过[nNO, TEM,等。),当C比较最终诊断结果为阳性或阴性的患者,诊断准确率(O考试的结果?”每个测试的PICO问题都是在几轮电话会议和电子邮件讨论中确定的(表S2)。
研究的基本纳入标准是,他们必须包括连续转诊进行PCD检测的患者,其中PCD诊断随后被确认或排除。我们排除了患者之前已经进行过诊断性检查的研究。在缺乏此类研究的情况下,在叙述性回顾中,我们讨论了将PCD患者与健康对照组或患有其他呼吸道疾病的患者进行比较的病例对照研究(如。囊性纤维化)。这些研究的结果不能推广到临床情况,在临床情况下,必须将患有PCD的患者与患有类似症状但没有PCD的患者区分开来。因此,病例对照研究的结果与临床护理的相关性较低。这个项目的主要限制是缺乏PCD诊断测试的金标准。在此情况下,我们比较了诊断性能指标(如。敏感性和特异性)对作者基于所有可用测试做出阳性/阴性PCD诊断的最终决定。
工作组还商定了一份与PCD诊断相关的非结构化问题清单,用于叙述性讨论。由于这些问题的证据没有正式分级,因此没有用于推荐。
文献检索方法
从1996年1月1日到2016年3月14日,我们搜索了Medline和Embase数据库(通过Ovid访问)。详细情况见补充材料。简而言之,标题和摘要经过筛选;然后对全文进行了审查,以寻找可能符合纳入标准的论文。这些手稿由工作组小组检查了完整性,以确保所有数据符合要求先天的存在纳入标准。PRISMA流程图显示了每个工作组的搜索过程(图S1)。
证据的质量和建议的强度
我们在整个过程中使用了GRADE方法,从对证据质量进行分级,到决定建议的强度[8,9].补充材料中提供了详细信息,并包括降低证据可信度的原因(证据表摘要)。根据证据强度和其他因素,如试验的总体准确性(敏感性和特异性)、净准确性的置信度(纳入研究的敏感性/敏感性范围和/或净敏感性和特异性的置信区间),以及患者对试验的可接受性、试验的可行性和试验的可获得性等考虑因素,提出了建议。四项检测均以证据为基础提出建议,患者均可接受,可行且可接受。
确认或排除PCD的一致声明
我们使用改进的德尔菲调查,就使用诊断测试来明确确认和排除PCD诊断达成共识,并为没有明确诊断但诊断测试表明诊断极有可能或不确定的患者提供建议。方法详见补充材料。
结果
证据评估的结果产生了所列的建议表1.
临床特征
建议摘要
哪些患者应转介进行诊断检查?
基于温和的对证据的信心:
1)如果患者有以下几个特征,我们建议检查PCD:持续湿咳;位置异常;先天性心脏缺陷;持续的鼻炎;慢性中耳疾病伴或不伴听力丧失;足月婴儿新生儿上呼吸道和下呼吸道症状史或新生儿重症监护入院史(强烈推荐)。
2)如果患者体位正常,但有其他提示PCD的症状,应转诊进行诊断检测(强烈建议)。
3)患者的兄弟姐妹应进行PCD检测,特别是如果他们有PCD的症状(强烈建议)。
4)我们建议结合使用不同的PCD症状和预测工具(如。PICADAR)识别患者进行诊断测试(弱推荐)。
对直接解决“在怀疑患有PCD的患者中,哪些临床特征预测阳性诊断”这一问题的证据的回顾?
我们的搜索确定了1269项研究,其中两项直接回答了这个问题,并被纳入了定量综合(图S1),另外六项有助于叙述性回顾。我们根据标题和摘要排除了1217篇论文。在全文审查后,我们排除了其余52项研究中的44项,因为它们不符合纳入标准(表S3)。
两项研究,Behanet al。[10]和Shapiroet al。[11],为我们的建议提供了证据。他们包括1408名患者(表2).
Behanet al。[10]分析了连续868名儿童和成人患者的数据。排除结果不确定或不完整的227例,留下641例进行分析。在诊断测试之前,所有的患者数据都是通过临床医生完成的形式表格收集的。他们报告了大量临床特征的敏感性和特异性(表2表S3)。湿性咳嗽在PCD阳性和阴性患者之间没有很好的区分(敏感性0.93,特异性0.15)。因为它是转诊的主要原因,它几乎存在于所有患者中。新生儿胸部症状和新生儿鼻炎的特异性较高(0.83和0.94),敏感性较低(0.27和0.75)。总结了25个临床特征的敏感性和特异性表2并在补充材料中有详细描述。
除了报告单一症状,Behanet al。[10]开发了一种基于7点问卷的预测工具(PICADAR),以帮助预测转介评估持续性湿性咳嗽患者患有PCD的可能性。PICADAR经过了内部和外部(在第二个队列中)验证,是针对PCD开发的第一个临床预测工具。比分从0到14不等。> - 5分的敏感性和特异性分别为0.90和0.75,明显优于单一症状。
年代hapiroet al。[11]分析了767名连续的儿童和成人患者的数据。位置信息由当地联盟的医生通过检查参与者病历中的放射学、外科和心脏病学报告以及放射学图像来确定。患者被分为三种体位类别:独位、逆位和异位(包括异位)。
Behanet al。[10]和Shapiroet al。[11]共1048名患者。两篇论文(任何部位异常)的合并敏感性和特异性分别为0.508和0.939(表S3)。
补充证据的叙述性回顾
leighet al。[12]描述了534名高度怀疑PCD的儿童的前瞻性队列,其中许多儿童已经被诊断为PCD。专家定义先天的并测试了儿童早期明显的五种临床特征,发现其中四种(单独或联合)可预测PCD: 1)足月婴儿不明原因的新生儿呼吸窘迫,>补充氧气24小时;2)早发、全年湿咳;3)早发性全年鼻塞;4)侧面缺陷[12].Nollet al。[13]描述了一项回顾性队列研究,涉及323例慢性咳嗽患者进行睫状体功能分析,并报道了新生儿呼吸窘迫、持续性中耳炎、逆位和支气管扩张的高特异性(>0.9)。C欣et al。[14]回顾性回顾了118例因怀疑PCD而转诊进行电子显微镜检查的患者的记录,并比较了电子显微镜异常和正常患者的症状组合,同时排除了不确定的病例。他们发现异常组的鼻部、中耳和肺部症状更多[11].B你们这里过得很愉快et al。[15]对89例疑似PCD儿童的回顾性队列中电子显微镜异常和正常的患者进行了比较,排除了21例不确定病例,发现两组之间只有逆位有显著差异。Pifferiet al。[16]比较了98例原发性PCD患者的临床症状与继发性睫状体运动障碍和支气管扩张的反位和严重程度存在统计学差异。在唯一关注新生儿的出版物中,Mullowneyet al。[17]比较了46名PCD患者和46名有新生儿呼吸窘迫综合征病史的对照组的新生儿症状,发现大叶塌陷、反位和长时间的氧气需要在PCD患儿中更为常见。在> ~ 2天内合并腹背位、大叶塌陷或需要氧气对PCD的敏感性为87% (95% CI 74-94),特异性为96%(85-99)。Goutakiet al。[18]描述了其他关于PCD临床症状流行率的病例对照或病例系列研究,这些研究不符合本研究的纳入标准。所有研究均来自发达国家,某些症状的预测值可能因地理区域的不同而不同;例如,撒哈拉以南非洲地区因结核病引起的支气管扩张很常见,因此对支气管扩张的敏感性和特异性就有所不同。
关键未解问题和研究需求
进一步的研究需要使用前瞻性队列研究的患者转诊怀疑PCD,在他们的临床特征在他们被诊断之前,以标准化的方式评估。分析必须按年龄分层。特别需要对患有新生儿呼吸窘迫综合征的新生儿进行前瞻性研究。此外,使用最先进的方法将信息合并到临床预测评分中可能会有所帮助[17].不同临床特征的有效性也可能因被评估人群的不同而有所不同。例如,症状的阳性和阴性预测值在很大程度上取决于转诊人群中疾病的患病率,在患病率较低的人群中预后较差(即。与PCD转介中心相比,在初级或二级保健方面)。敏感性和特异性(如表2所示)与患病率无关。然而,PCD表型的混合,以及因此不同症状对PCD预测的有用性,可能在参加专门诊所的患者之间有所不同(如。耳鼻喉,肺脏学和心脏病学)。例如,在肺科诊所中,慢性咳嗽无法区分是否患有PCD的患者,而在耳鼻喉科诊所中,(几乎)每个患者都有这些症状,慢性耳鼻喉症状也无法区分,在心脏病科诊所中,心脏缺陷也无法区分。另一个需要考虑的因素是不同基因变异的临床特征可能不同(如。CCNO变异体患者无原位异常,但女性不孕症增加),因此结果因评估人群中特定突变患病率的差异而异。因此,研究必须在特定的医疗保健环境和研究人群中进行,并考虑年龄、性别和遗传异常。
总结
回答我们问题的相关文献非常少(只有两篇论文,其中一篇仅报道了逆位),并且结果没有考虑症状的严重程度或按年龄分层。对其结果的总体信心是中等的,主要是因为诊断性能没有告知基于这些症状评估的进一步临床管理的下游后果。
结果表明,临床症状可能有助于区分PCD患者和非PCD患者,但单一症状的阳性预测价值(有多少特定症状的患者患有该疾病)较低。相反,提示性症状的组合可能会更好地区分,但这需要在不同人群中进一步研究。
在大多数PCD研究中,儿童早期开始的湿性咳嗽被用作初始选择标准。因此,由于其在PCD阳性和阴性个体中都有很高的患病率,因此具有较低的鉴别价值。
鼻用一氧化氮
建议摘要
在怀疑患有PCD的患者中,nNO是否应该用作诊断工具?
基于温和的相信证据,我们建议:
1) nNO测量应作为> - 6岁学龄儿童和怀疑患有PCD的成年人诊断工作的一部分,最好使用带膜闭合技术的化学发光分析仪(强烈建议)。
2)对于怀疑患有PCD的<6岁儿童,我们建议使用潮汐呼吸测量nNO作为诊断检查的一部分(弱推荐)。
我们建议有较强临床病史的患者进行进一步检查,即使nNO是正常的(弱推荐)。
诊断测试说明
与健康对照组和疾病对照组相比,PCD中的nNO含量极低,原因未知[19].nNO作为PCD诊断测试的准确性因分析仪类型、采样方法和患者年龄而异[20.].
目前的指南建议从一个鼻孔抽吸气体通过用固定化学发光分析仪在膜闭合时测量nNO,如屏气或抗阻力的口腔呼气。读数应从技术上可接受的平台读数[21].虽然化学发光分析仪在膜闭合期间的测量被认为是“金标准”,但这种操作并不适用于所有情况。在幼儿潮汐呼吸期间的测量已被报道[22,23].便携式机电分析仪[23]用于没有固定化学发光分析仪的地方。目前,对于什么阈值构成积极或消极的界限,没有达成共识。
虽然分析仪报告的读数为十亿分之一(ppb),但这受到机器采样率的影响,因此浓度转换为nL·min−1公式nL/min=ppb×sampling速率,单位为L·min−1.
对直接涉及“疑似PCD患者,nNO是否应被用作诊断工具?”这一问题的证据的回顾?
我们的检索确定了98项研究,其中23项符合定性评估的纳入标准。其中,四篇论文(n=588例患者)评估了PCD患者队列中最终诊断为阳性或阴性的nNO,直接解决了这个问题(表3表S4)。其他19篇论文被排除在建议之外,但对叙述审查作出了贡献(表S5)。
米arthinet al。[24]测定屏气、呼气阻力和潮汐呼吸时的nNO。敏感性范围为0.92(屏气)至1.0(口服呼气抵抗阻力),特异性范围为0.80(潮汐呼吸)至0.96(屏气)[24].leighet al。[25]的阈值为77 nL·min−1使用PCD专家中心的数据,然后在其他地点的155名连续患者中试验了这种切断。将pcd阳性患者与不确定患者进行比较,其敏感性为0.99,特异性为0.75 [25].特异性较低是因为诊断方案只包括电子显微镜和遗传学,因此遗漏了一些真正的PCD病例(“不确定”而不是PCD阴性)。Beydonet al。[22]报告了膜闭合的敏感性为0.91,特异性为0.86(截止值为82 nL·min−1),潮汐呼吸为0.90和0.97 (40 nL·min−1;5个峰的平均值)。Jacksonet al。[26]使用30 nL·min的临界值−1报告的敏感性和特异性分别为0.91和0.96,以区分34名pcd阳性患者和267名pcd阴性患者。这四项研究的进一步方法细节载于表S4。
对这一证据的总体信心中等,主要是因为诊断表现不能说明进一步临床管理的下游后果。
补充证据的叙述性回顾
一些不符合提出建议的纳入标准的研究涉及了重要问题。一些研究使用了替代方法来测量nNO,这些方法没有使用美国胸科学会/ERS指南“金标准”(膜闭合,静止分析仪)[21].潮汐呼吸是有用的,特别是在那些不能执行膜闭合,但可能不太有区别。M的研究arthinet al。[23与潮汐呼吸值(0.93和0.80)相比,屏气敏感性为0.92,特异性为0.96(阈值为屏气-52.5 nL·min−1潮汐呼吸-47.4 nL·min−1).然而,Beydonet al。[22]发现潮汐呼吸的准确性提高(37.9 nL·min−1阈值;敏感性0.94,特异性0.92)与膜闭合(82.2 nL·min−1敏感性0.91,特异性0.86)。在两项病例对照研究中评估了使用便携式分析仪的测量。使用便携式分析仪,Marthinet al。[23]将PCD患者与囊性纤维化患者和健康对照组进行了比较。他们发现屏气(64 nL·min)的敏感性和特异性分别为1.0和0.95−1潮呼吸(43 nL·min)的阈值分别为1.0和1.0−1) [23].H棱et al。[27]对13名PCD患者和37名疾病对照/健康患者进行了潮汐呼吸和便携式分析仪,截止时间为30 nL·min−1.敏感性和特异性分别为1.0和0.95。
测量幼儿的nNO是可能的;然而,PCD患者与对照组之间的差别降低了,因为在<12岁的健康患者中,nNO与年龄成反比[28,29].一项研究表明,早在3.9岁的儿童就可以闭合牙膜[20.].然而,大多数幼童无法配合牙膜闭合,因此必须使用潮汐呼吸测量。M的研究arthinet al。[23选项Beydonet al。[22]表明潮汐呼吸可能产生与成人牙膜闭合相似的准确性;然而,这并没有在儿童身上表现出来。本研究采用Marthinet al。[23]发现6岁以下儿童使用潮汐呼吸的假阳性率为39%。
越来越多的证据表明,一些导致PCD的基因突变可能与微妙的搏动异常和nNO水平在正常范围内有关。这包括两项关于编码径向辐头蛋白突变的PCD个体的研究,以及一项关于由于GAS8突变导致连接蛋白连接组成异常的PCD个体的研究,这些突变与PCD中通常看到的更高的nNO相关[30.- - - - - -32].这可能部分解释了在一些研究中nNO结果的可变性和低诊断性能。
关键未解问题和研究需求
目前的证据表明,作为诊断过程的一部分,nNO是一种有用的测试;但是,对于适当的阈值并没有达成共识。同样,需要为年幼儿童,特别是6岁以下儿童的潮汐呼吸、便携式分析仪和测量以及规范数据制定标准化方案和阈值。基因型-表型相关性的进一步研究有助于在诊断不确定的情况下解释nNO水平,以减少假阴性检测结果的数量。没有证据可以让我们推荐哪些正常的nNO患者应该进行进一步的检测,这需要评估。
总结
当测量时,nNO是PCD的高精度测试通过采用膜封闭技术的固定式化学发光分析仪,灵敏度和特异性分别为0.90-1.0和0.75-0.97。潮汐呼吸技术或使用便携式分析仪敏感性和特异性较低,但可能有助于诊断决定。不同的研究使用了不同的方法和临界值,因此很难提供确定的阈值。
nNO还不足以准确地单独排除PCD,但考虑到它相对容易执行,无创且负担得起,专家组认为它应该被用作疑似PCD患者诊断工作的一部分。
高速视频分析
建议摘要
在怀疑患有PCD的患者中,HSVA是否应该用作诊断工具?
基于低相信证据,我们建议:
1) HSVA,包括睫状体搏动频率和搏动模式分析,应作为怀疑PCD患者诊断工作的一部分(弱推荐)。
2)在诊断PCD时,不能在没有评估睫状体搏动模式的情况下使用睫状体搏动频率(强烈建议)。
为提高HSVA的诊断准确性,应在气液界面培养后重复CBF/p评估(强烈建议)。
测试说明
PCD与睫状体功能异常有关[33],可以进行分析体外通过评估鼻或支气管呼吸上皮中的纤毛活性。取样后可立即观察到纤毛细胞[34- - - - - -36]并在经过一段时间的培养以区分PCD与继发性运动障碍后再次进行[37- - - - - -40].连接在显微镜上的视频以高速(120-500帧/秒)记录,并以较慢的速度(30-60帧/秒)重播,以回顾睫状体搏动模式及测量睫状体搏动频率[41].大多数研究使用了专业显微镜学家的分析,而一些研究使用了计算机分析,试图减少主观性/观察者的偏见。HSVA提供永久记录,可用于审计、专家建议或研究。
对直接涉及“疑似PCD患者,是否应将HSVA用作诊断工具?”这一问题的证据进行了回顾。
我们的检索确定了113项研究,其中30项符合定性评估的纳入标准。(图S1)。两项研究(650例患者)在怀疑PCD的队列中评估了最终诊断为阳性或阴性的HSVA,为建议提供了证据(表4).其他28篇论文不符合提供建议的纳入标准,但对我们的叙述审查有贡献(表S6)。
P结束时et al。[42]测量了睫状搏动模式12项参数,包括睫状搏动频率。在区分10名PCD阳性患者和15名PCD阴性患者时,以拍打边缘百分比加权的纤毛尖端移动的距离具有最佳的敏感性(0.96)和特异性(0.95)[42].在9例先前诊断不确定的患者中使用该参数,有可能支持4例PCD的诊断,2例排除PCD。Jacksonet al。[26]发现,在625名转诊患者(包括60名PCD阳性患者)中,睫状搏动频率测量和搏动模式评估相结合的敏感性和特异性分别为1.00和0.93。
对这一证据的总体置信度较低,主要是因为基于HSVA评估的进一步临床管理的下游后果的诊断性能没有信息,并且由于研究的局限性(HSVA被广泛用作参考标准的一部分并且缺乏盲法)。
补充证据的叙述性回顾
到目前为止,还没有细胞处理和分析的标准化方法。可使用刷子、刮匙或镊子采集呼吸道上皮,通常从鼻子采集[43].睫状体功能在不同条件下有所不同;例如,温度和pH值,有些中心的测量值为37oC (26,40,42,44]和其他较低温度的[35,37,45].这将影响睫状体功能,所有中心都需要确定自己的规范数据,直到达成共识,允许中心之间的方法和报告标准化。
不明确的结果或异常的结果需要在细胞培养后重复采样或重新分析[38,40,46,47因为次生缺陷很常见。在712例患者中,Jorissenet al。[47]评估悬浮培养中睫状体搏动频率和睫状体协调性(即。球状体)。642例(20%)非pcd患者在培养前睫状体活性异常,但培养后100%的患者睫状体活性正常。相反,在70例PCD患者(56例可评估)的活组织检查中,20%的人在培养前睫状体搏动频率正常,10%的人睫状体活动协调。培养后,7%的PCD患者发现睫状体搏动频率正常,但睫状体功能从未正常协调,这使得该参数比睫状体搏动频率测量更敏感和具体[47].H首先et al。[40]报道了158例患者在气液界面培养前后睫状搏动频率和模式。在培养前,大多数PCD和非PCD患者表现出一定程度的功能性睫状体异常。经气液界面培养后,非PCD患者睫状体搏动模式均正常,PCD患者睫状体搏动模式均异常。Pifferiet al。[46]评估悬浮培养后睫状搏动模式及频率分析结果(即。9名受试者的鼻刷结果不确定。培养后,4例患者睫状搏动模式异常提示PCD诊断,2例为继发性运动障碍睫状搏动模式,3例仍不确定。培养技术的成功率从54%到83%不等[26,37,40].
睫状搏动频率测量不能充分区分PCD与非PCD,除非结合睫状体搏动模式评估。年代tannardet al。[48]发现,对运动障碍上皮边缘百分比的敏感性和特异性分别为0.97和0.95,而单纯的睫状搏动频率的敏感性和特异性分别为0.87和0.77。此外,PCD患者的睫状搏动频率可能是缓慢的、正常的或增加的,这取决于基因型[45].
一些引起PCD的超微结构缺陷和基因突变可能与睫状体搏动的特定模式有关。在一组56名儿童中,Chilverset al。[44]报告了内外动力蛋白臂(IDA和ODA)联合缺陷或孤立的ODA缺陷患者几乎不活动的纤毛;孤立性IDA或放射状辐条伴IDA缺损患者的僵硬搏动模式;睫状体转位缺损患者的环状跳动纤毛。R·埃迪特et al。[45]根据PCD的遗传变异研究了睫状体搏动模式。虽然与一些基因相关的数量非常少,但数据支持PCD引起基因与特定的纤毛跳动模式之间的联系:来自ODA引起基因突变患者的纤毛(Dnah5 dnai1 dnai2 armc4)显示残余运动极少。在DNAH11突变(正常超微结构)的患者中,纤毛表现出多动性纤毛搏动模式,近端轴突弯曲减少。一些遗传缺陷,如GAS8突变,可导致HSVA难以检测到的细微缺陷[30.].
关键未解问题和研究需求
目前的证据表明,作为诊断过程的一部分,HSVA是一个有用的测试,但在适当的细胞处理和纤毛评估方法上没有共识。同样,需要制定标准化的协议和阈值体外睫状体搏动模式分析。基因型/超微结构表型相关性的进一步研究有助于在诊断不确定的情况下解释HSVA参数。
总结
由经验丰富的观察者结合睫状搏动频率测量和模式分析(敏感性和特异性分别为0.95-1.00和0.93-0.95)进行HSVA是PCD的准确测试。培养呼吸细胞可能有助于提高HSVA的准确性,特别是排除假阳性。
HSVA还没有足够的标准化来单独排除PCD。考虑到纤毛功能评估的最佳条件仍有待确定,专家组认为HSVA应由有经验的工作人员进行,作为怀疑患有PCD患者诊断工作的一部分。这可能会影响许多检测中心的可用性。
透射电子显微镜
建议摘要
怀疑患有PCD的患者,透射电镜是否应该用作诊断工具?基于低相信证据,我们建议:
1)睫状体超微结构分析应作为怀疑PCD患者诊断工作的一部分(强烈建议)。
2)若有较强的临床病史,应进一步进行诊断调查。
3)对于有PCD标志性睫状体超微结构缺陷的患者,不需要进一步的确诊性诊断调查(强烈建议)。
诊断测试说明
1976年,Afzelius[33]证明透射电镜可用于原发性纤毛运动障碍患者纤毛超微结构缺陷的检测。随后,多年来,TEM被认为是PCD的“金标准”诊断测试。然而,一些遗传学研究表明,越来越多不同的PCD遗传亚型(如。由于DNAH11突变)无法通过透射电镜诊断[49].因此,TEM不能排除PCD诊断。
呼吸道上皮通常通过刷子或刮勺活检从鼻下鼻甲取样,或在支气管镜检查时从下呼吸道取样。用戊二醛化学固定上皮,加工并嵌入块,用超微切片。用重金属(铅和铀酰)染色可以形成对比。利用透射电镜对横切面健康细胞的纤毛进行评估[50,51].不同中心分析的纤毛和细胞数量不同;除非有足够的数量进行评估,否则由导致间歇性缺陷的基因突变引起的缺陷很可能会被遗漏。执行瞬变电磁法和解释结果需要相当的专业知识;设备和运行费用的支出很高。
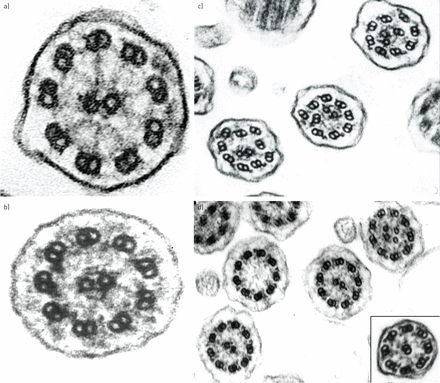
正常的超微结构睫状体横切面排列是由9个微管双联组成的圆形,每个微管双联都有一对动力蛋白臂,再加上一对中央微管(图1).有许多与PCD诊断相关的超微结构表型(图2).大多数病例是由于缺乏动力臂;其他缺陷包括微管孪晶的无序或中央微管对的缺失(表5).部分PCD患者在透射电镜下睫状体超微结构明显正常。继发性纤毛运动障碍可伴有短暂的超微结构异常,如复合纤毛、轴突泡或额外的小管,千万不要与PCD混淆。
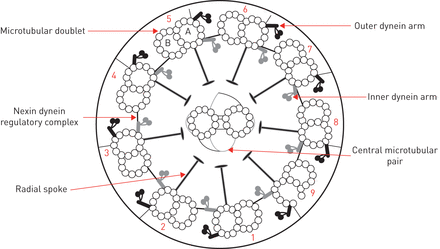
睫状体轴突横切面正常超微结构图。
原发性纤毛运动障碍缺陷的电子显微镜图像。a)内外动力蛋白臂缺陷,b)外动力蛋白臂缺陷,c)内动力蛋白臂和微管紊乱,d)中心对和转位缺陷。
对直接涉及“怀疑患有PCD的患者,TEM是否应该用作诊断工具?”这一问题的证据的回顾?
我们确定并筛选了370篇研究,其中46篇全文进行了合格性评估。在符合定性评估纳入标准的17篇论文中(表S7),有11篇论文(3200名患者)在一组疑似PCD的患者中评估了TEM,这些患者最终诊断为阳性或阴性,为推荐提供了证据(图S1)。
表5而且6总结解决这个问题的11项研究。每项研究的敏感性在0.71 - 1.00之间,特异性在0.92 - 1.00之间。在两项研究中有5名假阳性患者。P结束时et al。[42]鉴定出两个假阳性结果;一个是严重哮喘,没有复发性上气道感染的儿童,44%的鼻纤毛和90%的支气管纤毛有短或缺失的ODA,另一个是无下气道症状的内位鼻息肉成人,没有IDA,没有微管组织(个人交流)。米unkholmet al。[57]在最终被认为患有继发性纤毛运动障碍的个体中发现了三个假阳性,其中两个临床表型改善,变得无症状,第三个患有严重哮喘。综合所有11项研究,总特异性为>0.99。
证据质量被评为较低,因为诊断性能不能反映进一步临床管理的下游后果,而且由于研究的局限性(参考标准中经常使用TEM和缺乏盲法)。然而,TEM极低的假阳性率和极高的特异性导致了强烈的推荐。
补充证据的叙述性回顾
对PCD患者TEM缺陷比例的评估是在回顾了描述超过50人队列的所有手稿(1996年以后)后进行的[26,42,48,56,58,59) (表4).ODA缺陷(26-59%)和ODA和IDA联合缺陷(6-39%)是最常见的。以下建议是针对常见的标志性缺陷(ODA缺失、IDA和ODA合并缺失、IDA缺失合并微管排列紊乱)。TEM分离的IDA缺陷是有争议的。一些研究承认,利用透射电镜很难观察到IDA [42,60,61]并建议在确诊前进行重复分析[62].对于中心对缺陷,纤毛缺陷通常出现在少数纤毛中,这使得诊断困难,特别是因为患者没有反位。
本文综述了电子显微镜技术在PCD诊断中的应用。据报道,计算机辅助分析可以增强动力蛋白臂的可视化,从而提高电子显微镜的灵敏度[60,61].电子断层扫描是一种先进的透射电镜技术,可以在三维结构中可视化。通过围绕两个垂直轴以规则增量倾斜试样阶段,可以获得一系列TEM图像。然后,来自两个倾斜系列的图像对齐成单个三维高分辨率投影。如果一个结构特征在一个层析图中重复出现,它可以通过次层析图平均得到增强;一种由软件提取所选的共同特征并通过相互关联进行比较的技术。电子断层扫描已被证明可以提高纤毛的三维可视化和分辨率,从而识别患有HYDIN而且DNAH11研究环境中的基因缺陷[63].断层扫描在诊断中的应用尚未得到评估。
我们的证据回顾只考虑了结论性结果。报告的不确定结果比率由1.7%至28.6%不等[26,37,39,58].这是由于取样技术差或存在纤毛的二次变化。11项研究中有7项报告了采取措施避免在上呼吸道感染期间或之后立即取样,以提高充分性并尽量减少继发性纤毛超微结构变化。
从人体活检中诱导纤毛发生的细胞培养技术被用于许多PCD诊断中心。两种诱导基底细胞增殖和纤毛细胞分化的技术已被描述用于PCD诊断[37,40].Jorissenet al。[37]建立了深埋培养技术,并首次描述了气液界面技术在PCD诊断中的应用首先et al。[40].这两种方法都表明,在正常和PCD受试者的细胞培养后,TEM轴突结构是保守的,并且它们已被证明可以减少继发性损伤[37,40].透射电镜培养后可帮助诊断多运动纤毛减少[64].
关键未解问题和研究需求
基础科学研究必须改进透射电镜技术,在“超微结构正常”的人群中鉴别PCD。诊断界需要标准化的协议和术语上的共识,特别是关于诊断所需的纤毛数量和比例。IDA和其他罕见缺陷的真正相关性和患病率有待证实。
遗传学
在怀疑患有PCD的患者中,是否应该将基因分型用作诊断工具?没有研究符合纳入标准来回答这个问题。
诊断测试说明
PCD是一种遗传异质性疾病。与一般常染色体隐性遗传疾病一样,疾病更有可能发生在近亲关系的后代中,并且在父母双方都是健康携带者的任何受孕中有1:4的概率。迄今为止,已有超过30种基因的突变可引起PCD (表7).补充材料中介绍了pcd相关基因的更详细的解释。
为了建立遗传诊断,应确定常染色体隐性PCD中的非模糊双等位基因突变和x连锁PCD中的半合子突变。大多数报道的突变是无义突变、移码突变或剪接突变,而在少数病例中发现了错义突变。大多数突变是私有的,但创始突变(如。在DNAI1[105),DNAH5[95])和突变热点(例如CCNO[106])。突变影响的排序应遵循国际建议[107良性(1类),可能良性(2类),意义未知(3类),可能致病(4类),致病(5类)。
TEM和/或免疫荧光记录的基因型和结构缺陷之间的关联已经很好地建立起来,但对基因HSVA的关联知之甚少。由于研究对象是少数患者,而且每位患者的视频数量往往有限[45],没有足够的数据表明基因突变与运动障碍表型相关。迄今为止,我们的知识表明,DNAH5中的致病突变总是与主要的静态纤毛有关,而DNAH11不同区域的突变可以导致静态纤毛或过度频繁的硬纤毛[45,108].因此,要确定PCD的遗传原因,应将超微结构缺陷与基因联系起来;在未来,我们可能能够使用基因突变的纤毛模式相关性作为进一步的支持。
原则上,所有的DNA测序技术都可以应用于PCD确诊或高度怀疑PCD患者的基因检测(见补充材料)。然而,由于PCD基因数量多、体积大,高通量技术得到了广泛应用。由于PCD具有较高的遗传和等位基因异质性,等位基因特异性方法的产量较低。检测到的突变应通过Sanger测序确认,并检查亲本的分离。遗传实验室必须意识到,在PCD个体中已经报告了大量的杂合基因组缺失,这可能会被DNA测序技术所遗漏。纯合和杂合的基因内大重复和深内含子突变也被测序技术所遗漏。基因内缺失和重复的检测将受益于有针对性的下一代测序面板的精细设置;然而,这种方法需要特定的开发和敏感性评估。所有技术,特别是二线入路,都得益于对患者超微结构缺陷的了解,以便评估分子发现的相关性。迄今为止涉及的约30个PCD基因包含>700个外显子,因此根据超微结构数据,在明显与患者疾病无关的基因中识别杂合变异并不罕见。 Cell and whole organism models can be used to confirm that a gene is disease causing.
对直接涉及“疑似PCD患者,是否应将基因分型用作诊断工具?”这一问题的证据的回顾?
检索确定了462项研究,其中95项符合定性评估的纳入标准(表S8)。大多数研究纳入了确诊PCD的患者,目的是鉴定新基因,而不是诊断队列。没有研究符合定量评估的纳入标准。
补充证据的叙述性回顾
在确诊或高度怀疑PCD诊断的人群中,有可能在50-75%的病例中确定遗传原因[109,110].基因检测作为PCD一线诊断检测的敏感性目前尚不清楚,但可能较低。随着更多PCD基因的发现和高通量测序技术的发展,未来可能会考虑将PCD基因检测作为“独立”检测。基因分型在其他方法难以确认诊断的情况下是有用的(例如DNAH11,CCNO,MCIDAS而且RSPH基因突变)。常染色体隐性PCD中双等位基因致病突变或x连锁PCD中半合子突变的检测是高度特异性的。
大多数鉴定新型PCD基因缺陷的研究以常规透射电镜检测到的超微结构缺陷为遗传学搜索的起点;因此,在有超微结构缺陷的PCD中识别突变的可能性高于没有超微结构缺陷的PCD。这强调了不需要依赖透射电镜作为PCD的唯一诊断测试。
特定基因突变的报告通常涉及少数患者,并不一定具有种族代表性;因此,每个基因的贡献都应谨慎解释。研究测试DNAH5而且DNAI1突变表明,这些突变占ODA缺陷病例的~ 50-70% [94,95,111,112].突变CCDC39或CCDC40[89,90,103,113]几乎所有PCD患者都伴有微管组织紊乱和缺乏IDA。在58例无相关的PCD患者中,22%的PCD患者有双等位基因突变DNAH11[96].径向辐头和茎蛋白(RSPH1, RSPH3, RSPH4A, RSPH9), HYDIN和nDRC蛋白(DRC1, CCDC65, GAS8)的基因突变可导致PCD的超微结构正常或轻微异常(表7);到目前为止,这些基因对PCD患病率的贡献尚未确定。
一项系统的基于人群的以色列遗传研究显示,RGMC在其特定PCD人群中可能比先前估计的更频繁(6%)[106].
遗传分析表明,RGMC基因突变CCNO而且MCIDAS,以及编码径向辐条蛋白(RSPH1, RSPH3, RSPH4A, RSPH9)和中心对相关蛋白HYDIN的基因,不导致侧性缺陷。此外,迄今为止,所有在编码nDRC蛋白的基因(如CCDC164、CCDC65和GAS8)中携带双等位基因突变的PCD个体均未表现出任何位点异常。
考虑到PCD患者中测序区域的大小,识别一个或几个与疾病无关的罕见错义变异并不罕见。应该非常小心地解释这些变体。对这些变异进行分离分析是很重要的,它们的解释可以依赖于专家实验室。在某些情况下,免疫荧光显微镜已被证明是一种有用的工具,可用于确定编码径向辐头蛋白的RSPH4A和RSPH9突变的PCD个体错义性突变的致病性[86].然而,免疫荧光分析可以正常,如果突变蛋白仍然表达和正确组装在轴突内,如报道DNAH11错义突变[97].
我们没有发现证实或反驳基因分型作为PCD诊断测试的证据。虽然需要证据证明基因分型在诊断环境中的实用性,表8总结了工作组对目前发表的PCD基因检测证据的评估。
关键未解问题和研究需求
在PCD诊断途径中,基因检测的作用还没有很好地定义。我们需要研究来调查遗传学作为PCD诊断工具的准确性和局限性。PCD的诊断检测标准需要明确。
总结
由于缺乏合适的研究,我们无法确定基因检测的准确性。一些研究已经确定了PCD患者的基因,表明基因检测可以在65%的病例中识别出该基因;随着更多的基因被发现,这种情况可能会增加。随着新数据的出现,诊断准确性的问题应该重新考虑。
免疫荧光
在怀疑患有PCD的患者中,免疫荧光是否应该用作诊断工具?没有研究符合纳入标准来回答这个问题。
诊断测试说明
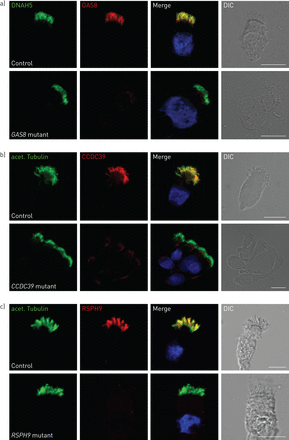
睫状蛋白标签的发展是为了提高对致病基因对睫状蛋白影响的认识[116].具有二级荧光标记的特异性抗体定位于人呼吸道上皮细胞中的蛋白质,并通过荧光或共聚焦显微镜可见。许多针对睫状体蛋白的抗体是可用的,包括靶向ODA, IDA,径向辐头和动力蛋白调节复合物蛋白的抗体。中显示了该技术的一个示例图3.
免疫荧光显微镜可用于识别运动纤毛的结构缺陷,并有助于原发性纤毛运动障碍的诊断。本文列举了三个染色异常的例子。a)针对外动力蛋白臂重链DNAH5(绿色)的抗体用于检测控制和携带a的人沿整个睫状体长度的外动力蛋白臂复体GAS8突变。针对GAS8的抗体(红色)可以识别nexin-dynein调控复合物的孤立缺陷。b) CCDC39抗体(红色)可以检测96nm轴突尺的缺陷,该尺由CCDC39和CCDC40组成。抗乙酰化微管蛋白(绿色)抗体用于描绘纤毛。c)抗RSPH9抗体(红色)可用于识别径向辐头复合体的各种缺陷。正常的睫状体成分定位表现为与睫状体轴突标记物共定位(黄色),如乙酰化微管蛋白(b和c中的绿色)或未受影响的睫状体成分(即.DNAH5 (a中绿色)。相反,突变细胞中该蛋白的缺失显示了与睫状体运动有关的结构成分的缺失(a - c中下图)。原子核用蓝色表示。差示干涉造影术。比例尺=10µm。
将悬浮液中的呼吸道上皮细胞置于载玻片上,风干并固定。细胞与与PCD无关的纤毛蛋白抗体一起孵育(如。乙酰化微管蛋白)标记轴突,并与不同物种产生的感兴趣的抗体(如。anti-DNAH5来识别ODA结构)。
对直接涉及“在怀疑患有PCD的患者中,免疫荧光是否应该用作诊断工具?”这一问题的证据的回顾?
我们的搜索确定了276项研究(图S1)。没有研究报道在诊断环境中使用免疫荧光抗体,因此,我们无法确定IF作为诊断测试的准确性。40项研究有助于我们理解免疫荧光诊断的潜力,总结如下(表S9)。
补充证据的叙述性回顾
虽然文献的研究重点是了解pcd相关基因突变的下游影响(表7),若干中心现采用免疫荧光辅助诊断[117].随着更多抗体的出现,以及检测准确性的数据获得,这一数字可能会增加。在两项最大的以患者为基础的队列研究中,在16名PCD患者和另外17个TEM观察到有ODA缺陷的家族中检测了DNAH5免疫荧光;所有病例均报告蛋白定位错误。此外,DNAH5蛋白存在于囊性纤维化患者和健康对照中[94,95].许多研究使用免疫荧光检测与基因突变相关的蛋白质错定位(表7),提供了可能被使用的抗体的指标,以及当免疫荧光被用作诊断测试时预期的结果。免疫荧光可以识别具有一系列突变的PCD患者的蛋白质定位错误,提供关于突变致病性的信息[86].然而,大多数手稿报告了来自少数患者的每个基因的免疫荧光结果,而突变的具体结果尚不清楚。
利用免疫荧光技术,可以识别几乎所有透射电镜检测到的超微结构异常,以及透射电镜明显正常或轻微异常的一些病例[30.,86,97].免疫荧光的敏感性和特异性尚不清楚,但可以反映抗体的组合和质量。根据作者的经验,许多抗体不起作用,在用于诊断前需要进行验证,包括适当的疾病和健康对照。如果突变蛋白仍在轴突内表达,免疫荧光分析可正常[97].
我们没有发现证据证实或反驳免疫荧光作为PCD的诊断测试。虽然在诊断环境中需要进一步的证据,但已发表的证据的工作组发现的摘要显示在表9.
关键未解问题和研究需求
在诊断队列研究中,我们需要验证研究来调查免疫荧光作为PCD诊断工具的准确性和局限性。每个应用的抗体都需要在研究中验证,包括适当的PCD疾病和健康对照。
总结
由于缺乏合适的研究,我们无法确定免疫荧光检测的准确性。工作组专家一致认为免疫荧光在临床环境中是有用的。免疫荧光比其他诊断检测更便宜、更容易,为资源有限的环境提供了一种潜在的检测方法。
确诊或排除PCD诊断
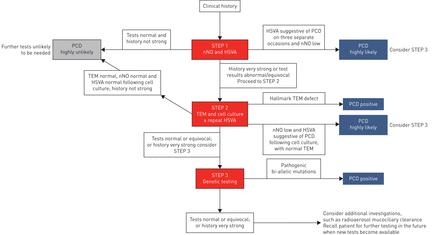
德尔福共识调查包括四项连续的在线调查,每项调查都建立在前几轮调查的基础上。表S11总结了每一轮的结果。ERS工作组的专家同意(≥80%的受访者)以下观点,这使我们能够提出一种诊断算法(图4).
在使用GRADE(建议分级、评估、发展和评估)方法开发建议之后,德尔菲调查允许我们提出原发性睫状体运动障碍(PCD)的诊断算法。并非所有患者都需要经历所有步骤。请参阅正文了解每种诊断结果(阳性、极有可能和极不可能)的影响,以及使用现有诊断测试继续获得不确定结果的患者的后果。随着诊断检测的进步,预后不确定的患者应重新考虑进一步检测。nNO:鼻一氧化氮;TEM:透射电子显微镜;HSVA:高速视频显微分析。
积极的诊断
对于有支持性PCD病史的患者,以下结果证实了PCD的阳性诊断。
1)透射电镜检测PCD的标志性睫状体超微结构缺陷(ODA缺失、IDA和ODA合并缺失、IDA缺失合并微管排列)。
2) PCD引起基因的非歧义双等位基因突变。
工作组未达成共识(80%),即任何其他单独或联合检测均可提供结论性阳性诊断。
高度可能的诊断
在有相容PCD病史的患者中,以下诊断测试结果使PCD的诊断极有可能,但不能提供明确的PCD诊断。
1)非常低的nNO加上HSVA的发现始终提示PCD (如。静止纤毛或盘旋)三次。
2)非常低的nNO加上与PCD一致的HSVA发现(如。静态纤毛或环绕)在细胞培养后。
如果诊断是“极有可能”,但不是结定论,应该告诉患者诊断是有可能的,但考虑到诊断测试的局限性,诊断并不是100%确定,可能需要在有更好的测试时进行确认。患者应排除其他导致其症状的原因,并应像患有PCD一样治疗。随着新的诊断方法的出现,应进行进一步的调查。
排除PCD诊断
工作组未达成共识(80%),即任何单一检查或检查组合都可以排除PCD诊断。然而,根据审查的证据,他们一致认为,在某些情况下,诊断“极不可能”。如果临床怀疑仅为中度,细胞培养后nNO高/正常+正常HSVA或nNO高/正常+正常HSVA。
可以告知患者诊断极不可能,不需要进一步检查。如临床怀疑程度很高(如。Kartagener综合征,PICADAR评分≥10)目前的诊断测试还不足以准确排除诊断。
一般的语句
工作队成员建议,诊断检测只能在具有该领域专门知识的实验室进行。结果应由具有PCD专业知识的专家解释,并向患者及其非专业护理人员解释结果。PCD的诊断测试目前还不完善。随着我们对PCD的理解和技术的进步,临床怀疑高或检测结果不确定的患者可以被召回并进行重复检测。
一些患者的诊断测试不符合标记为阳性、极有可能或极不可能的标准。这些患者应被认为是不确定的;进一步的调查和处理应由具有PCD专业知识的专家决定。
诊断算法
基于GRADE建议和德尔菲共识声明的证据,可以使用以下逐步诊断测试方法(图4).并非所有患者都需要接受所有步骤。对于许多患者,第一步(nNO和HSVA)将提供“极不可能”的诊断,患者不需要进一步的调查。部分患者应进行第2步(TEM或重复HSVA细胞培养)。基因检测(步骤3)可能有助于在其他检测未能提供明确诊断结果的患者中做出诊断。仍“不确定”的患者可能会在未来进行进一步的测试时被召回。这种方法并不适用于所有诊断服务;应考虑到当地的专门知识和设备。
第一步:nNO和HSVA
如果两者都完全正常,PCD的诊断是非常不可能的,可以避免进一步的检测,除非临床怀疑特别高。如果nNO低和/或HSVA异常,PCD是可能的诊断。重复第1步测试,然后执行第2步。
2 .透射电镜
如果TEM正常,则考虑对与正常或轻微TEM缺陷相关的基因进行遗传检测,并在细胞培养后重复HSVA。如果TEM显示PCD确认为“标志性”缺陷,则考虑进行基因检测以进一步表征潜在缺陷。
步骤3:遗传学和重复HSVA±细胞培养。
进一步的测试
对于诊断极有可能或仍不确定的患者,可能会使用免疫荧光或放射性气溶胶粘液纤毛清除分析等进一步的调查,但证据太有限,我们不推荐它们。随着PCD诊断技术的进步,PCD临床医生应考虑在未来召回这些患者进行进一步检测。
讨论
ERS工作组提出了第一个基于证据的PCD诊断指南。这是及时的,因为新的诊断测试(如。睫状蛋白免疫荧光和基因检测)随着现有检测方法的改进(如。电子显微镜断层扫描和计算平均)。随着新的证据的出现,指南将需要重新审视。我们已经就谁应该被推荐进行诊断检测提供了指导。我们已经证实,没有任何诊断测试是完美的,在没有黄金标准的情况下,有必要进行综合测试。然后,我们使用改进的德尔菲方法,使用个别测试的证据来开发诊断算法,提供将患者定义为阳性、极不可能、极不可能和不确定的标准。
有助于建议的研究都是在PCD专业诊断中心进行的。这些测试通常很复杂,需要有经验的科学家和临床医生来分析和解释结果。因此,我们的发现为具有高样本吞吐量、由经验丰富的技术人员分析和良好质量控制的诊断中心提供了证据。新的诊断中心将需要有经验的中心支持培训和持续的质量控制/评估。Beatpcd(成本行动bm 1407;www.beatpcd.org/)正协调一项研究和培训计划,以改善PCD的诊断和治疗。这包括提供培训学校,为在专家中心短期实习提供奖学金,以及建立讨论困难和模棱两可的诊断决定的网络。与预期的PCD欧洲参考网络一起,这一协作方法将提高整个欧洲的诊断检测标准。
诊断研究的结果是测试应用的下游后果的间接测量,因此对测试准确性测量的置信度充其量被判断为中等到低。来自患者的证据不会改变已发表证据的强度,但在决定推荐的强度时予以考虑。专责小组对来自25个国家的352名PCD患者进行了问卷调查,并进行了20次深入访谈[7].患者告诉我们,准确的诊断是一个重要的结果,可以使医生更好地认识到他们的问题,并获得有效的治疗,从而改善他们的健康和生活质量。
一旦工作组的建议得到同意,就使用修改后的德尔菲调查来就诊断方法达成共识。工作队的专家一致认为,透射电镜和基因检测的结果可导致明确的阳性诊断。这为未来的临床试验和临床护理提供了指导,但需要注意的是,我们的定义将系统地排除纤毛超微结构正常、基因突变尚不清楚的PCD患者。此外,工作组的大多数成员(>50%)认为以下测试组合可以导致阳性诊断,但我们没有达成共识(定义为≥80%):在两次情况下,非常低的nNO加标记HSVA,细胞培养后非常低的nNO加标记HSVA(表S11)。我们还定义了PCD诊断可被认为是“极有可能”和诊断为“极不可能”的条件。鉴于目前的证据,不可能100%肯定地排除诊断,但我们已经确定了可以合理停止进一步检测的情况。我们预计,随着我们对PCD了解的增长,这种高度异质性疾病的新表型将被描述,这些表型可能无法被当前的诊断测试检测到。
所有有助于我们建议的研究都因缺乏调查单项检测准确性的金标准而受到阻碍。因此,我们接受了从一些测试(综合诊断结果)构建参考标准或使用不完美测试的手稿,如。TEM作为替代品[118].使用TEM或遗传学作为参考标准的研究将系统地排除超微结构正常或基因突变未知的PCD患者。此外,一些证据是基于在综合诊断决策中包含指数测试的研究。这些重要的局限性表现出强烈的偏倚风险,并可能过度夸大或缩小我们报告的每个测试的敏感性和特异性。所有诊断测试都没有国际商定的行为或报告标准。这导致了我们回顾的研究之间的方法差异。工作队建议,为了增进我们对PCD诊断测试的理解,需要考虑以下问题。
1)方法学家应参与未来研究的设计,以调查测试的诊断准确性。由于缺乏完善的参考标准,需要考虑。
2)为了在研究之间进行比较,需要制定进行诊断试验和报告结果的国际标准。这些标准应该以证据为基础。
3)改进和规范纳入诊断研究的患者的临床表型报告。
4)应调查诊断对患者预后和生活质量的影响。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充的方法erj - 01090 - 2016 - _guideline_supplement
幻灯片工具包ERS_PCD_Slide_set
披露的信息
补充材料
分子量是利erj - 01090 - 2016 - _leigh
卢卡斯J.S.二erj - 01090 - 2016 - _lucas
b . Rindlisbachererj - 01090 - 2016 - _rindlisbacher
确认
工作组成员也是BEAT-PCD (COST Action BM 1407)的参与者。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
这些指南于2016年9月由ERS科学理事会和执行委员会批准。
由欧洲呼吸学会(ERS)发布的指南纳入了对当时最新研究的全面和系188bet官网地址统的文献综述中获得的数据。鼓励卫生专业人员在临床实践中考虑这些指南。然而,本指南发布的建议可能并不适用于所有情况。卫生专业人员的个人责任是咨询其他相关信息来源,根据每个患者的健康状况作出适当和准确的决定,并在适当和/或必要时与该患者和患者的护理人员协商,并在处方时核实适用于药物和器械的规则和条例。
支持声明:J.S. Lucas、K.G. Nielsen、C.E Kuehni、C. Hogg、M.W Leigh和H. Omran根据赠款协议n8305404 (BESTCILIA)获得了欧盟第七框架计划(FP7/2007-2013)的资助。J.S. Lucas, L. Behan, W.T. Walker和S.A. Collins得到了南安普顿大学医院NHS基金会信托(南安普顿,英国)和AAIR慈善机构的NIHR呼吸生物医学研究部门的支持。A. Bush是NIHR高级研究员,并得到了皇家布朗普顿和海尔菲尔德NHS基金会信托基金和伦敦帝国理工学院(均位于英国伦敦)NIHR呼吸疾病生物医学研究部门的支持。M. Goutaki得到了以下国家赠款的支持:伯尔尼肺联盟、Milena- Pro Kartagener基金会和瑞士国家基金会32003B_162820/1。S. Dell和M.W. Leigh通过粘液纤毛清除遗传疾病联盟获得了NIH (U54HL096458)的资助,这是国家推进转化科学中心的NIH罕见疾病研究办公室和国家心脏、肺和血液研究所的一项倡议。
利益冲突:D. Rigau和T. Tonia是急诊室的雇员。其他信息可以在本文旁边找到www.qdcxjkg.com
- 收到了2016年5月31日。
- 接受2016年8月25日。
- 版权所有©ERS 2017