摘要
吸烟者和慢性阻塞性肺病患者气道中ACE-2的表达增加,ACE-2是COVID-19病毒的入口受体。这可能解释了在这些亚人群中发生严重COVID-19的风险增加,并突显了戒烟的重要性。https://bit.ly/3bC29es
致编辑:
世界卫生组织(世卫组织)已宣布2019冠状病毒病(COVID-19)为大流行[1].COVID-19是由严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)引起的。COVID-19的症状从轻微到严重(肺炎),可能导致一些人死亡[2- - - - - -4].截至2020年4月18日,全球已有2 280945例COVID-19病例,156 354例死亡[5].SARS-CoV-2使用血管紧张素转换酶II (ACE-2)作为细胞进入受体[6].尽管该病毒可感染任何年龄的个体,但迄今为止,大多数严重病例都发生在55岁的人群中,并伴有严重的共病,如慢性阻塞性肺病[7].在这里,我们确定COPD患者下呼吸道支气管上皮细胞中ACE-2的表达是否增加。
为临床目的在圣保罗医院(温哥华,卑诗省,加拿大)接受支气管镜检查的患者入选。该方案得到了英属哥伦比亚大学/普罗维登斯卫生保健伦理委员会(UBC/PHC REB H15-02166)的批准。所有患者均要求≥19岁,并根据国际指南进行肺量测定[8].慢性阻塞性肺病患者被定义为经委员会认证的呼吸科医生临床诊断为慢性阻塞性肺病,用力呼气量为1 s (FEV)1)/用力肺活量(FVC) <70%或视觉检查时计算机断层成像有明显肺气肿证据。细胞学刷取肺亚节段气道(第6 - 8代),不受患者支气管镜检查的潜在临床指征影响。
使用RNeasy Mini Kit (Qiagen, Hilden, Germany)从细胞学刷取总RNA。在NovaSeq 6000 (Illumina, San Diego, CA, USA)上进行转录组测序,测序深度为5500万次。原始测序读数用FastQC进行质量控制[9]并使用STAR(拼接转录本对齐到参考)对齐到GENCODE(版本31)GRCh37基因组参考[10].对齐后,使用RSEM(期望最大化RNA-seq)对数据进行量化,以获得读取计数。Limma voom [11]用于将计数归一化到log2次/百万(CPM)读取,这用于下游分析。
使用了两个队列进行验证,详细情况见以前的出版物[12].首先,我们使用从单个中心收集的第10 - 12代支气管刷取的16个数据集;使用U133 Plus 2.0 (ThermoFisher, Waltham, MA, USA)微阵列(称为Cornell队列)进行转录组测量[13].其次,我们使用数据集GSE37147,其中包括来自第6代至第8代气道的支气管刷,其基因表达谱由genchip Human gene 1.0 ST微阵列(ThermoFisher)生成[14].该数据集被命名为不列颠哥伦比亚癌症机构(BCCA)队列。
我们还测定了切除肺组织标本中ACE-2蛋白的表达。这些样本来自10例慢性阻塞性肺病(mean±sdFEV1/FVC 61±7%),9例非吸烟对照组(FEV1/FVC 85±2%)1/ FVC 78±6%)。作为James Hogg肺注册(UBC/PHC REB协议H00-50110)的一部分,在知情同意的情况下,从接受胸外科手术的患者中获得人类肺组织样本。福尔马林固定的石蜡包埋的人肺组织用ACE-2抗体(Ab15348;Abcam,剑桥,英国)在徕卡邦德自动染色机上使用邦德聚合物精制红色检测试剂盒(均为徕卡生物系统,康科德,on,加拿大),如上所述[15].使用Aperio成像系统(徕卡生物系统)对气道上皮特异性ACE-2蛋白强度进行量化,归一化为基底膜的长度。
对于主要研究人群,ACE-2的CPM为log2。采用稳健线性模型确定:1)调整年龄和性别后,ACE-2在COPD患者和吸烟者中的表达是否存在差异;2) ACE-2表达与肺功能是否存在显著相关性。所有分析均在R(版本3.5.0;https://cran.r-project.org).在免疫组化数据集中,采用了Kruskal-Wallis和Dunn多重比较试验。连续数据用平均值±表示sd,除非另有说明。
圣保罗医院队列的平均年龄为64.8±12.0岁;其中55%为女性,24%为吸烟者。与对照组(n=21)相比,COPD组(n=21) FEV较低1%预测(72.0±15.6)与85.9±17.9% pred;p=0.011)和FEV1/ FVC(64.1±7.9与76.3±5.9%;2.621×10−6).大多数(79%)接受支气管镜检查以检查肺结节,其次是慢性咳嗽(7%)和淋巴结病(7%)。COPD中上皮细胞中ACE-2表达明显增加与非COPD受试者(COPD 2.52±0.66与non-COPD 1.70±0.51;p = 7.62×10−4;图1一个).ACE-2基因表达与FEV呈显著负相关1% pred (r=−0.24;p = 0.035;图1 b).有趣的是,吸烟状况也与受试者气道中ACE-2基因表达水平显著相关,吸烟者的基因表达水平显著高于不吸烟者(吸烟者为2.77±0.91)与不吸烟者1.78±0.39;p = 0.024)。前吸烟者的基因表达水平介于从不吸烟者和现吸烟者之间(前吸烟者为2.00±1.23;图1 c).调整吸烟状态后,ACE-2表达与COPD之间的相关性仍然显著(调整后的平均值±se非copd 0.90±0.65与慢性阻塞性肺病1.75±0.82;p = 0.016)。
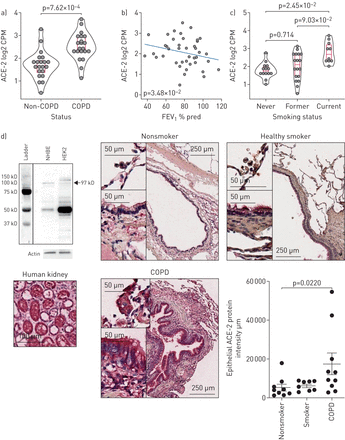
a)在圣保罗医院(温哥华,BC,加拿大)队列中COPD和非COPD患者小气道中血管紧张素转换酶II (ACE-2)表达的小提琴图。红框表示中位数和四分位之间的范围。p值是用一个稳健的线性模型得到的。b)根据1 s用力呼气量(FEV)绘制的小气道ACE-2表达散点图1%在圣保罗医院队列中预测。ACE-2基因在气道上皮细胞中的表达与FEV呈负相关1% pred (p=0.0348)。c)圣保罗医院队列中从不吸烟、曾经吸烟和现在吸烟的人的小气道中ACE-2表达的小提琴图。红框表示中位数和四分位间范围。p值是用一个稳健的线性模型得到的。d) COPD患者和非COPD患者气道中ACE-2蛋白的染色。ACE-2阳性对照为人肾载片。以HEK2细胞裂解物作为阳性对照,用免疫印迹法测定抗ACE-2抗体的特异性。ACE-2的预期分子量为90-100 kDa。在气道中,大部分蛋白表达在上皮层,在COPD患者中最明显。CPM:每百万分数; NHBE: normal human bronchial epithelial cells.
接下来,我们验证了上述发现:1)康奈尔队列(n=211);2) BCCA队列(n=238)。Cornell队列的平均年龄为43.6±10.5岁;其中33.2%为女性。32.2%的人从不吸烟,67.8%的人在支气管镜检查时正在吸烟。BCCA队列的平均年龄为64.5±5.9岁;43.3%的队列为女性。所有人都是重度吸烟者,吸烟≥30包年。其中41.6%在支气管镜检查时为吸烟者,其余为前吸烟者。
在康奈尔和BCCA队列中,与不吸烟者相比,当前吸烟者气道中ACE-2基因表达水平增加(在康奈尔队列中,当前吸烟者为4.34±0.45)与从不吸烟4.15±0.36;p = 1.92×10−3)和前吸烟者(在BCCA队列中,现吸烟者为6.05±0.53与戒烟者5.57±0.37;p < 2×10−16).在BCCA队列中,支气管扩张剂前FEV1与ACE-2基因表达水平显著相关(r=−0.10;p = 0.037)。
非吸烟者、健康吸烟者和慢性阻塞性肺病患者中上皮特异性ACE-2蛋白表达的代表性图像见图1 d.与不吸烟者相比,慢性阻塞性肺病患者人小气道上皮细胞ACE-2表达显著增加,但在健康吸烟者中没有(图1 d).ACE-2蛋白染色主要局限于气道上皮细胞和粘膜下隔室细胞。
2019冠状病毒病在全球范围内暴发。尽管大多数感染和诊断为COVID-19的患者症状较轻,但约20%的患者表现出严重或危重疾病,包括肺炎、呼吸衰竭、感染性休克和多器官衰竭的症状和体征。估计病死率为1-2% [2,3.].重要的是,几乎所有的死亡都发生在患有严重潜在慢性疾病的人群中,包括慢性阻塞性肺病和心血管疾病[4].这其中的原因在很大程度上是未知的。
一种可能是ACE-2的差异表达,它是SARS-CoV-2进入宿主粘膜并引起活动性感染的主要受体。在本研究中,我们研究了COPD患者和非COPD患者气道中ACE-2的基因表达水平,发现COPD和当前吸烟者的ACE-2表达显著增加。重要的是,ACE-2基因表达水平与个体FEV呈负相关1这表明这是一种剂量依赖性反应。这些发现在三个不同的队列中被观察到,表明它们的普遍性和稳健性。
ACE-2是一种I型跨膜金属羧基肽酶,与ACE同源。与将血管紧张素I转化为活性血管收缩素II的ACE不同,ACE-2将血管紧张素II分解为其代谢物,包括血管紧张素-(1-9)和血管紧张素-(1-7),这是一种有效的血管扩张剂,因此可能是肾素-血管紧张素系统的负调控因子[16].ACE-2在多种不同的组织中表达,包括上、下呼吸道、心肌和胃肠道黏膜[17].虽然它在人类健康和疾病中的作用尚未完全阐明,但它似乎在血压和心脏功能方面具有重要的调节作用。ACE-2在气道中的生理作用在很大程度上是未知的。然而,在小鼠中,ACE-2已被证明可以保护动物免受与误吸和败血症相关的严重肺损伤[18].
据我们所知,我们的研究首次证明了ACE-2在当前(但不是以前)吸烟者和COPD患者气道中的表达增加。这些结果也与先前对小动物的观察结果一致,即暴露于烟雾中可上调呼吸道中ACE-2的表达和活性[19,20.].虽然ACE-2的上调可能有助于保护宿主免受急性肺损伤,但长期而言,这可能使个体更易增加冠状病毒感染的风险,冠状病毒利用该受体进入上皮细胞。这可能在一定程度上解释了活跃吸烟者病毒呼吸道感染和慢性阻塞性肺疾病患者病毒相关加重的风险增加。
这项研究也有局限性。首先,这项研究是横断性的,因此,我们无法确定吸入皮质类固醇或支气管扩张剂(对COPD患者)等干预措施是否可以调节气道中的ACE-2基因表达。其次,由于受体表达是控制个人感染风险的众多宿主因素之一,吸烟和慢性阻塞性肺病造成的确切归因风险(对于冠状病毒感染)尚不确定。第三,尽管气道上皮细胞是COVID-19的主要入口,但病毒可以通过包括胃肠道粘膜在内的其他端口进入宿主,本研究未对这一点进行评估。第四,我们没有接触到上呼吸道组织,上呼吸道组织也可能感染SARS-CoV-2。
总之,主动吸烟和慢性阻塞性肺病上调了下气道ACE-2的表达,这在一定程度上可能解释了这些人群中严重COVID-19风险的增加。这些发现强调了戒烟对这些人的重要性,并加强对这些风险亚群体的监测,以预防和快速诊断这一潜在致命疾病。
可共享的PDF
脚注
数据可用性:作者可根据要求提供原始数据。数据也发布在GEO(基因表达综合)上。
利益冲突:梁振英没什么可透露的。
利益冲突:c.x.y Yang没有什么可透露的。
利益冲突:A. Tam没有什么可透露的。
利益冲突:t·沙帕尼奇没有什么可透露的。
利益冲突,t·l·哈克特没什么可透露的。
利益冲突:G.K.辛格拉没有什么可透露的。
利益冲突,多希德博士没什么可透露的。
利益冲突:D.D. Sin报告了来自默克的拨款,来自赛诺菲-安万特和Regeneron顾问委员会工作的个人费用,来自勃林格殷格翰的研究拨款和个人费用,来自阿斯利康的顾问委员会工作和讲座的拨款和个人费用,来自诺华的顾问委员会工作和讲座的个人费用,在提交的工作之外。
支持声明:这项工作得到了加拿大卫生研究院、不列颠哥伦比亚省肺脏协会和HLI de Lazzari家族主席的支持。梁建明博士获得了迈克尔·史密斯健康研究基金会(MSFHR)/普罗维登斯医疗保健健康专业调查员奖(HPI)和加拿大健康研究所(CIHR)/阿斯利康早期职业调查员奖的支持。T-L。Hackett获得了MSFHR学者和CIHR早期职业研究者奖的支持。D. Dorscheid由MSFHR/PHC HPI奖支持。D.D. Sin是加拿大COPD一级研究主席(CRC)和HLI de Lazzari家族主席。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2020年3月2日。
- 接受2020年3月25日。
- 版权所有©ERS 2020
本版本按照创作共用署名非商业性许可4.0的条款发布。