摘要
在大多数发达国家,约25%的成人哮喘患者目前是吸烟者。哮喘和频繁吸烟相互作用可导致更严重的症状,加速肺功能下降,并损害对皮质类固醇的短期治疗反应。
吸烟可能会改善与哮喘相关的炎症,尽管关于患有哮喘的吸烟者的气道病理的发表数据有限。迄今为止,有证据表明,与患有哮喘的非吸烟者相比,吸烟者的炎症反应既增强又抑制。
哮喘吸烟者皮质类固醇耐药的机制尚不清楚,但可能是气道炎症细胞表型改变的结果(如。中性粒细胞增多或嗜酸性粒细胞减少),糖皮质激素受体-α -β比值的改变(如。糖皮质激素受体β的过表达,促炎转录因子的激活增加(如。核因子-κB)或组蛋白去乙酰化酶活性降低。
总之,应该尽一切努力鼓励吸烟的哮喘患者戒烟,尽管戒烟对扭转烟草烟雾对哮喘控制的不利影响、对皮质类固醇的治疗反应和气道病理的影响尚未完全阐明。对于无法戒烟的哮喘患者,需要对吸入糖皮质激素进行替代或额外的治疗。
在16世纪中期,沃尔特·罗利爵士将烟草引入英国,吸烟很快被推荐为各种医疗疾病的治疗方法,包括呼吸道疾病。曼陀罗烟叶及根(曼佗罗),其中含有抗胆碱能化合物,在17世纪首次被用于治疗哮喘1.吸烟“治疗”哮喘一直很流行,直到20世纪30年代肾上腺素被引入。在上世纪下半叶,人们日益认识到环境烟草烟雾对儿童和成人哮喘患者的有害影响,并注意到其对哮喘发展和加重发作的不利影响2- - - - - -5.最近,积极吸烟和哮喘之间的重要相互作用已被确定,包括对发病率的影响,对皮质类固醇的治疗反应和疾病的机制(图1)⇓)6.这篇综述总结了积极吸烟与哮喘之间临床联系的已发表数据,可能解释这些联系的生物学机制,以及治疗哮喘吸烟者的潜在药物。
吸烟的普遍程度
据世界卫生组织估计,全世界约有12.5亿吸烟者,其中约三分之二生活在发展中国家。在许多发达国家,至少四分之一的成年人吸烟。美国和英国男性吸烟率分别为26%和27%,女性吸烟率分别为21%和25%7,8.欧洲各国吸烟者的总比例各不相同,如。德国38%,法国30%,意大利29%,瑞典18%。在收入较低的国家和年轻人中,尤其是女性,吸烟的流行率较高8.总的来说,不发达国家的吸烟率要高得多。在英国,戒烟的男性占27%,女性占21%8.
关于成年哮喘患者吸烟率的信息少得多,但主动吸烟很常见,患病率与普通人群相似。目前美国和英国哮喘患者的吸烟率在17-35%之间9- - - - - -15.在美国,在急诊科就诊的成年人中,急性哮喘的发病率特别高12.另有一些成年哮喘患者以前是吸烟者,患病率为22%至43%9,10.因此,在大多数发达国家,至少有一半的成年哮喘患者可能是目前或以前的吸烟者。
吸烟者哮喘的发展
对一些人来说,主动吸烟与哮喘的发生有关16- - - - - -19,但并不是所有的研究20.,21.在无症状青少年中,6年期间哮喘样症状的发展与主动吸烟(优势比(OR)(95%置信区间(CI)(2.1(1.2-3.8))以及过敏性和支气管对乙酰胆碱的高反应性独立相关17.在一项对15813名成年人进行呼吸问卷筛查的随机人群样本的回顾性研究中,与从不吸烟的女性相比,吸烟者成年发作哮喘的发病率OR (95% CI)增加了1.6(1.1-2.2),但在男性中没有19.在非特应性个体中,吸烟与哮喘发病密切相关(5.7(1.7-19.2))。16,是老年人哮喘的危险因素(4.8 (2.3-10.1))18.的β2-肾上腺素能受体基因多态性,精氨酸-14基因型,与从不吸烟的甘氨酸-16纯合子相比,经常吸烟者哮喘风险增加(7.8 (2.07-29.5))22.
不同的哮喘表型可能与开始吸烟有关23.在一项与哮喘和吸烟相关的危险因素的研究中,开始吸烟前发生的哮喘与特异反应有关,而开始吸烟后发生的哮喘与一秒钟内用力呼气量(FEV)较低有关1)23.
临床特征
哮喘控制及严重程度
与从不吸烟的人相比,吸烟者哮喘的发病率和死亡率都有所增加。哮喘吸烟者有更严重的哮喘症状9,10在美国,救援药物的需求更大24与从不吸烟的人相比,健康状况指数更差11,24.吸烟可导致急性支气管收缩,尽管烟草烟雾并非对所有患者都是急性刺激物25.基线FEV1直接与吸入香烟烟雾的即时反应有关吗26这表明,肺功能较差的哮喘吸烟者可能特别容易受到烟草烟雾的急性影响。与非吸烟者相比,患有特应性哮喘的吸烟者对吸入腺苷的反应较弱,这可能指向气道炎症的差异27.
在高水平的环境臭氧污染后的几天里,哮喘严重的重度吸烟者更经常因哮喘加重而去急诊科就诊28.目前的吸烟率与急诊科出现哮喘严重加重的患者相似,无论症状是在3小时内出现还是在较慢的时间出现29.吸烟者哮喘住院率和住院治疗率增加11,30.尽管在年轻人中可能没有31.关于当前吸烟是否是导致近致命性哮喘或致命性哮喘的危险因素,目前尚无相互矛盾的证据13,32- - - - - -34.然而,吸烟者发生近致命哮喘发作后的6年死亡率高于非吸烟者,年龄调整OR (95% CI)为3.6(2-6.2)。35.
肺功能下降
吸烟和哮喘结合在一起会加速肺功能的衰退,其程度比单独的任何一个因素都要大15,36.哥本哈根城市心脏研究包括FEV的纵向测量1在15年期间,发现FEV的平均下降1在患有哮喘的吸烟者中比不吸烟者更严重36.FEV的年平均下降140-59岁的哮喘男性患者中,非吸烟者为33 mL (n=36),吸烟者为58 mL (n=150;p < 0.001)36.存在慢性粘液分泌亢进和吸烟与FEV的更大下降有关136.一项对4000名最初年龄在18-30岁之间的成年人的研究,通过连续的肺活量测量随访了10年,发现FEV下降1不吸烟者无哮喘(n= 2393)为8.5%,不吸烟者有哮喘(n=437)为10.1%,吸烟者无哮喘(n=514)为11.1%。哮喘合并吸烟≥15支·天−1(n=101)对肺功能下降有协同作用,导致FEV下降17.8%1超过10年15.
对皮质类固醇的治疗反应
国际哮喘管理指南强调吸入皮质类固醇是治疗慢性哮喘最有效的抗炎疗法37.这一建议的证据是基于临床研究,这些研究主要是在从不吸烟或曾经吸烟的哮喘患者中进行的。一些研究表明,皮质类固醇的功效在积极吸烟的哮喘患者中是降低的38- - - - - -41虽然这一结论在另一项研究中没有得到支持42.”,Kerstjens等.38报道了一项针对轻度至中度重度阻塞性气道疾病(哮喘和慢性阻塞性肺疾病(COPD))患者的随机对照试验的结果,该试验旨在确定预测吸入糖皮质激素治疗反应的因素。当前吸烟史预示FEV受损1吸入倍氯米松800µg反应q.d。与不吸烟的人相比,3个月时的剂量为382毫升。然而,目前尚不清楚是否哮喘吸烟者、COPD患者或两组患者都对吸入糖皮质激素有耐药性。一个事后一项旨在研究吸入布地奈德(400µg)长期疗效的随机临床试验分析q.d。或1,600µgq.d。)或茶碱(600毫克)q.d。)对哮喘患者炎症和肺功能的血液标志物的研究指出,吸入布地奈德的疗效在不吸烟的哮喘患者中存在,但在吸烟的哮喘患者中不存在39.即使在吸入高剂量布地奈德9个月后,吸烟者的肺功能或嗜酸性粒细胞标志物也没有改善。
吸入丙酸氟替卡松(1000µgq.d。)或安慰剂,为期3周,在corticosteroid-naïve成年哮喘患者中进行了随机安慰剂对照交叉研究40.所有受试者均有支气管高反应性哮喘。非吸烟者平均晨峰呼气流量(PEF;图2⇓),表示FEV1几何平均刺激浓度导致FEV下降20%1(电脑20.),氟替卡松与安慰剂相比,痰嗜酸性粒细胞显著减少。这些结果指标显示吸烟哮喘患者无显著变化。吸入丙酸氟替卡松(2000µg)的随机平行组研究q.d。)或安慰剂,为期6周,研究了52 treatment-naïve成年哮喘患者对methacholine的气道反应性的影响,其中约一半是目前的吸烟者42.吸入氟替卡松可降低几何平均PC20.与安慰剂相比(1.9倍PC20.).多元线性回归分析显示,当前吸烟不影响吸入氟替卡松对PC的影响程度20.醋甲胆碱。
长期稳定的哮喘吸烟者短期口服皮质类固醇治疗的疗效受损41.泼尼松龙40mg的效果q.d。在哮喘吸烟者、戒烟者和从不吸烟者的随机对照交叉试验中研究了2周的安慰剂。所有受试者都有临床哮喘,有证据表明FEV具有可逆性1吸入沙丁胺醇≥15%,支气管扩张剂后平均FEV1%预测>80%。与安慰剂相比,口服强的松龙对FEV有显著改善1哮喘从不吸烟者的早晨PEF和哮喘控制评分,但哮喘吸烟者没有变化(图3)⇓).目前吸烟是吸入或口服皮质类固醇治疗反应受损的一个预测因素,可以通过FEV的改善进行评估1,但不改变PC20.或哮喘生活质量在轻度不稳定哮喘43.有趣的是,在COPD患者中,当前吸烟是与FEV变化降低最密切相关的因素1强的松后44.
综上所述,这些临床研究的结果表明,患有哮喘的吸烟者可能对皮质类固醇的有益治疗效果产生耐药性。有几个临床因素可能会影响哮喘吸烟者对皮质类固醇的反应。这些包括:
诊断
吸烟是慢性阻塞性肺病发病的主要因素。在这些研究中,哮喘吸烟者有几个不同于COPD患者的临床特征40,41,因为他们比通常与症状性COPD相关的受试者更年轻40,41而且有长期的哮喘病史。此外,患者有甲基胆碱支气管高反应性的证据40或沙丁胺醇≥15%后可逆性41.
吸入皮质类固醇治疗的持续时间
治疗持续时间是否会影响吸入皮质类固醇的反应仍有待确定。Chalmers的短期随机对照研究等.40其中吸入氟替卡松3周,Pedersen进行了更长期的试验等.39在该研究中,吸烟者吸入布地奈德9个月,显示出皮质类固醇耐药。这些研究使用症状和肺功能来评估对药物治疗的反应,长期吸入皮质类固醇可能对其他临床终点(包括加重率)有有益的影响。
吸烟强度
先前关于哮喘吸烟者吸入糖皮质激素耐药性的研究招募了有中度重度吸烟史≥10年的个体40,41,45.目前尚不清楚,当吸烟史强度较低时,对皮质类固醇的反应是否也会降低。在一项研究报告中,当前吸烟不影响吸入氟替卡松对PC的影响程度20.的醋甲胆碱42在美国,哮喘患者每天至少吸5支烟,但没有提供更多有关吸烟史强度的细节。因此,皮质类固醇抵抗是否只发生在有中度至高度吸烟史的患者中,还是所有哮喘吸烟者的特征仍有待确定。
哮喘持续时间
目前尚不清楚最近患哮喘的吸烟者是否对皮质类固醇有耐药性。
吸烟者的茶碱代谢
吸烟通过诱导几种代谢酶来增加药物的清除46.细胞色素P450-1A2负责茶碱的代谢,与不吸烟者相比,吸烟者的清除率增加了60-100%。戒烟1周可使茶碱的消除减少35%。
耐心教育和自我管理
目前吸烟者不太可能使用适当的方法来控制急性和慢性哮喘47,48.一项针对在美国急诊科就诊的急性哮喘患者的研究发现,目前吸烟是缺乏哮喘知识和自我管理技能的一个预测因素48.英国一项基于社区的研究发现,患有慢性哮喘的吸烟者比不吸烟的人更不可能使用吸入糖皮质激素或峰值流量计,也不太可能在病情加重期间改变治疗方法47.患有哮喘的吸烟者不太可能参加哮喘教育项目49- - - - - -51.在一项针对125名成年哮喘患者的门诊研究中,只有4%的吸烟者完成了哮喘教育计划,而31%的戒烟者和65%的从不吸烟者完成了哮喘教育计划49.
戒烟
主动吸烟对哮喘的有害影响加强了戒烟的必要性,即使对那些病情轻微的人也是如此。然而,许多患有哮喘的成年吸烟者并不认为吸烟对他们个人有危险52.在一项对患有哮喘的长期吸烟者的研究中,戒烟的平均时间为17年53.预测较长时间戒烟的因素是教育水平低、吸烟强度高、过早开始吸烟和儿童晚期患哮喘53.在一般人群中,使用简短的机会主义建议、行为支持、尼古丁替代疗法或安非他酮的戒烟干预措施都是有效的,尽管每年只有少数吸烟者成功戒烟54.这些干预措施尚未在哮喘人群中进行专门研究,尽管其效果可能与当前吸烟者的一般人群相似。
非哮喘受试者戒烟可减少呼吸道症状,如咳嗽和咳痰,以及呼吸道感染的频率55,56.肺功能改善≤5%,肺功能下降率恢复到不吸烟者水平57.戒烟可能对患有哮喘的吸烟者产生类似的临床益处,尽管现有的数据有限。对27名当前吸烟者和27名戒烟者的横断面研究发现,后者的慢性咳嗽和痰量较低25;然而,在另一项研究中,一小部分吸烟者和患有哮喘的戒烟者之间的哮喘症状评分相似41.一项对59名停止吸烟的成年哮喘患者的研究报告称,18人(30.5%)抱怨症状恶化58.Fennerty等.59报告14例哮喘患者中有2例在戒烟24 h内症状加重,而7例中有4例在戒烟1周后症状减轻。吸烟对皮质类固醇反应性的影响可能是部分可逆的,因为与当前吸烟者不同,前吸烟者在口服皮质类固醇治疗后显示出早晨PEF值的改善41.
戒烟后,与从不吸烟的人相比,戒烟者发生自我报告哮喘的风险增加21,58,60,但在戒烟后随着时间的推移而减少21.这种影响被认为不是因果关系,而是由于个人将COPD症状归因于哮喘,或者由于吸烟者因出现呼吸道症状而停止吸烟,后来被诊断为哮喘21,60.
生物学机制
气道病理
吸烟可改善哮喘相关炎症;然而,关于主动吸烟对哮喘患者气道病理影响的数据有限。
炎症细胞表型
与非吸烟者相比,无气流阻塞的非哮喘吸烟者会诱发气道炎症61- - - - - -64.正常吸烟者t淋巴细胞增多,主要是CD8+细胞65气道壁内的巨噬细胞数量,支气管分泌物内的中性粒细胞数量较高61单核细胞和巨噬细胞浸润外周气道61.据报道,与非吸烟者相比,吸烟者的周围肺切片浸润粘膜下层的嗜酸性粒细胞数量增加66.
目前还没有发表关于哮喘吸烟者气道炎症组织学的研究,无论是通过支气管活检还是肺切除标本评估。与非吸烟者相比,轻度哮喘患者诱导痰嗜酸性粒细胞计数减少45.哮喘吸烟者痰中嗜酸性粒细胞计数减少的原因尚未阐明6,但可能是香烟烟雾中的外源性一氧化氮(NO)增加了活化嗜酸性粒细胞的凋亡67,68.据报道,与不吸烟的小鼠相比,短期暴露于烟草烟雾会降低卵清蛋白敏感小鼠对卵清蛋白的反应,并降低支气管肺泡灌洗(BAL)嗜酸性粒细胞和巨噬细胞数量69.烟草烟雾中的尼古丁可能通过抑制巨噬细胞释放促炎细胞因子,对嗜酸性粒细胞功能产生二次免疫调节作用70,71.然而,其他小鼠过敏模型的研究指出,暴露于烟草烟雾会增加支气管高反应性、嗜酸性粒细胞增多和过敏原刺激后的t辅助性(Th)2细胞因子反应72,73.与哮喘非吸烟者相比,有平均21包年吸烟史的轻度哮喘吸烟者诱导痰中性粒细胞计数升高45.
在正常吸烟者中升高的BAL细胞总数和肺泡巨噬细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞浓度在戒烟9个月内恢复正常74.然而,以前吸烟导致慢性阻塞性肺病患者戒烟后肺部持续炎症56,75,76.目前吸烟的COPD患者与曾经吸烟的COPD患者的诱导痰差异细胞计数和巨噬细胞表型相似76.目前和曾经患有慢性支气管炎的吸烟者的支气管活检显示炎症程度相似75.戒烟是否会像正常人一样减轻哮喘吸烟者的气道炎症,还是会像COPD患者那样持续减轻气道炎症,仍有待研究。
细胞因子和介质
哮喘吸烟者痰白细胞介素(IL)-8水平升高,其浓度与痰中中性粒细胞比例及吸烟史呈正相关,与FEV呈负相关1%的预测45.这些发现为哮喘吸烟者吸烟、气道炎症和肺功能下降之间的联系提供了间接证据。哮喘患者痰中嗜酸性蛋白(ECP)浓度在吸烟者和非吸烟者之间相似45.IL-18是一种参与th1淋巴细胞反应发展的细胞因子,可能通过抑制th2淋巴细胞反应在哮喘中起调节作用。与不吸烟者相比,吸烟与正常和哮喘患者IL-18水平的显著降低有关,并且这种影响在哮喘患者中比在正常人中更为明显77.与非吸烟者相比,哮喘吸烟者IL-18 mRNA表达降低。这些发现表明,吸烟可能在一定程度上通过改变Th1-/ th2细胞因子分泌的平衡来改善气道炎症。哮喘吸烟者在BAL样本中抗炎蛋白脂质-1的浓度高于非吸烟者哮喘患者78.作者推测,吸烟者体内脂质素-1的升高是一种抑制气道炎症的自我保护机制。
与患有哮喘的非吸烟者相比,轻度steroid-naïve哮喘吸烟者呼出的NO (eNO)水平降低79.卷烟烟雾可能通过抑制诱导NO合成酶而降低eNO,这可能是高浓度外源NO直接作用的结果68或者香烟烟雾中的一氧化碳与血红素蛋白相互作用80.在正常吸烟者中,戒烟后eNO水平升高81.氧化应激在哮喘、COPD和无气流阻塞的吸烟者中增强82,83.氧化负担的增加很可能是吸烟者哮喘的一个特征。在哮喘吸烟者中,神经源性炎症也可能导致气道炎症84.
气道重塑
哮喘吸烟者的气道重塑可能更为严重,因为与非吸烟者相比,吸烟者死于哮喘以外原因的哮喘患者的气道标本中气道纵向弹性纤维网络增加85.粘膜下弹性纤维面积的增加可改变气道壁的力学特性。使用高分辨率计算机断层扫描来评估肺部的结构变化86,87是否揭示了哮喘吸烟者中肺气肿的存在与较大的吸烟史有关88.与不吸烟的哮喘患者相比,有49包年重度吸烟史的哮喘戒烟者肺恶性膨胀或肺气肿改变增加89.
循环外周血细胞
与不吸烟的哮喘患者相比,吸烟伴哮喘患者外周血嗜酸性粒细胞计数减少90相反,在正常非哮喘患者中,当前吸烟与循环嗜酸性粒细胞计数增加有关91- - - - - -93.这些结果指出了哮喘吸烟者炎症细胞反应的改变,抑制了与哮喘相关的循环血液嗜酸性粒细胞计数的升高。循环血液中髓过氧化物酶和ECP浓度在哮喘吸烟者与哮喘非吸烟者和戒烟者之间是相似的39.白三烯B的生成4(LTB4吸烟的老年哮喘患者与不吸烟的哮喘患者相比,其外周血白细胞含量增加89.在一般人群中,当前吸烟与室内尘螨的特异性免疫球蛋白E抗体呈正相关94.因此,吸烟可能会影响哮喘患者对过敏原的免疫反应。
吸烟者哮喘的气道病理概述
综合这些研究的结果,与患有哮喘的非吸烟者相比,吸烟者的炎症反应似乎同时增强和抑制。例如,患有哮喘的吸烟者的诱导痰样本中嗜酸性粒细胞数量减少,而中性粒细胞数量增加。一些细胞因子的浓度,如IL-8,会因吸烟而升高,而其他的,如IL-18,则会受到抑制。目前尚不清楚这些细胞数量和细胞因子浓度的变化在吸烟者哮喘症状加重的发病机制中是否重要。另外,这些变化可能反映了吸烟史的持续时间和强度,但可能与哮喘吸烟者的疾病机制没有直接关系。需要进一步使用侵入性和非侵入性技术进行研究,以评估哮喘吸烟者与哮喘非吸烟者和COPD患者气道的细胞和结构变化。特别重要的是,确定哮喘吸烟者的气道病理主要是哮喘非吸烟者、COPD,还是这两种情况的组合。
哮喘吸烟者皮质类固醇抵抗的机制
糖皮质激素的抗炎作用是由作为配体激活转录因子的细胞质糖皮质激素受体(GRs)的激活介导的,这些受体通过直接结合DNA序列(转激活)或与促炎转录因子相互作用(转抑制)转位到细胞核中抑制或诱导糖皮质激素靶基因。95- - - - - -97.在哮喘非吸烟者和其他疾病(包括炎症性肠病和类风湿性关节炎)中,各种机制涉及皮质类固醇抵抗95- - - - - -99.哮喘吸烟者皮质类固醇抵抗的潜在机制在很大程度上尚未研究,但可能包括一个或多个与哮喘非吸烟者和其他炎症性疾病有关的途径(图4)⇓;表1⇓).
皮质类固醇药物动力学
气道粘膜通透性在活的有机体内是否在肺功能正常的吸烟者中增加One hundred.不吸烟的哮喘患者与正常人相比101.目前尚不清楚吸烟和哮喘对气道渗透性是否有附加作用或协同作用,如果是这样,与哮喘非吸烟者相比,哮喘吸烟者是否可能有更高的气道吸入皮质类固醇的清除。吸烟引起慢性粘液分泌亢进的两种正常情况102还有哮喘吸烟者36.与不吸烟的哮喘患者相比,哮喘吸烟者气道内过多的粘液会损害吸入的皮质类固醇对气道内靶细胞上GRs的通路。然而,其他机制必须起作用,因为没有慢性粘液分泌亢进症状的哮喘吸烟者对吸入皮质类固醇的治疗反应降低40.此外,皮质类固醇对口服强的松龙的抵抗不太可能受到过多气道粘液或气道粘膜通透性增加的影响41.吸烟对哮喘患者口服皮质类固醇清除的影响尚不清楚,但很可能是正常的,因为吸烟不会改变健康成年男性体内强的松、强的松和地塞米松的药代动力学46,103.
皮质类固醇和β2-肾上腺素能受体相互作用
据报道,长期吸烟会降低β的密度2淋巴细胞上的-肾上腺素能受体减少配体与β的结合2-肾上腺素能受体,损害环磷酸腺苷的形成104.这些影响在戒烟8周后是可逆的104,105.吸烟诱导β下调程度2-肾上腺素能受体可能因人而异,取决于他们的β类型2-肾上腺素能受体多态性22.β2-激动剂可能通过增加GRs的核定位而增强皮质类固醇的作用106.因此,在哮喘吸烟者中,β的下调2-肾上腺素能受体功能可能不仅损害临床对β的反应2-激动剂,还有皮质类固醇的有益作用。
炎症细胞表型
香烟烟雾会改变气道炎症细胞的数量和功能107,108.与不吸烟的哮喘患者相比,吸烟多年的哮喘患者痰中嗜酸性粒细胞数量减少40,45可能会导致吸烟者对皮质类固醇的反应受损。另一种可能是,患有哮喘的吸烟者的痰中性粒细胞计数升高可能对皮质类固醇治疗反应不佳109.然而,关于皮质类固醇对哮喘中性粒细胞性炎症的影响,有相互矛盾的数据110.与皮质激素敏感性哮喘患者相比,皮质激素对外周血单个核细胞t淋巴细胞增殖的抑制作用受损111.肺功能正常的吸烟者BAL液中CD8+ t淋巴细胞数量增加,与吸烟包数呈正相关112.如果哮喘吸烟者气道CD8+淋巴细胞数量或活性增加,这些细胞可能有助于皮质类固醇耐药,因为在COPD中也发现CD8+淋巴细胞升高113这种疾病对皮质类固醇的反应很差。
细胞因子和炎症介质
也可以暴露在香烟烟雾中在体外或在活的有机体内,增加了包括IL-4在内的促炎细胞因子的产生114,引发115肿瘤坏死因子(TNF -α)115,116.这些细胞因子与皮质类固醇耐药有关,尽管其确切机制尚不确定。当加入t淋巴细胞时,IL-2和IL-4的组合在体外,会导致对皮质类固醇的反应降低117.TNF-α可引起人类单个核细胞的皮质类固醇耐药离体的,可能通过激活核因子-κB (NF-κB)118.
皮质激素诱导的t淋巴细胞合成抗炎细胞因子IL-10的缺陷与皮质激素耐药性哮喘有关119.与健康的非吸烟者相比,正常吸烟者痰中IL-10水平降低120.皮质类固醇诱导IL-10释放的能力受损在体外IL-2和IL-4的结合121.总的来说,这些结果表明,哮喘吸烟者t淋巴细胞产生IL-10的抑制可能导致皮质类固醇不敏感。
NO在烟草烟雾中浓度很高122,在体外,降低gr -配体的结合亲和力123.有研究表明,内源性产生的“亚硝化应激”可能导致哮喘皮质类固醇反应不良124由于烟草烟雾引起的外源性和内源性“亚硝化应激”的影响,类似的机制可能在哮喘吸烟者中起作用。
糖皮质激素受体数量或结合亲和力
GR有两种自然存在的亚型:GR-α具有功能性,GR-β不与配体结合,主要位于细胞核中,不能转激活糖皮质激素敏感基因。有研究表明,GR-β的过表达可能通过抑制配体激活GR-α的作用而损害对皮质类固醇的反应97,125- - - - - -128.另外,GR-α数量的减少也被认为是皮质类固醇抵抗的一种机制129.GR-β在各种类型的细胞中表达增加,暴露于促炎细胞因子和介质后,暴露于香烟烟雾中增加。在联合作用下,IL-2和IL-4,而不是单独的细胞因子,会增加t淋巴细胞GR-β的数量130.IL-8导致中性粒细胞增加GR-β的表达131这可能是这些细胞对皮质类固醇反应不良的原因。TNF-α在Helen Lake人宫颈癌S3细胞中不成比例地增加GR-β的表达132.gr结合亲和力的降低可能导致吸烟者的皮质类固醇耐药。吸烟者与非吸烟者培养的人支气管上皮细胞具有较低结合亲和力的GRs,尽管结合位点的数量没有差异133.IL-2和IL-4联合作用可降低外周血单个核细胞中gr配体的结合亲和力117,121,在小鼠成纤维细胞中被NO激活123和IL-13在外周血单核细胞中的作用111.尚不清楚GR-α与-β比值的改变或GR-结合亲和力是否有助于吸烟者的皮质类固醇耐药。
促炎转录因子激活
香烟烟雾中可能含有多种成分,包括细菌脂多糖(LPS),可能激活NF-κB134.NF-κB与多种炎症因子的诱导有关,包括TNF-α和IL-8。与不吸烟者相比,肺功能正常的吸烟者的p65表达增加,p65是支气管上皮NF-κB的主要亚基135.GRs可阻断NF-κB信号通路,但相反,NF-κB可通过磷酸化GR抑制GR-α功能,并抑制GR与DNA结合的能力96.NF-κB与克罗恩病皮质类固醇无反应性相关136在哮喘吸烟者中可能存在类似的机制,GR-α功能与NF-κB活性升高之间的不平衡相互作用导致皮质类固醇抵抗。可能其他促炎转录因子,包括激活蛋白-1和信号转导激活转录因子,在吸烟者的细胞中过表达137这些可能有助于哮喘吸烟者对皮质类固醇的抵抗。
治疗吸烟者哮喘的潜在药物
对于无法戒烟或戒烟后症状持续的哮喘患者,可能需要对吸入糖皮质激素进行替代或额外治疗。目前还没有发表的非皮质类固醇治疗哮喘吸烟者的临床试验,但一些目前已获许可的药物以及正在开发的新药可能对这组患者有效(表2)⇓).
长效β的结合2受体激动剂和吸入皮质类固醇在治疗哮喘和COPD(在较小程度上)方面非常有效142,143.这两种药物可能相互作用,以加强抑制炎症相关的两种情况106,144.因此,这些药物的组合可能对治疗哮喘吸烟者有益。低剂量茶碱激活HDAC,由皮质类固醇招募以抑制炎症145.茶碱逆转了香烟烟雾对HDAC的抑制作用在体外146,因此,有可能恢复吸烟哮喘患者的皮质类固醇敏感性。选择性磷酸二酯酶-4抑制剂,如西洛咪司特和罗氟咪司特在COPD治疗中的疗效147它们对中性粒细胞功能的抑制作用表明,这些化合物可能对哮喘吸烟者有效。
目前正在开发的一些选择性GR激动剂具有更强的效力在体外引起炎症基因转抑制的作用,而不是基因的转激活,这与皮质激素诱导的副作用更相关148.这些化合物的解离性使它们不太可能引起不良反应,但这些性质是否会影响它们在皮质类固醇耐药存在时的疗效尚不清楚。
吸烟导致尿中半胱氨酸白三烯E的剂量相关增加4生产149,健康吸烟者气道中15-脂氧合酶亚型活性增加150.这些发现可能指向白三烯受体拮抗剂在哮喘吸烟者中的作用。Histamine-H1受体拮抗剂,如西替利嗪和氮elastine,减弱NF-κB的活性151,通过这一作用可能抑制NF-κB对哮喘吸烟者糖皮质激素敏感性的潜在不良影响。初步结果表明,IL-2受体阻断可以诱导皮质类固醇抵抗性溃疡性结肠炎的缓解152.阻断其他介质作用的药物涉及香烟烟雾引起的气道炎症,如TNF-α, LTB4, IL-8,氧化剂,诱导NO和几种趋化因子,具有作为治疗吸烟者哮喘的抗哮喘药物的潜力148,153.
其他正在开发的抗炎疗法,用于治疗皮质类固醇抵抗性哮喘,可能对哮喘吸烟者的治疗有用。干扰素-α治疗改善了肺功能,也增加了皮质类固醇耐药哮喘患者的皮质类固醇敏感性154,155.皮质类固醇诱导的t淋巴细胞合成抗炎细胞因子IL-10的缺陷与皮质类固醇耐药性哮喘有关119IL-10激动剂可能是这组患者未来的治疗方法。p38 MAPK抑制剂可能在治疗皮质类固醇耐药哮喘中发挥作用,因为它和其他MAPK降低了皮质类固醇对GR的激活121,156.以抑制吸烟者激活的NF-κB为靶点的药物、阻止氧化应激的抗氧化剂或降低IL-8产生的大环内酯类抗生素可能在治疗吸烟相关气道疾病中有价值148,153.
未来研究方向
关于哮喘与吸烟之间的相互作用,仍有许多研究问题有待回答,包括以下问题。1)吸烟者的皮质类固醇耐药是一种全身性反应还是局限于肺部?2)哪些因素影响哮喘吸烟者对皮质类固醇的治疗反应,包括吸入皮质类固醇治疗的持续时间或剂量,用于评估疗效的结果,吸烟史的持续时间或强度,或哮喘的持续时间?3)系统性皮质类固醇治疗急性哮喘吸烟者有效吗?4)哮喘吸烟者的气道病理是什么?5)哮喘吸烟者皮质类固醇耐药的机制是什么?6)戒烟是否能改善哮喘控制和对皮质类固醇的治疗反应?7)对于无法戒烟或戒烟后症状持续的哮喘患者,吸入糖皮质激素的替代或额外治疗是否有效?
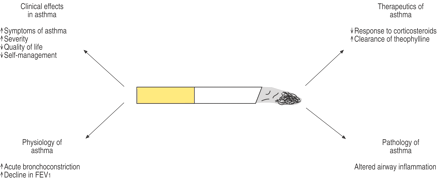
哮喘和吸烟之间的相互作用。FEV1: 1秒用力呼气量;↑:增加;↓:减少。

呼气流量峰值(PEF;L·敏−1)在吸入安慰剂(□)或丙酸氟替卡松治疗后,在非吸烟和吸烟哮喘患者中(点数点数;1000µg·−1).#:安慰剂后p=0.016,大于不吸烟者;***: p=0.001,大于服用氟替卡松后的吸烟者。转载须获授权40.
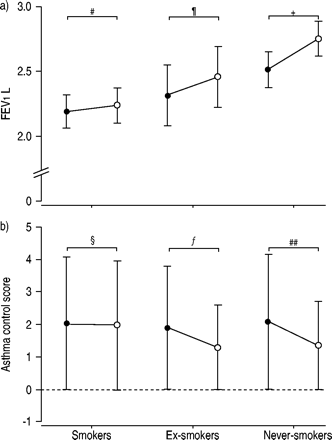
在患有哮喘的吸烟者、已戒烟的哮喘患者和从未吸烟的哮喘患者中,安慰剂(•)后和强的松龙(〇)后的平均差异(95%置信区间)为:1秒内用力呼气量的变化(FEV)1)和b)哮喘控制评分。分数的降低意味着哮喘控制的改善。#: p = 0.605;¶: p = 0.386;+: p = 0.019;§: p = 0.865;ƒ: p = 0.108;# #: p = 0.04。转载须获授权41.
糖皮质激素的抗炎作用是由作为配体激活的转录因子的细胞质糖皮质激素受体(GRs)的激活介导的,这些转录因子转位到细胞核中抑制或诱导糖皮质激素靶基因。GR-α通过直接与DNA序列结合(转激活)或与促炎转录因子相互作用(转抑制)起作用。GR-β不与配体结合,主要位于细胞核内,不能转激活糖皮质激素敏感基因。哮喘吸烟者皮质类固醇耐药的潜在途径和机制包括:1)皮质类固醇药代动力学;如。气道粘膜通透性增加,支气管分泌物增多;2)皮质类固醇和β2肾上腺素能受体(β2基于“增大化现实”技术)交互,如。β下调2基于“增大化现实”技术的功能;3)炎症细胞表型;如。气道中性粒细胞或CD8+淋巴细胞数量增加,气道嗜酸性粒细胞数量减少;4)细胞因子和介质水平;如。白细胞介素(IL)-4、IL-8、肿瘤坏死因子-α的产生增加,IL-10的产生减少,亚硝化应激增加;5) GRs,如。GR-β过表达,GR-α表达降低;6)促炎转录因子激活;如。核因子-κB (NF-κB)、激活蛋白-1、信号转导激活因子;7)皮质类固醇细胞信号系统如。降低组蛋白去乙酰化酶活性(HDAC),增加p38丝裂原活化蛋白激酶活性。HAT:组蛋白乙酰转移酶。
致谢
作者要感谢苏格兰国家卫生服务教育,首席科学家办公室和英国哮喘协会的支持。作者也要感谢K. McFall(英国格拉斯哥Gartnavel总医院医学插图系)的帮助。
脚注
↵编辑评论见第720页。
- 收到了2004年4月1日。
- 接受2004年7月6日。
- ©ERS期刊有限公司















