摘要
尽管特发性肺纤维化的急性加重已得到很好的认识,但没有研究记录其患病率或确定预先存在的危险因素。
本研究分析了147例活检证实的特发性肺纤维化患者中符合急性加重标准的11例患者的临床、放射和病理资料。另有5名患者具有相似的人口统计学、放射学和外科肺活检病理,但临床疾病较轻,因此未纳入研究。诊断后2年急性加重发生率为9.6%。大多数急性加重是特发性的,尽管有两例是在外科肺活检和支气管肺泡灌洗后出现的。
单因素比例危害分析未发现显著危险因素。影像学显示弥漫性双侧磨玻璃影叠加在胸膜下网状和蜂窝状密度上。4例急性加重期患者的活检显示弥漫性肺泡损伤叠加在通常的间质性肺炎之上。
本研究结果表明,特发性肺纤维化急性加重是相当常见的,这种加重可能有一个严重程度的频谱。
特发性肺纤维化(IPF)是一种病因不明的致命性肺纤维化疾病,其组织学特征为常见的间质性肺炎(UIP)。1- - - - - -5.虽然临床病程通常是慢性的,进展缓慢1- - - - - -5,有些病人在病程中病情迅速恶化。大多数关于IPF急性加重(AE)现象的报道出现在日本医学文献中6- - - - - -14.在英国医学文献中,Colby15和Kitaichi16首次报道AE的病理表现为弥漫性肺泡损伤(DAD)叠加在UIP上。Kondohet al。17描述了3例AE和后来的Akira患者的临床和病理资料et al。18报告了17例患者的放射学资料。最近,大米et al。19报道了12例IPF患者的DAD模式叠加在UIP上的尸检结果。安布罗西尼et al。20.最近还介绍了5例的临床和病理特征。然而,这一现象的临床特征尚不清楚,不同作者对AE的定义在严重程度和迅速程度上都有所不同。
11例符合Kondoh标准的患者的临床特征et al。17在作者的间质性肺疾病诊所(首尔峨山医疗中心,韩国)进行了复查;11人中有4人在AE发生时接受了手术肺活检(SLBx)。
研究对象与方法
研究设计与课题
这是一项回顾性描述性研究。共对147例患者进行了复查;根据美国胸科学会(ATS)/欧洲呼吸学会(ERS)共识分类,经SLBx诊断为IPF188bet官网地址211990年1月至2003年9月,他在韩国首尔的峨山医疗中心(一个拥有2000个床位的大学附属三级转诊中心)工作。在这147例患者中,有11例符合Kondoh提出的AE标准et al。17.所有患者均由首尔峨山医院IPF诊所的一名医生进行诊断和随访。大多数IPF患者已在肺生理学研究中进行过回顾22.
急性加重的标准
Kondoh的严格标准et al。17用来定义一个声发射事件。其中包括:1)1个月内呼吸困难加重;2)动脉氧张力/吸入性氧张力比值<225的低氧血症;3)胸片上新发现的肺浸润;4)无明显感染或心脏病。
方法
所有临床和实验室数据均从病历中回顾性收集。
肺功能检查
使用Sensor Medic 2100 (Yorba Linda, CA, USA)进行肺功能测定。用Sensor Medic Model Vmax 22测量弥散能力,用Sensor Medic Auto Box 6200测量肺容积。
高分辨率计算机断层成像
对所有患者进行高分辨率计算机断层扫描(HRCT),通常在入院当天,使用HiSpeed Advantage扫描仪(GE医疗系统公司,Milwaukee, WI, USA)或Somatom Plus 4扫描仪(西门子医疗系统公司,Erlangen, Germany)。这些图像在窗口水平为−700 HU和窗口宽度为1,500 HU的情况下进行分析。一位放射科医生(J.S. Lee)在不了解活检结果或临床结果的情况下回顾了肺的HRCT。声发射时的HRCT表现分为周围性、多灶性或弥漫性实质影18.
支气管肺泡灌洗
支气管肺泡灌洗(BAL)如先前报道23.
病理评价
活检切片由两位病理学家(A.G. Nicholson和T. Colby)独立复查,首先,根据ATS/ERS共识分类对慢性间质性肺炎(如果样本中存在)的背景组织学模式进行分类21,其次,以渗出性(带透明膜)或组织DAD的形式,确认是否存在叠加的急性改变。背景:出现慢性间质性肺炎时,根据之前描述的成纤维细胞病灶范围、间质单核细胞炎症、肺泡巨噬细胞积聚和已建立的纤维化的方案,使用0-6的半定量量表进行评分24.最终组织学诊断的共识观点再与HRCT及临床资料进行关联,以提供最终的临床病理诊断。
统计分析
数据以均数±表示sd对于连续变量,百分比用于分类变量。BAL数据用带范围的中值表示。分类数据比较使用卡方检验(皮尔逊检验或费雪精确检验)。两组比较采用非配对t检验和Mann-Whitney u检验。由于急性加重组只有8例患者,因此使用Mann-Whitney u检验比较了急性加重组和非急性加重组之间的所有数据。本次比较中排除了3例在声发射时出现的患者,因为他们的数据是在声发射时获得的,而没有声发射前的数据。通过将声发射作为“死亡变量”,对患者在随访结束时(死亡或失访)构建Kaplan-Meier曲线,得到声发射的频率。在随访结束时或死亡时,通过对数秩检验(单变量比例风险法)分析AE的危险因素,以确定AE作为“死亡变量”。由于本研究涉及的人数较少(n = 11),因此没有使用相同的比例风险模型进行多变量分析。所有病例均采用双侧检验; p-values <0.05 were deemed statistically significant.
结果
急性加重的频率
经SLBx诊断为IPF的147例患者中,23例因病情急性加重而入院,随访期间无明显感染。其中7名患者被排除在外,因为不能完全排除感染的可能性。另外5例患者不满足Kondoh的所有标准(病程较长和/或较轻的低氧血症),因此即使其中4例在病情加重时进行了活检,但确实表现出DAD叠加在UIP上的特征,他们也没有被包括在内。因此,仅其余11例患者符合Kondoh的所有AE标准et al。17是本研究的研究对象。
在幸存者的IPF随访中,AE的1年频率为8.5%,2年频率为9.6%。
与急性加重相关的危险因素
大多数患者中未发现AE的诱发因素。2例患者之前病情稳定,但在SLBx后不久发生AE。另一位患者在BAL后立即发生AE, 12天后进行了SLBx,显示出组织DAD模式。该患者BAL液培养及肺活检均为阴性。
当使用单变量比例危险法比较AE患者与无AE患者的初始人口统计学和临床特征时,未发现显著的危险因素(表1)⇓).
急性加重患者的临床特点
表2总结了AE受试者的临床特征⇓.在符合Kondoh标准的11例患者中,5例在手术肺活检诊断IPF后13.3±11.7个月(范围:3-60个月)发生AE。11例患者中有3例在诊断后立即发生AE(1例在BAL后,2例在SLBx后)。其余3例患者表现为AE,既往未诊断IPF,其中2例患者出现呼吸困难6个月和2个月,但直到入院前20天和14天症状急剧加重才就诊。其余患者在入院前1个月出现呼吸困难,进展迅速。4例患者(3例表现为肺声发射,1例发生BAL后发生肺声发射)在发生声发射时进行手术肺活检。从声发射发生到入院平均时间为13.0±10.7天(范围2 ~ 30天)。快速进行性呼吸困难(100%)是最显著的症状,伴咳嗽(55%)和痰量少(46%)。1例患者出现轻度发热,所有患者均无心脏病迹象。
支气管肺泡灌洗结果
11例患者中8例在AE发生时行BAL;其余3例在BAL和SLBx后发生AE。3例患者仅中性粒细胞升高(>5%),5例患者中性粒细胞和淋巴细胞均升高(>20%)(表2)⇑).
微生物研究
AE发生时采集的血液、痰液和尿液培养均为阴性。8例患者在发生声发射时进行的BAL液培养(不包括与手术相关的声发射)均为细菌、真菌和病毒阴性,试验也是如此卡氏肺孢子虫并巨细胞病毒。AE时SLBx获得的肺组织全部培养,未培养生物。10例患者(未检测BAL后发生AE的患者)进行了支原体、军团菌和病毒的血清学检测,均为阴性。一名患者的血液培养和一名患者的痰培养,都是在疾病过程中机械通气时采集的样本,好氧细菌呈阳性。这些被认为要么代表污染,要么是呼吸机相关肺炎的原因。
急性加重的放射学特征
高分辨率计算机断层扫描结果
所有8例患者在AE时均表现为新出现的弥漫性双侧磨玻璃影(GGO),叠加在胸膜下网状和蜂窝状密度上(图1)⇓- - - - - -⇓3.⇓).3例无事先诊断的AE患者的HRCT除弥漫性GGO外,还表现为双侧蜂窝状。新发GGO的分布模式在3例患者中主要为外周型,7例为多灶性,1例为弥漫性(表3)⇓).
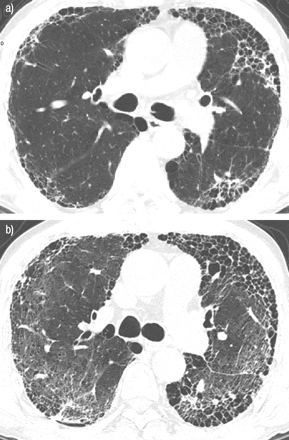
63岁男性,特发性肺纤维化,急性加重,外周型。a)初始高分辨率计算机断层扫描显示双肺胸膜下区域网状混浊和严重蜂窝状。b) 2个月后复查ct,双侧周围胸膜下分布出现磨玻璃影。
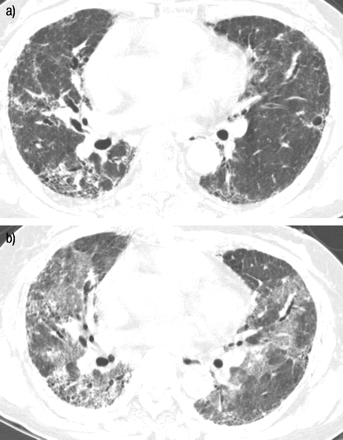
57岁女性,特发性肺纤维化,急性加重,表现为多灶斑片状。a)初始高分辨率计算机断层扫描显示肺胸膜下区域的网状混浊和蜂窝状。b) 1个月后的ct随访中,双肺均出现多灶斑片状分布的磨玻璃样混浊。斑片状的磨玻璃浑浊物随机分布,在磨玻璃浑浊物内也可见细小的网状浑浊物。
56岁男性,特发性肺纤维化,急性加重,弥漫型。患者在急性加重时首次到峨山医疗中心就诊,高分辨率计算机断层扫描显示双肺弥漫性磨玻璃混浊。近距离观察,在磨玻璃密度范围内,双下肺胸膜下可见蜂窝状和一些网状密度。患者于入院后22天死亡。
急性加重的病理表现
7例患者在发生AE前接受SLBx治疗,其中2例患者在发生SLBx后立即发生AE。这7例患者的病理共识诊断为UIP,无急性变化。其余4例患者在AE时为SLBx,所有病例均表现为UIP并合并DAD。在2例间质和空域组织、间质水肿和2型细胞增生的病例中,DAD主要处于组织期。只有2例患者的主要发现(相对于组织)是伴有透明膜的急性DAD(图4b)⇓),另外两例以肺泡内组织为主的病例中,有一例可见透明膜。而在每个域的基础上,特征可能与组织性肺炎相同,如隐源性组织性肺炎(COP)(图5b)所示⇓),透明膜的存在加上临床情况表明适当的分类为DAD的组织期。在这些病例中,气道组织通常也可与位于完整和疤痕肺交界处的UIP成纤维细胞灶区分开来。
一名66岁男性,在没有事先诊断的情况下出现急性加重。A)显示一个致密的疤痕区域,有较浅的成纤维细胞灶(图的下半部分),毗邻较密的嗜酸性旧胶原蛋白(上半部分)。b)所示区域显示完整的肺组织,急性肺损伤表现为气隙组织(中间和右下),气隙内有透明膜和纤维性渗出物。肺泡壁水肿增厚。这代表了急性加重的组织学相关性。
70岁女性,特发性肺纤维化并急性加重。a)常见间质性肺炎的典型背景特征,伴斑块状致密纤维化和结构破坏(右半)。b)该病例的急性加重表现为一个斑块组织性肺炎,涉及结构完整的肺组织,该区域与闭塞性细支气管炎组织性肺炎/隐源性组织性肺炎相同。
急性加重的临床病程
所有患者均使用广谱抗生素和皮质类固醇治疗,6例患者接受皮质类固醇脉冲治疗(甲基强的松龙1克·日)−13天)。
在机械通气的9例患者中,医院死亡率为78%。4例患者在初始发作后存活,但其中2例在3个月内死亡(总死亡率为81.8%)。除1例患者(呼吸机相关性肺炎)外,死因为进展性疾病。在发生手术(BAL和SLBx)相关AE的3例患者中,只有1例(SLBx后)死亡。AE发生时的HRCT模式有显著的预后价值(p = 0.042);所有3例外周型GGO患者和1例多灶型GGO患者在初始发作后均存活(表3)⇑).有2例AE复发,分别在2.5个月和9个月后出现类似的恶化,并于当时死亡。
讨论
根据作者对大量IPF患者的经验,IPF中AE的1年频率为8.5%,2年频率为9.6%。但本研究的实际发生率可能更高,因为:1)部分患者在随访中丢失;2)即使在住院患者中,由于诊断的不确定性,也没有将所有急性加重的患者纳入本研究;3)仅纳入手术确诊的UIP患者;4)另外5名患者没有严格满足Kondoh的所有标准,因此也被排除在外,但实际上具有临床和外科肺活检病理特征(其中4例),这强烈表明他们是AE病例。对AE患者与未发生AE患者的人口学特征和肺功能参数进行单因素比例危险分析,未能发现显著的危险因素。
IPF通常是一种慢性疾病,平均/中位生存时间为3年1,3.,4,尽管疾病的发展速度各不相同25.急性恶化可继发于感染、肺栓塞、气胸或心力衰竭26,但也可能在没有可识别原因的情况下发生,这被称为IPF的AE6- - - - - -20.,27,28.然而,这种现象的临床特征尚不清楚,也没有广泛接受的AE定义。AE的定义在严重性和快速性方面从作者到作者有所不同。Kondoh说et al。17,低氧血症的判据为氧张力/吸入性氧张力比<225,而Akiraet al。18在类似条件下,采用>标准降低1.33 kPa (10 mmHg)。此外,尽管在大多数定义中,加重性呼吸困难的持续时间被定义为<1个月(或几周),但从Rice的受试者入院前开始快速恶化的时间et al。193-60天,Akiraet al。182 ~ 44天。这项研究只包括满足Kondoh最严格标准的受试者et al。17以集中研究这些核心患者的数据,这导致排除了5名满足Akira不太严格的标准的患者et al。18.其中4例患者的组织病理学结果与研究队列中的患者相似,这表明IPF可能存在一系列疾病进展,从典型的慢性进展性疾病到Kondoh定义的显性AEet al。17.康多的标准很重要,因为它们代表了定义一个以前未知实体的第一次尝试;然而,这项研究表明,它应该重新定义。当AE发病前基线疾病严重程度较轻时,同样严重的加速下降可能不会导致足够严重的缺氧以满足Kondoh的标准。因此,在这方面,明的标准et al。18似乎更合适。此外,呼吸困难加重的发作时间可延长至数周。如果使用Akira的标准,并将不能完全排除感染的7名患者也包括在内,1年的频率将为15.4%,2年的频率为18.0%。当加速衰退的患者与AE患者(由Kondoh定义)进行比较时,急性加重的任何参数均无显著差异(表2)⇑)在两组之间发现;此外,没有发现“加速衰退”发展的显著危险因素。
尽管我们认为所有患者在随访时均应已诊断为IPF并表现为AE,但有3例患者在表现为AE前未确诊为IPF。其中2例患者在入院前出现呼吸困难,3例患者HRCT上除了弥漫性GGO外,还出现大量蜂巢状病变,强烈提示存在潜在的IPF。此外,UIP的病理表现,如胸膜下镜下蜂窝状、致密纤维化和成纤维细胞灶(不是闭塞性细支气管炎组织肺炎型的马松体),加上DAD特征,提示诊断IPF为AE,而非AIP。本研究中3例明确声发射患者和4例可疑声发射患者在HRCT和病理上均具有上述特征。
与已发表的报告一致,在本研究的大多数受试者中,声发射的病因不明;然而,3例患者在医源性手术后立即发生声发射(2例发生在SLBx后,1例发生在BAL后),也有几例SLBx后发生声发射的报道6,7,肺切除术8,9,或BAL10- - - - - -12.此外,伍兹et al。29报道称,IPF/UIP患者SLBx后的短期死亡率(16.7%)较高,而在同一机构接受SLBx的771名未选择的患者的死亡率为1.7%30..在他们的报告中,作者将80%的死亡记录归因于急性肺损伤。然而,由于这些患者已经有IPF(因为该研究的对象根据定义是IPF患者),我们有理由认为这些病例代表的是AE,而不是病因不明的急性肺损伤。事实上,当作者更详细地回顾这篇论文时,发现SLBx可能在25%的病例中诱发了声发射,其余75%可能在活检时发生了声发射。在本研究中,2例患者在SLBx后发生AE, 4例患者在病情迅速加重后进行活检,2例患者在活检后进一步恶化并死亡。因此,本研究结果与以往报道的SLBx可诱发或加重IPF患者呼吸状况的快速恶化相一致。因此,从作者的经验和文献报道来看,现在认为在病情迅速恶化时进行SLBx是不必要和不道德的,除非有额外的适应症,如排除感染或相关恶性肿瘤。
感染是AE鉴别诊断中最重要的因素,因为许多IPF患者接受了皮质类固醇治疗,或联合或不联合细胞毒性药物。虽然这项研究是回顾性的,但所有可能的微生物学研究都是在所有患者中进行的,除了那些因手术相关AE而没有进行BAL的患者,因为他们当时没有免疫功能受损。所有调查结果均为阴性,从鉴别诊断中排除感染。胃食管反流也可能与AE的病因有关,因为IPF患者的食管酸反流明显多于其他间质性肺部疾病患者31.这需要进一步的研究来评估。
HRCT显示,除了3例未事先诊断为AE的患者外,新出现的、广泛的GGO叠加在原有的胸膜下网状密度上,并伴有蜂窝状。这些患者的hrct显示胸膜下区蜂窝状病变与广泛的GGO并存,手术肺活检显示UIP合并DAD,提示IPF AE,排除急性间质性肺炎。
AE治疗的报告仅限于少数病例,尽管有几篇论文报告了皮质类固醇治疗的改善14,17,28.冢本et al。28IPF发病年龄、AE(二氧化碳动脉张力)前的呼吸状态、炎症活动性(c反应蛋白)与反应性和患者结局密切相关。然而,由于本研究中所有患者都接受了皮质类固醇治疗,而且死亡率很高,因此不可能评估皮质类固醇的疗效。此外,在本研究的患者中,上述参数在治疗反应或预后方面没有发现显著差异。然而,有报道显示,多灶性和弥漫性实质混浊患者的预后比周围性实质混浊患者差18,本研究的结果与此数据一致。
在AE期间进行的组织学方面,主要的组织学发现是DAD,主要是在组织期,正如病理学文献中所描述的那样32,33.虽然在特定的显微镜视野下,由于COP等其他原因,其外观与肺泡内组织相同,但同时存在急性呼吸衰竭,HRCT数据,加上四例中三例中相邻透明膜的区域,表明组织DAD的特征。然而,尽管有人认为纯粹的组织模式比透明膜的更急性模式更有利18在美国,只有4名患者的局限性排除了对这一假设的评估。也不可能在背景UIP中确定任何表明急性加重易感的特征。
综上所述,本研究显示特发性肺纤维化急性加重在2年内的频率为9.6%。数据表明,急性加重可以作为一个谱系而不是一个明确定义的事件发生。病因尚不清楚。需要进一步的研究来评估这种恶化的范围,确定危险因素,并确定治疗的疗效。
- 收到了2004年10月2日。
- 接受2005年9月9日
- ©ERS期刊有限公司