摘要
利奈唑胺用于治疗耐多药(MDR)/广泛耐药(XDR)-结核病(TB)患者,但缺乏关于其安全性、耐受性和疗效的临床数据。
我们进行了一项回顾性、非随机、非盲观察研究,评估利奈唑胺600mg时的安全性和耐受性q.d。或b、 身份证。在四个欧洲国家的耐多药/广泛耐药结核治疗。疗效评价比较了45例利奈唑胺治疗与110例未治疗利奈唑胺治疗的疗效终点。
在195名耐多药/广泛耐药结核病患者中,85人接受利奈唑胺治疗,平均治疗时间为221天。在85例患者中,35例(41.2%)出现利奈唑胺引起的严重副作用(贫血、血小板减少和/或多神经病变),其中27例(77%)需要停药。大多数副作用发生在治疗60天后。每日两次给药比每日一次给药产生更多的主要副作用(p = 0.0004),疗效没有发现差异。虽然利奈唑胺治疗的患者有更多的一线(p = 0.002)和二线(p = 0.02)耐药和更多的既往治疗方案(4.5与2.3;p = 0.07)。
Linezolid 600毫克q.d。添加到个体化多药方案中可能会提高细菌转化的机会,仅在最复杂的耐多药/广泛耐药结核病例中提供更好的治疗成功机会。其安全特性不保证在有其他更安全的替代品的情况下使用。
结核病(TB)是全世界死亡的主要原因。世界卫生组织(世卫组织)估计,2006年约有920万新结核病病例和150万结核病相关死亡1..耐多药(MDR)的流行结核分枝杆菌(定义为在体外对异烟肼和利福平(两种最有效的结核病治疗一线药物)的耐药性在全球正在增加2.,3..在前苏联一些国家、以色列和中国地区,目前在所有结核病病例中发现了15%以上的耐多药毒株4.–6..结核分枝杆菌对二线药物的耐药性也正在出现。广泛耐药(XDR)结核病(世卫组织定义为在体外对异烟肼和利福平以及任何氟喹诺酮类药物和至少一种注射药物(卷曲霉素、卡那霉素或阿米卡星)的耐药性在世界大多数地区都有描述7.,8..本文是结核病网络欧洲试验小组(TBNET)的一项更大努力的一部分,该努力旨在描述欧洲耐多药和广泛耐药结核的临床流行病学特征,从而加强对耐多药和广泛耐药结核控制的临床和公共卫生建议的证据基础。
复杂耐多药结核病例(除异烟肼和利福平以外还有其他耐药性的病例)和广泛耐药结核病例的治疗结果很差9–15.因此,关于其他可能在治疗中有用的抗生素的安全性、耐受性和有效性的信息对于改善个别结果和控制耐多药和广泛耐药结核的传播是迫切需要的。在体外药理学数据表明,恶唑烷酮类抗生素利奈唑胺可用于治疗分枝杆菌感染,包括耐多药结核病16–23.然而,利奈唑胺用于批准用途之外的临床经验主要局限于非结核分枝杆菌疾病的病例报告24–29.利奈唑胺在东欧和西欧都用于治疗多药/广泛耐药结核,这是该药物批准用途之外的一个用途,但治疗成本很高。在德国最近的一项关于耐多药结核病的流行病学研究中15在美国,利奈唑胺被广泛使用:33.8%的患者报告有副作用,56%的患者出现严重贫血。然而,这些数据和其他之前的研究22,30.–33没有提供足够的细节来评估利奈唑胺在多药/广泛耐药结核治疗中的安全性、耐受性和有效性。本研究的目的是评估利奈唑胺的安全性、耐受性和有效性,研究对象为来自四个欧洲国家的大量耐多药/广泛耐药结核病患者。
方法
研究设计
这项回顾性队列研究分析了2001年至2007年期间来自白俄罗斯、德国、意大利和瑞士21个参与中心的耐多药/广泛耐药结核患者的安全性和耐受性。为了评估利奈唑胺在耐多药/广泛耐药结核治疗中的疗效,我们只比较了有明确治疗终点记录的患者(治愈、完成、死亡或失败)。在收集数据时仍在接受治疗的患者被排除在分析之外,因为这些病例没有后续信息。
该数据收集工具在德国进行了预测试15,提供以下信息:以前的治疗、艾滋病毒状况、耐药情况、痰液时间和培养转化、住院时间、不良反应(是/否)、治疗中断(是/否)和治疗结果。该工具经过改进,包括利奈唑胺剂量和不良反应、利奈唑胺再入(包括剂量)和治疗方案中使用的抗结核药物的细节。最后的数据集包括来自德国的74例耐多药/广泛耐药结核病例中的59例和来自意大利、白俄罗斯和瑞士的另外26例病例的完整信息。
意大利桑达洛医院临床协调中心的伦理委员会和意大利Tradate的Fondazione S. Maugeri统计协调中心批准收集研究数据。所有参与中心都遵守国家有关人体保护的法规和组织要求。所有数据都进行了编码,个人识别码仅供治疗医生使用。
定义
Laserson提出的标准治疗结果定义et al。34是否如前所述使用11,35.
完成治疗且在最后12个月治疗中培养持续阴性且至少有5个结果的患者被定义为治愈。如果没有细菌学结果(即进行了少于5个培养),该病例被定义为治疗完成。治疗失败定义为在过去12个月的治疗中有两个或两个以上的阳性培养,或由于反应不良或不良事件而决定终止治疗。
安全性和耐受性终点包括大的和小的副作用。主要副作用被定义为导致利奈唑胺暂时或永久停用的任何不良反应,而轻微副作用仅需要调整剂量和/或增加伴随治疗。所有接受利奈唑胺治疗的患者都纳入了安全性和耐受性分析。
疗效终点包括痰涂片和培养转化的时间和比例,以及治疗结果。痰转阴定义为在诊断时痰涂片呈阳性的患者中连续两次痰涂片呈阴性。培养转换时间定义为从治疗开始到两个连续阴性培养的第一个日期的时间。
数据收集
数据提取自参与中心连续诊断的所有经培养确认的耐多药/广泛耐药结核病例的临床记录,并经研究审查小组验证。对一线和二线抗结核药物的药敏试验(DST)由世卫组织超国家参考实验室(罗马/米兰,博尔斯特尔,斯德哥尔摩)保证质量的实验室进行。9–11. 所有参与中心每周进行痰涂片检查,直到阴性,然后每月进行一次。每月进行一次培养。
治疗方案
在所有国家,治疗多药/广泛耐药结核病例的方案都根据世卫组织的建议,使用氟喹诺酮类药物、注射药物和其他二线口服药物,根据DST结果量身定制。利奈唑胺的供应没有任何限制,但在白俄罗斯,由于该国供应有限,为优化药物使用,该药的处方最长为3个月。
统计分析
分类变量比较采用卡方检验,连续变量比较采用未配对数据t检验。p值≤0.05被认为有统计学意义。使用Stata 9.0 (StataCorp, Stata Statistical Software Release 9, College Station, TX, USA)对标准化电子表格数据进行收集和分析。
结果
在195例MDR/XDR-TB病例中,85例患者接受了包括利奈唑胺的个体化方案治疗,110例患者接受了不使用利奈唑胺的个体化方案治疗。在利奈唑胺组,45例患者有明确的治疗终点,40例患者没有:40例中有1例(2.5%)违约,1例(2.5%)转移,38例(95%)仍在接受治疗。
安全性和耐受性
对所有75例耐多药结核病患者(88.2%)和10例广泛耐药结核病患者(11.8%)服用利奈唑胺后的安全性和耐受性进行了评估。其中28名患者在600分钟时服用利奈唑胺 镁q.d。57名患者服用600毫克b、 身份证。(1,200 毫克)。在这两组人之间,主要社会人口统计学变量或耐药谱没有观察到差异(数据未显示)。
利奈唑胺平均±1sd疗程222±249天(中位93天)。
中位值为69后出现不良事件 天数(范围1-596 总的来说,85名患者中有35名(41.2%)出现了52次可归因于利奈唑胺的副作用。在出现副作用的35名患者中,27名(77.1%)出现了需要暂时或永久停用利奈唑胺的严重副作用,而8名(22.9%)患者有轻微的副作用。
副作用主要表现为贫血(52例中23例(44.2%))。在23例贫血患者中,5例(21.7%)受到严重影响,由于血红蛋白水平<8 mg·dL,需要输血−1;其中两名患者患有溶血性贫血。其他副作用包括血小板减少症(7例(13.5%),恶心/呕吐(4例(7.7%))和多神经病变(3例(5.7%))。27例出现严重副作用的患者中有8例(29.6%)成功地再次使用利奈唑胺,27例患者中有19例(70.4%)永久停用利奈唑胺。没有观察到利奈唑胺相关的死亡。
服用600毫克的两组患者的副作用有显著差异与每天1200毫克。28例接受600毫克利奈唑胺治疗的患者中,只有4例(14.3%)出现了任何副作用与57名受试者中有31人(54.4%)接受了1200名受试者 mg(p = 0.0004;图。 1.⇓).每日服用利奈唑胺600毫克的患者发生重大副作用的风险和任何副作用的风险均低于每日服用1200毫克的患者(表1)⇓).
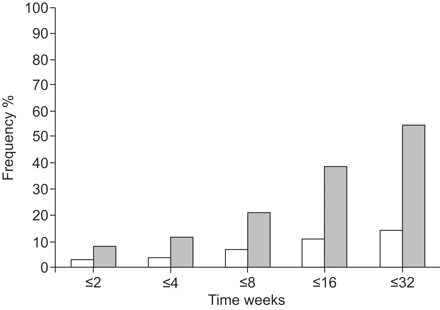
在600 mg治疗开始后的不同时间点,利奈唑胺联合治疗多药耐药/广泛耐药结核病期间的不良反应频率q.d。或者600毫克b、 身份证。方案(分母为每组总人数)。□:600毫克q.d。, n = 28;▓:600毫克b、 身份证。, n = 57。
疗效端点分析
45例利奈唑胺治疗的患者与110例未治疗的患者在主要人口统计学和临床变量上的疗效没有发现显著差异。45例利奈唑胺治疗的患者中有41例(91.1%)耐多药结核病患者,110例未治疗的患者中有102例(92.7%;P = 0.83), 4例(8.9%)和8例(7.3%;p = 0.82)。利奈唑胺组和非利奈唑胺组一线药物平均耐药数分别为4.3和3.8 (p = 0.002),二线药物平均耐药数分别为1.5和0.9 (p = 0.02)。两组均包括再治疗患者,但利奈唑胺治疗组先前处方治疗方案的平均数量(>1个月)几乎增加了一倍(4.5与分别为2.3;p = 0.07)。接受过利奈唑胺治疗和未接受过利奈唑胺治疗的患者平均服用五种药物。
与未接受利奈唑胺治疗的患者相比,接受利奈唑胺治疗的患者在痰涂片和培养转换上花费的时间明显更长,但总体转换百分率更高(尽管不显著)(表2)⇓).均值±sd涂片转化时间为102.9±74 利奈唑胺组为65.4±80.1天 非利奈唑胺组(p = 0.007),而平均值±sd培养转化时间分别为109±71天和69±63天(p = 0.0007)。利奈唑胺组达到痰涂片转换的比例为69%与非利奈唑胺组54%(相对风险(RR) 1.28;95%可信区间(CI) 0.99-1.6;p = 0.08)。实现培养转化的比例为87与78% (RR 1.1;95%可信区间0.95 - -1.28;p = 0.22)。对于那些有明确治疗终点的患者,治疗结果没有显著差异:45例利奈唑胺治疗患者中有36例(80%)获得了治疗成功与110例非利奈唑胺治疗的患者中有90例(81.8%)(p = 0.88),两组之间的失败或死亡风险没有差异。
对于开600美元处方的患者,疗效相似 镁与1200 mg利奈唑胺:600 mg中达到痰涂片转换的比例为71.4%与1200毫克组为67.7% (p = 0.8)。600 mg·d组达到培养转化的比例为92.9%−1与每天1200毫克,83.9%−1组(p = 0.4)。均值±sd600 mg·d时痰涂片转换时间为101.5±79.3天−1组,103.6±73.4 1200天 毫克·天−1组(p = 0.9),而平均±sd培养转化时间分别为109±74.6天和108.8±70天(p = 0.9)。疗效终点(痰液和培养转换,或阳性治疗结果)与胸片上有无空腔无显著差异。
根据耐药模式分层的疗效终点分析
当分层隔离的药物数量抗性,痰涂片和培养的比例转换器linezolid组高于non-linezolid组地层,达到统计学意义仅为例窝藏菌株耐超过7药物(p = 0.009涂片;P = 0.004;表3⇓).与菌株耐药的药物数量相关的转化时间没有明确的趋势(数据未显示)。
讨论
在缺乏结核病治疗新药的情况下,治疗耐多药/广泛耐药结核患者严重依赖于耐药模式以及具有合理安全性、耐受性和有效性的二线和三线抗结核药物的可用性13,14.据传闻,利奈唑胺可能是治疗复杂的耐多药/广泛耐药结核病例的有效选择。然而,人们对安全性和耐受性提出了严重的担忧。5项研究的结果表明,不良事件可能在43%左右30.高达80%或更多22,29,32,33,35.本研究的结果增加了以前研究的发现15,在33.8%的病例中观察到不良反应,但没有关于处方剂量或副作用详情的信息。
我们的结果证实了利奈唑胺的主要副作用发生率很高,特别是在1200毫克以上的剂量和治疗时间超过8周的情况下。尽管我们的研究结果比之前描述的大多更令人鼓舞22,30.–33在及时停药或减少剂量后不久,不良事件似乎是可逆的30.,它们仍然非常相关。接受治疗的三分之一以上的病例(85例中有35例(41.2%)出现副作用,其中27例(31.8%)出现严重不良反应,足以表明停药。
我们的数据显示每日600毫克和1200毫克利奈唑胺的副作用有显著差异:当处方剂量较低时,副作用发生的频率较低,而两种剂量之间的疗效没有显著差异。这些数据表明,较低的剂量足以传达利奈唑胺可能的好处,同时降低重大副作用的风险。相比之下,根据8名患者每天服用600毫克利奈唑胺的病例系列,Parket al。33提示这种“每日半剂量”治疗难治性耐多药/广泛耐药结核病例是有效的,但不能防止重大不良事件的出现。
在我们的队列中,利奈唑胺的平均服用时间超过32周。13例(37.1%)利奈唑胺所致不良反应发生在治疗的前8周。28名每日服用600毫克利奈唑胺的患者中,只有1名(3.6%)在治疗的前8周出现了药物不良反应。不良反应出现的中位时间为~ 10周(69天),表明在~ 2个月的利奈唑胺治疗后,不良事件的风险增加。
我们的数据显示,接受利奈唑胺治疗(两种剂量)的患者与非利奈唑胺组的患者取得了相似的治疗结果,尽管接受利奈唑胺治疗的患者比未接受利奈唑胺治疗的患者有更频繁的既往治疗史,并且对更多的一线和二线药物产生耐药性。接受利奈唑胺治疗的患者痰涂片和培养转化比例较高(仅对7种以上药物耐药显著),但转化所需时间明显长于未接受利奈唑胺治疗的患者。广泛耐药结核患者治疗成功率的明显提高可能是减少广泛耐药结核菌株传播的一个机会。这将有助于在未来的研究中改进方法(如。前瞻性、随机或盲法评价),以便更彻底地评估药物的安全性、有效性和质量。这些发现表明,利奈唑胺可能有助于治疗最复杂的耐多药/广泛耐药结核病例,并值得在一项随机对照试验中进行进一步研究。
据我们所知,这是首个全面评估利奈唑胺耐受性的研究,也是首个在临床环境中对利奈唑胺长期疗效的报告。这项研究的优势包括相对较大的样本量、实验室数据的质量(检测和质量控制的DST检测的所有广泛耐药结核病定义药物)以及从四个欧洲国家提供代表性数据的能力。
该研究具有回顾性观察性质,有几个局限性。虽然所描述的不良反应在所有病例中当利奈唑胺治疗停止时是可逆的,但利奈唑胺治疗和不良反应的因果关系尚未得到证实,因为它们也可能是其他药物引起的。另一个偏倚是患者接受利奈唑胺治疗的非随机分配。由于接受利奈唑胺治疗的患者比未接受利奈唑胺治疗的患者对更多药物产生耐药性(因此可能治疗成功的机会较差),从这些数据来看,利奈唑胺对治疗结果的影响可能已经减弱。此外,即使是一个相当大的队列患者,当数据按耐药模式分层时,患者数量也变得很小,这挑战了我们以确定的方式评估利奈唑胺对疗效的潜在影响的能力。
该研究结果的重要意义在于:1)证实了利奈唑胺在其他研究中所提到的不良反应的实质性风险,但建议在不失去利奈唑胺的潜在益处的情况下,可以使用更安全的剂量;2)提供文献,谨慎证明利奈唑胺仅用于最复杂的耐多药/广泛耐药结核病例的临床实践;3)为监管当局制定明确的利奈唑胺用于耐多药/广泛耐药结核治疗的适应症提供证据;4)表示未来研究可比较的基线;5)允许对前瞻性、控制性临床试验进行论证和改进计划。总的来说,研究结果具有临床和公共卫生的相关性。
总之,数据表明,利奈唑胺可能有助于提高涂片和培养转化的机会,并可能在没有其他治疗方案的情况下,仅在最复杂的耐多药/广泛耐药结核病例中提供更好的治疗成功机会。但是它的安全性并不能保证在其他更安全的二线或三线药物可用的情况下使用它。与利奈唑胺相关的副作用是频繁且经常严重的,需要仔细监测,特别是治疗超过8周时。很可能,利奈唑胺的潜在益处可以通过使用较低的剂量600 mg来实现q.d。,这似乎降低了该队列患者的副作用风险,因此在不改变疗效的情况下降低了成本。此外,还应开展利奈唑胺用于耐多药/广泛耐药结核难治病例的随机对照试验,以证实这些发现。
支持声明
本研究由参与机构的现有研究经费支持。该数据收集系统于1996年启动,由意大利医院肺病学家协会(AIPO)通过卫生部/高级卫生研究所赠款(国家结核病项目,第1 641/96号赠款)获得资金。该研究由欧洲呼吸学会临床研究合作项目部分资助。188bet官网地址
利益陈述书
没有宣布。
致谢
作者的联系如下。G.B.Migliori和R.Centis:世卫组织结核病和肺病合作中心,意大利特拉达特护理研究所Fondazione S.Maugeri。B.Eker和C.Lange:德国博尔斯特尔研究中心临床传染病科。理查德森博士:HIV/TB全球计划,PATH,西雅图,瓦城,USA. G. Sotgiu:卫生与预防医学研究所,萨萨里,萨萨里,意大利大学。J.P.齐薇格:结核病诊所,瑞士洛桑,洛桑大学门诊和社区医学系。A.Skrahina:白俄罗斯明斯克肺病和结核病研究所。J.Ortmann:肺科诊所,卡尔·汉森诊所,巴德·利普斯普林格,德国。E.Girardi和N.Bevilacqua:意大利罗马国家传染病研究所(INMI)L.Spallanzani。H.Hoffmann:超国家结核病参考实验室,Asklepios诊所,慕尼黑戈廷,慕尼黑戈廷,德国。G.Besozzi:E.Morelli医院,耐多药结核病和艾滋病毒结核病参考医院,索达洛,意大利。D.Kirsten:德国格罗·汉斯多夫格罗·汉斯多夫医院,肺病学和胸外科中心。
TBNET研究小组的其他参与成员如下。白俄罗斯:H. Hurevich,肺病和结核病研究所,明斯克;A.白俄罗斯国立医科大学斯克拉欣,明斯克。德国:R. Muetterlein, Pasberg地区医院;T. Schaberg, Rotenburg Deakoness医院肺部诊所;R. Eberhardt, Division of Pulmonary Medicine, thorax - clinical -Heidelberg,海德堡;H.弗利克,传染病司,Charité柏林,柏林;A. de Roux,肺诊所,新教肺诊所,柏林;M. Hamm, Diekholzen医院肺部诊所;H. Hang,肺部诊所,医院Schillerhöhe, Schillerhöhe; P. Hannemann, Pulmonary Clinic, Deakoness Hospital, Neustadt; D. Hillemann, Division of Mycobacteriology, Research Center Borstel, Borstel; B. Kretz, Asklepios Pulmonary Hospital, Gauting; C. Laumanns, Bethania Hospital, Solingen; A. Paulick, Pulmonary Clinic-Coswig, Coswig; M.W. Pletz, Division of Pulmonary Medicine, Hanover Medical School, Hanover; M. Rau, Pulmonary Clinic, Wangen; C. Schaudt, Pulmonary Clinic, Hospital St Blasien, St Blasien. Italy: A. Matteelli, Brescia University, Brescia; A. Spanevello, Insubria University, Varese; O. Toungoussova, Fondazione S. Maugeri, Cassano delle Murge; Lia D’Ambrosio, Fondazione S. Maugeri, Tradate; S. De Lorenzo, P. Troupioti and G. De Iaco, Sondalo Hospital, Sondalo; A. Gualano, P. De Mori and F.N. Lauria, INMI L. Spallanzani, Rome; G. Ferrara, University of Perugia, Perugia; D. Cirillo, S. Raffaele Hospital, Milan. Switzerland: J.P. Janssens, University Hospital Geneva, Geneva.
- 收到了2009年1月20日。
- 认可的2009年2月24日。
- ©ERS期刊有限公司















