摘要
严重或耐药哮喘日益被认为是一种未得到满足的主要需求。由欧洲呼吸学会和美国胸科学会支持的一个工作组审查了该定义,并就188bet官网地址儿童和成人严重哮喘的评估和治疗提供了建议和指南。
进行了文献综述,然后由专家委员会根据GRADE (GRADE of Recommendations, Assessment, Development and Evaluation)方法进行讨论,以制定具体的临床建议。
当诊断为哮喘并解决了合并症时,严重哮喘被定义为需要使用高剂量吸入糖皮质激素加上第二个控制者和/或全身性糖皮质激素治疗以防止其变得“不受控制”或尽管采用这种治疗仍然“不受控制”的哮喘。严重哮喘是一种由嗜酸性哮喘等表型组成的异质性疾病。具体建议使用痰嗜酸性粒细胞计数和呼出一氧化氮来指导治疗,以及抗ige抗体、甲氨蝶呤、大环内酯类抗生素、抗真菌药物和支气管热成形术治疗。
改善表型的协调研究工作将为严重哮喘治疗提供安全有效的生物标志物驱动方法。
摘要
ERS/ATS指南修订了严重哮喘的定义,讨论了表型,并为患者管理提供了指导http://ow.ly/roufI
执行概要
欧洲呼吸188bet官网地址学会(ERS)/美国胸科学会(ATS)严重哮喘工作组包括严重哮喘的最新定义,与遗传学、自然史、病理生物学和生理学有关的严重哮喘表型的讨论,以及对严重哮喘的评估和治疗的部分,其中提出了具体的实践建议。有关严重哮喘的定义、表型和实践建议的详细讨论,请参阅未删节的在线版本。
当诊断为哮喘并已解决合并症时,严重哮喘被定义为“需要使用高剂量吸入皮质类固醇(ICS)治疗的哮喘”表4对于成人和儿童的剂量),再加上第二个控制器(和/或全身皮质类固醇),以防止它变得‘失控’或尽管采用这种治疗仍然‘失控’。”
本文件中用于制定临床建议的方法遵循ATS和ERS指南方法学。该委员会包括在严重哮喘方面具有专业知识的临床医生和研究人员,以及一名方法学家,他帮助按照GRADE(分级建议、评估、发展和评估)方法准备了系统的证据摘要。根据ATS和ERS规则管理潜在的利益冲突。
系统地搜索支持这些指南中建议的证据,发现很少有低偏倚风险的随机对照试验(rct)能够提供直接、一致和精确的证据。因此,许多建议都是基于对轻中度哮喘患者进行的研究的间接证据,这些研究往往无法准确估计预期和预期的健康影响。此外,很少有研究评估了委员会认为在提出建议时至关重要的所有结果。
委员会根据GRADE方法制定和分级建议,并评估支持证据的质量。根据评估的偏倚风险、直接性、一致性和准确性,证据质量(对现有治疗效果估计的置信度)分为:高、中、低或极低。低质量和极低质量的证据表明,干预措施的估计效果非常不确定,进一步的研究很可能对最终的建议产生重要影响。
建议的强度表示为强(我们建议……)或有条件(我们建议……),并具有明确的含义(表2).理解这两个等级的解释对于做出明智的临床决策至关重要。
范围和目的
本文的目的是修订严重哮喘的定义,讨论可能的表型,并为严重哮喘患者的管理提供指导。这些指南的目标受众是呼吸医学和过敏管理成人和儿童严重哮喘的专家。全科医生、儿科医生、初级保健医生、其他卫生保健专业人员和政策制定者也可从这些指南中受益。这份文件也可作为制定和执行适合当地情况的准则的基础。
简介
虽然大多数哮喘患者可以用目前可用的药物进行有效治疗,但仍有相当一部分患者难以治疗。这些病人在资源支出中所占的比例相对较大。关于管理这些患者的最佳方法,或驱动这一过程的潜在机制,仍有许多不清楚的地方。在1999年和2000年,严重/难治性哮喘的第一个定义分别发表在欧洲呼吸杂志在美国呼吸与重症监护医学杂志,随后的队列采用了这些方法的变体[1,2].2009年,由ATS和ERS组成的23人联合工作组由成人和儿科培训专家和科学家组成,他们在管理和调查哮喘患者,特别是严重哮喘患者方面拥有丰富的经验,以:1)更新以前的定义,2)确定严重哮喘的潜在机制/表型,3)概述其评估,4)提供关于成人和儿童的治疗建议。专责小组的另一个目标,是总结过去12年的研究结果。[1,2并为逐步提高我们对严重哮喘的认识提出方向。严重哮喘现在被广泛认为是一种异质疾病,由多种表型组成,研究开始定义表型生物标志物,表型靶向生物治疗越来越显示出疗效。
方法
委员会的组成以及披露和管理潜在利益冲突、证据综合、提出建议和对指南进行同行评审的过程在这些指南仅在线发布的全文文件中进行了详细描述。
简单地说,该指南代表ATS和ERS之间的协作努力。该委员会由临床医生和研究人员组成,他们在严重哮喘和根据GRADE方法制定指南方面具有公认的专业知识[3.].根据ATS和ERS政策,所有委员会成员都披露了他们潜在的利益冲突。在所有审议过程中,认为存在利益冲突的成员都弃权,不就涉及潜在利益冲突的具体建议作出决定。ATS和ERS以及为这两个专业学会提供外部资金的任何商业实体的观点和利益对最终建议没有影响。
披露潜在的利益冲突
委员会成员根据ATS和ERS政策披露了所有潜在的利益冲突。主席(K.F.C.和S.E.W.)审查并解决委员会成员的所有潜在利益冲突。所有潜在的利益冲突(包括主席的利益冲突)都与ATS的道德和利益冲突委员会主席进行了讨论。在所有审议过程中,认为存在利益冲突的成员都放弃了有关潜在利益冲突的具体建议的决定。ATS的方法学家(J.L.B.)没有参与对任何建议的投票。
ATS和ERS在年会期间提供会议设施,并为电话会议提供财政支助。ATS和ERS以及为这两个专业学会提供外部资金的任何商业实体的观点和利益对最终建议没有影响。
每个问题的证据摘要(在线补充材料1)均按照GRADE方法准备[3.并由所有委员会成员审查。我们的证据总结基于现有的、最新的、执行良好的系统综述,如有必要,还补充了其他的近期随机对照试验。当没有近期有效的系统综述时,我们没有进行严格的系统综述,但我们系统地检索了相关研究(在线补充资料2)。
根据GRADE方法,我们将建议标记为“强”或“有条件”。我们用“We recommend”表示强烈的建议,用“We suggest”表示有条件的建议。表2对患者、临床医生和卫生保健政策制定者提出的强有力和有条件的建议提供建议性解释。
许多与严重哮喘患者管理相关的问题已被委员会确定为潜在的重要问题,但尚未得到解决(在线补充材料2)。委员会打算在2015年之前定期更新该文件。
如何使用这些指南
ERS/ATS关于严重哮喘管理的指南并不打算强加一个护理标准。它们为治疗严重哮喘的合理决策提供了依据。临床医生、患者、第三方付款人、机构审查委员会、其他利益相关者或法院永远不应将这些建议视为命令。没有任何指南和建议能够考虑到所有通常引人注目的独特的个人临床情况。因此,任何负责评估临床医生行动的人都不应试图死记硬背或一板一张地应用这些指南中的建议。
关于基本价值观和偏好的陈述以及每项建议附带的限定说明是不可分割的部分,有助于更准确的解释。在引用或翻译这些指南中的建议时,绝不能省略它们。
1.专责小组对严重哮喘的定义
≥6岁患者严重哮喘的定义见表3.
第1阶段:确认哮喘诊断并确定难以治疗的哮喘
严重哮喘的定义固有地排除了那些表现为“难治性”哮喘的个体,在这些个体中,适当的诊断和/或混杂因素的治疗极大地改善了他们目前的状况(见评估部分)。因此,建议表现为“难治性哮喘”的患者确认哮喘诊断,并由哮喘专家进行3个月以上的评估和管理。因此,根据ATS/ERS的定义,严重哮喘仅包括难治性哮喘患者和那些对严重鼻窦疾病或肥胖等共病治疗尚不完整的患者。
第2阶段:区分重度哮喘和轻度哮喘
当诊断为哮喘并解决了合并症时,严重哮喘被定义为“需要高剂量吸入糖皮质激素(ICS)治疗的哮喘”(见“重症哮喘”)表4对于成人和儿童的剂量),再加上第二个控制器(和/或全身皮质类固醇),以防止它变得‘失控’或尽管采用这种治疗仍然‘失控’。”这一定义包括接受了这些疗法的充分试验,但因缺乏反应而停止治疗的患者。对于>岁的6岁患者,“金标准/国际指南治疗”是高剂量ICS加长效β2-激动剂(LABA)、白三烯调节剂或茶碱和/或连续或接近连续的全身皮质类固醇作为背景治疗[4- - - - - -7].这一定义类似于最近的创新医学计划[8],但没有涉及世界卫生组织确定的未经治疗的严重哮喘患者群体[9].虽然在目前尚无广泛治疗方法的许多地区,未经治疗的严重哮喘是一个巨大的问题,但2013年ATS/ERS工作组商定的严重哮喘定义侧重于严重哮喘难治性或对现有药物(包括皮质类固醇)不敏感,以及哮喘并发合并症,这是两个社会主要服务的国家最关心的类型[9].
第三阶段:确定严重哮喘是否得到控制
在线补充资料3中介绍了不受控制哮喘标准的背景。以下四项标准中的任何一项都是哮喘不受控制的患者:1)症状控制不良;即。哮喘控制问卷(ACQ)持续≥1.5或哮喘控制测试(ACT) <20(或在3个月的评估中被国家哮喘教育和预防计划或全球哮喘倡议指南“控制不佳”[6,10]);2)频繁的严重加重,定义为前一年两次或两次以上系统性皮质类固醇爆发(每次≥3天);3)严重恶化,定义为过去一年至少一次住院、重症监护病房住院或机械通气;4)气流限制,即。用力呼气量在1秒(FEV1) <80%预测(存在FEV降低1/强制肺活量(FVC),定义为低于正常的下限),在暂停使用短期和长效支气管扩张剂后。
在目前的高剂量治疗中,有证据表明患者患有“严重哮喘”(表3).不符合哮喘不受控制标准,但在逐渐减少皮质类固醇后哮喘恶化的患者,也符合严重哮喘的定义。实现这一定义预示着来自疾病本身(加重和肺功能丧失)以及药物副作用的高度未来风险。
2.表型:流行病学、发病机制、病理生物学、结构和生理学
严重哮喘的表型和聚集
越来越明显的是,严重哮喘不是一种单一的疾病,其临床表现、生理特征和结局的多样性证明了这一点。为了更好地理解这种异质性,出现了哮喘表型的概念。表型被定义为一个生物体的复合的、可观察的特征,由其遗传组成和环境影响之间的相互作用产生,随着时间的推移,这些特征相对稳定,但不是不变的。表型整合了生物学和临床特征,从分子、细胞、形态学和功能到以患者为导向的特征,目的是改善治疗(图1).在这方面的详细努力需要将这些定义特征组织和整合到临床可识别的表型中。最终,这些表型应该演变成哮喘“内型”,将临床特征与可识别的机制途径结合起来。到目前为止,他们的身份充其量只是推测[11].一般来说,表型的时间稳定性将被要求提供其临床有用性的证据。这些严重哮喘表型的最终临床用途将由其治疗效果决定(见评估部分)。
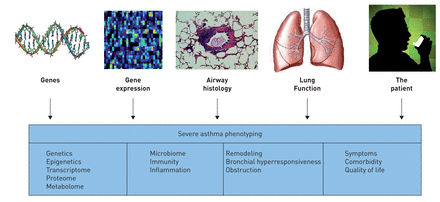
综合因素,从遗传学开始,这可能有助于严重哮喘患者的最终表型。
目前有两种描述表型的策略:基于假设的方法和无偏倚的方法。无偏分析应用于广泛的临床、生理和生物学特征,利用无监督分层聚类、逐步判别和其他方法[12- - - - - -15].严重哮喘研究计划(SARP)主要利用临床特征,在轻度、中度和重度哮喘的成年患者中确定了五类哮喘。他们包括三组轻度、中度和重度早发型特应性哮喘(基于肺功能范围、药物使用和发作频率),一组更严重的晚发型肥胖,主要是中度FEV的老年女性1减少和频繁使用口服皮质类固醇,以及发病较晚但持续时间较长的非常严重、特应性较轻、可逆性气流限制较少的组[15].莱斯特组的另一项成人哮喘队列分析包括痰中嗜酸性粒细胞计数,并确定了四个聚类,包括类似的早发型特应性哮喘、肥胖性非嗜酸性粒细胞性哮喘、早发型症状为主的哮喘和晚发型炎症为主的哮喘[14].在两组聚类分析中,重度哮喘患者分布在几个聚类中,支持重度哮喘的异质性。最后,一项针对儿童的SARP研究发现了四个聚类:1)晚发性肺功能正常,2)早发性特应性肺功能正常,3)早发性特应性轻度气流受限,以及4)早发性晚期气流受限[[16].
这三项研究通过较少偏倚的分析得出表型,尽管进入分析的数据不同,方法也不同。尽管SARP成人聚类分类主要与肺功能、发病年龄和治疗水平有关,但莱斯特聚类表明嗜酸性粒细胞表型可能在晚发型严重哮喘中更常见。有趣的是,这些无偏倚表型与先前临床确认的表型(晚发型嗜酸性粒细胞性和早发型特应性/过敏性)有大量重叠,特别支持这些表型的鉴定[17,18].
自然史和危险因素
对于严重哮喘在成人或儿童中的患病率了解甚少,特别是在使用本文概述的严格定义时。然而,通常估计的数字为哮喘总人数的5-10%。
估计这些数字的一些困难可能也是由于哮喘的异质性。严重哮喘及其表型的异质性,以及长期研究的缺乏,限制了我们对严重哮喘自然史的理解,包括严重哮喘是在疾病病程早期发展,还是随着时间的推移而发展。越来越多的证据表明,严重哮喘表型与遗传因素、哮喘发病年龄、病程、加重、鼻窦疾病和炎症特征有关[14,16,17,19- - - - - -21].儿童早期发作哮喘(严重程度不等)的特点是过敏致敏性、强烈的家族史以及最近的非过敏/特异反应相关遗传因素[14,17,22].晚发性严重哮喘通常与女性和肺功能下降有关,尽管疾病持续时间较短。在一些亚组中,它与持续性嗜酸性粒细胞炎症、鼻息肉和鼻窦炎有关,通常与阿司匹林敏感性(阿司匹林加重的呼吸道疾病)和呼吸道感染有关,但与特定遗传因素有关的情况较少[14,15,17,23,24].然而,在这些明显的晚发病例中,至少有一些可能在生命早期表现出气道生理异常的症状,但与严重哮喘发展的关系尚不清楚[25].
职业性暴露也与晚发性和通常严重的哮喘有关[26].肥胖与儿童期和成年期发作的严重哮喘都有关,但肥胖的影响可能因发病年龄和过敏性炎症程度而异[27,28].吸烟和环境空气污染通常被认为是更严重哮喘的危险因素[29,30.].个人吸烟和肥胖都与皮质类固醇不敏感有关,也与严重哮喘有关[31,32].成人严重哮喘在合并严重鼻窦疾病、胃食管反流、反复呼吸道感染和阻塞性睡眠呼吸暂停等共病的患者中更常出现反复发作[33].对真菌的敏感曲霉属真菌也与成人严重哮喘的发展有关[34,35].
遗传学和表观遗传学
在哮喘等复杂疾病中,遗传方法可以预测发展(易感性)或进展(严重程度)的风险。使用全基因组关联方法进行的综合遗传关联研究已经确定并复制了在确定哮喘易感性方面很重要的基因变异,而哮喘易感性通常基于医生对哮喘诊断的松散描述,而不是全面的临床特征[22,36].其他研究比较了较严重哮喘与非哮喘对照组或较小的轻度哮喘队列,并确定了相似的基因[20.].哮喘易感基因的差异似乎也因发病年龄而异,这是有偏表型和无偏表型方法的关键特征[22,37].了解这些基因变异的功能生物学可能有助于识别与表型和新的药物治疗相关的生物标志物。例如,白细胞介素(IL)-4受体-α中的单核苷酸多态性与持续性气道炎症、严重哮喘加重和粘膜下肥大细胞相关,这些细胞支持IL-4途径的功能改变,影响一些严重哮喘患者的过敏性炎症[19].另一篇最近的论文表明,IL-6受体的变化与肺功能降低和更严重的哮喘亚表型相关,这表明了另一个治疗靶点[38].最后,有证据表明,一些基因的遗传变异可能相互作用并影响肺功能、哮喘易感性和严重程度[39].另一种诱发更严重或更难治疗哮喘的机制可能与药物遗传学有关,在某些个体中,对哮喘治疗的反应性改变或降低。哮喘患者对控制疗法(如吸入糖皮质激素或甚至特定的新型生物疗法)的治疗反应性降低,可能表现出更难以控制的哮喘,并被归类为更严重的哮喘[40,41].
表观遗传变化源于DNA的非编码结构变化,如DNA甲基化或组蛋白的染色质结构改变,或来自小的非编码RNA, microRNA (miRNA)的影响。miRNAs在调节t辅助细胞(Th)2功能、随后的过敏性气道疾病和t细胞产生IL-13中的作用已从小鼠研究中提出[42,43].另一项研究报告了哮喘CD4和CD8 t细胞中特异性mirna的改变[44],但与严重哮喘的相关性仍有待确定。
炎症与适应性免疫
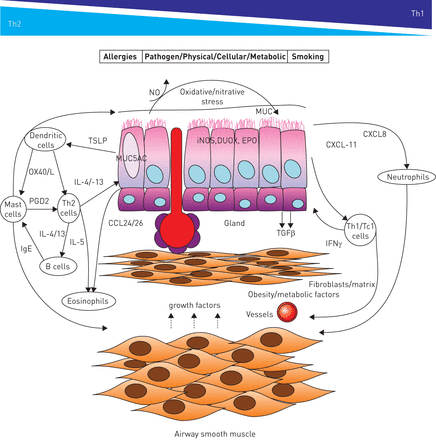
在严重哮喘患者中,通过列举吸入高渗盐水引起的痰中的炎症细胞,以及通过支气管活检和支气管肺泡灌洗来测量炎症。这种炎症可分为嗜酸性粒细胞性、嗜中性粒细胞性和/或少粒细胞性[14,18,45- - - - - -47].据报道,嗜酸性粒细胞和中性粒细胞(混合细胞)的同时存在与最严重的疾病有关[48].然而,在严重哮喘患者中,嗜酸性粒细胞和中性粒细胞痰液数量显示出广泛的变异性,尽管使用了高剂量的皮质类固醇,但这两种细胞的水平均为零或非常高[48- - - - - -50].痰液的嗜中性粒细胞和嗜酸性粒细胞成分每月可发生重大变化[51].然而,当对成年人进行较长时间的年度检查时,痰中嗜酸性粒细胞似乎更稳定,特别是在严重哮喘中[52].这种稳定性在儿童中似乎较少[53].这些不同炎症特征背后的机制可能是复杂的,多样的,并与皮质类固醇敏感性有关(图2) [54,55].例如,嗜酸性粒细胞炎症可能具有Th2免疫成分,这是适应性免疫的反映,四项独立的研究证明了IL-5单克隆抗体对成人嗜酸性粒细胞严重哮喘的疗效[14,56- - - - - -58].Th2谱是否与corticosteroid-naïve患者中观察到的Th2谱相似有待进一步研究,但抗il -13抗体在改善FEV方面的有效性将得到研究的支持1中度至重度哮喘成人患者[59,60].重度哮喘儿童Th2模式的证据仍存在争议[61,62].与Th2细胞因子高表达相关的炎症也与肥大细胞有关[63].哮喘患者气道平滑肌和上皮区室中的肥大细胞增加,它们与哮喘控制不良和气道高反应性有关[64,65].
潜在的免疫炎症和细胞相互作用有助于哮喘表型的发病机制。CXCL: CXC趋化因子配体;CCL24/26: CC趋化因子配体24/26;DUOX:双氧化酶;EPO:嗜酸性粒细胞过氧化物酶;干扰素γ干扰素-γ;IgE:免疫球蛋白E;IL:白介素;iNOS:诱导型一氧化氮合酶;MUC5AC:粘蛋白5AC; NO: nitric oxide; OX40/L: CD134 ligand; PGD2: prostaglandin D2; Tc1: cytotoxic T-cell type 1; TGFβ: transforming growth factor-β; Th1: T-helper cell type 1; Th2: T-helper cell type 2; TSLP: thymic stromal lymphopoietin.
气道中性粒细胞增多的机制尚不清楚。糖皮质激素本身可在一定程度上促进中性粒细胞增多,甚至Th1因子也可发挥作用[66,67].Th17免疫被认为是中性粒细胞增多的原因,主要是在哮喘小鼠模型中,有一些来自严重哮喘的支持数据[66,68- - - - - -70].
对于那些很少或没有炎症的患者发生严重哮喘的潜在机制仍然知之甚少,但可能涉及到平滑肌细胞、成纤维细胞和神经元等驻留细胞元素的激活。重要的是,虽然重点是通过分析痰样本来评估炎症,但其与气道/肺组织中细胞谱的关系尚不清楚,并且仍不清楚[55,71].
分子表型方法也正在出现,来自严重哮喘儿童的数据表明,与中度哮喘儿童相比,Th1偏斜,而最近对外周血细胞的转录组分析表明CD8的差异激活+t细胞与CD4细胞的比较+t细胞(44,62].在有固定气流限制的哮喘患者和慢性阻塞性肺病患者之间,呼出的挥发性有机化合物的模式也有所不同,这支持了他们在严重哮喘表型中的潜力[72,73].最后,呼出的一氧化氮分数(F伊诺)在轻度至中度哮喘方面进行了广泛的评估,ATS最近发布了具体的指南F伊诺在这些病人中使用[74].严重哮喘的横断面研究显示了一些潜在的有用性F伊诺作为症状频率的量度[75],并将其作为急诊最困难和最频繁使用者的索引[76].
呼吸道感染
感染,特别是病毒感染,在哮喘加重中的作用已得到证实,其对哮喘发展和进展的贡献也日益得到认识;然而,其与哮喘严重程度的关系很少被讨论。77- - - - - -79].葡萄球菌超抗原特异性IgE抗体与哮喘严重程度和鼻窦炎之间存在关联,而固定气流限制与细胞内病原体的血清学阳性相关,如衣原体肺炎[24,80,81].新出现的数据表明,通过16s rRNA测量,哮喘中的微生物组发生了改变,但细菌在严重哮喘中的作用需要进一步研究[82].积极的流感嗜血杆菌而且假单胞菌aeroginosa在没有支气管扩张证据的严重哮喘患者和过去一年哮喘持续时间长且病情加重的患者的痰样本中报告了培养[83].除了成人哮喘衣原体感染与肺功能的关系外,这些感染相关因素仅在横断面研究中进行了评估,对哮喘特征或表型的影响不大[24].
激活先天免疫途径
越来越多的证据表明涉及先天免疫途径,某些方面异常减弱,而其他方面可能增强。因此,据报道,巨噬细胞对凋亡上皮细胞或细菌的吞噬能力受损,这可能导致炎症增强[84,85].toll样受体信号也可能受损,导致I型和III型干扰素(IFN)反应不足,从而减少病毒清除[86].此外,当气道上皮细胞暴露于Th2细胞因子时,其抗菌活性及其β-防御素的产生降低,而过敏性炎症导致cathelicidin抗菌肽的减少[87,88].相反,先天性免疫的其他要素可能得到增强,包括严重哮喘患者气道细胞中胸腺基质淋巴生成素、IL-25和IL-33的表达增加[70,89,90].这些异常是否特定于某些表型有待进一步研究。
一些研究表明,在严重哮喘中,氧化应激和硝化应激也会增加。更高的F伊诺值,可能是由于在严重哮喘上皮细胞中较高的诱导型一氧化氮合酶表达,与严重哮喘更容易恶化的表型以及FEV更快速的下降有关1[76,91- - - - - -93].此外,较高水平的氧化应激与超氧化物歧化酶和s-亚硝基硫醇消耗的减少有关[94,95].
据报道,肿瘤坏死因子(TNF)-α的表达在严重哮喘气道中增加,最近的基因组和蛋白质组学方法表明,某些哮喘患者IL-1β与中性粒细胞增多有关[96- - - - - -98].虽然在严重哮喘中使用抗tnf -α抗体的试验提供了令人失望的结果,但有迹象表明,与晚发性可逆性疾病相关的某些表型可能反应更好[99].
最后,人们对缓解炎症的因素越来越感兴趣。因此,在严重哮喘中,可以想象,一些病理生物学与缺乏解决有关。在这方面,与轻度哮喘患者相比,重度哮喘患者体内脂素水平较低,而脂素具有潜在的抗炎作用[One hundred.- - - - - -102].
结构异常
常住的气道细胞,如上皮细胞、成纤维细胞和平滑肌细胞,越来越被认为是炎症和重塑的调节剂。结构改变可影响气道力学,而结构细胞也可通过释放细胞因子、趋化因子、生长因子和细胞外基质元素而促进炎症过程[103].首先,据报道,重度哮喘患者的上皮细胞比轻中度哮喘患者要厚[104],从而改变促炎因子的增殖、凋亡和释放[105].其次,尸检和活检研究已将气道平滑肌数量的增加与哮喘严重程度、气流阻塞和支气管高反应性联系起来[71,106- - - - - -109].最后,在患有固定气道阻塞和/或严重哮喘的哮喘患者的血液和平滑肌束中,可以分化为肌成纤维细胞的纤维细胞增加[110,111].
支气管网层上皮下增厚是儿童严重哮喘的早期特征,似乎是嗜酸性表型的一个特征[18,112,113].与轻度哮喘患者相比,重度哮喘患者转化生长因子-β异构体的表达和胶原沉积也增加,再次与嗜酸性哮喘有关,有证据表明外周气道也有重塑[18,114].事实上,小气道中细胞外基质的增加和成分的改变是致命哮喘的特征[114].
气道结构的高分辨率计算机断层扫描(HRCT)研究提供了严重哮喘成人气道和远端肺的定量形态测量,但对儿童的了解较少[115- - - - - -118].在成人中,这与肺功能和更严重的易加重疾病有关。这些结构变化导致通气缺陷,可以通过超极化氦磁共振成像来观察[119].初步研究表明,中性粒细胞性炎症可能与空气滞留有关,而活检测量的上皮厚度可预测HRCT扫描测量的气道壁厚度[116,117].
生理学
在一些严重哮喘表型中观察到慢性气流限制,对支气管扩张剂和吸入或口服皮质类固醇治疗反应较差[15,16,120].慢性气道阻塞可导致气道关闭或小气道通气不均匀,严重时可导致病情加重[121].发现严重哮喘患者表现出空气滞留(与FEV相关的FVC减少1/FVC),与FEV测量的气流限制水平相匹配的非严重哮喘患者进行比较1/植被覆盖度[122].低基线FEV患者使用支气管扩张剂1导致植被覆盖度显著增加,支持气道平滑肌在气流阻塞的空气捕获成分中的作用。最后,严重气道阻塞是一些严重哮喘表型的特征,研究表明嗜酸性粒细胞和/或嗜中性粒细胞炎症可能导致更大的气流限制[116,123,124].其中一组SARP以严重气道梗阻为特征,β-激动剂可持续可逆性,但未可逆性进入正常范围,并与痰中性粒细胞增多有关[15].重度哮喘患者肺功能的日常变化变化也较小[125].气道动态行为的降低表明,在严重哮喘中,不受控制的临床状态可能意味着比气道通畅的快速变化更固定和更严重的梗阻。
关于重度哮喘肺功能下降的前瞻性研究有限,但提示男性吸烟增加F伊诺和非洲血统是原因之一,而有趣的是,过敏状态可能是保护性的[93,126].
除了气道口径外,肺弹性后坐力也是最大气流的决定因素,也是防止气道关闭的力量。严重哮喘和支气管扩张后持续气流受限的患者肺弹性反冲减少,占其剩余气流受限的一部分[127].这是否与哮喘死亡病例中所报道的肺泡附着缺失有关,仍有待证实[128].
关于支气管高反应性的敏感性和最大反应的研究尚未被证明对严重哮喘有帮助,部分原因是在肺功能低的情况下难以测量。然而,可以从肺功能在数天内的波动模式中获得相关信息[125,129].使用来自物理学的新方法,对肺功能进行波动分析,每天两次,持续数周,可以为患者未来病情恶化的个体风险提供标记。这些波动对严重哮喘患者的影响尚不清楚,尽管与轻度至中度哮喘患者相比,波动的差异表明这些波动模式也可能是一种表型特征[130].
3.评价
本节着重于成人和儿童难以控制哮喘的评估。它将解决:1)确定“难治性哮喘”患者患有哮喘所需的评估,2)对混杂因素和共病的适当评估,3)对可能有助于优化治疗的表型的初步确定。
第一步:确定患者患有哮喘
临床医生应对诊断保持一定程度的怀疑,并确定患者的病史和评估是否真正代表哮喘。据报道,将非哮喘病症误诊为不受控制的哮喘的比例高达12-30% [131,132].评估应从详细的病史开始,重点关注哮喘症状,包括呼吸困难(与运动有关)、咳嗽、喘息、胸闷和夜间觉醒。此外,应获得有关加剧诱因的信息,以及可能造成影响的环境或职业因素。与肥胖相关的呼吸道症状也被误认为是哮喘,特别是当病人在紧急护理环境中出现时[133].应评估儿童和成人是否有其他可能类似哮喘或与哮喘有关的情况(表6).由于可逆性气流限制的确认是哮喘诊断的一部分,因此在使用支气管扩张剂前后应进行吸气和呼气循环的肺活量测定[134].为了最好地评估可逆性,需要适当停用药物。在肺功能相对保存的情况下,可以根据具体情况考虑进一步进行完整的肺功能测试,包括扩散能力测试和支气管刺激测试,如甲胆碱测试或运动挑战,特别是当病史、身体特征和肺活量测量之间存在不一致时。这应该提高对替代诊断的怀疑(在线补充资料3,表S1)。
确诊疑似哮喘的儿童是否有变异性气流阻塞是很重要的,但在实践中这是很困难的。患有严重哮喘的儿童通常肺功能正常,对支气管扩张剂无急性反应[135].FEV正常的儿童1在短效β-激动剂使用前和使用后,在强迫呼气流量为FVC (FEF)的25-75%方面,都可能表现出支气管扩张反应25 - 75%) [136].然而,FEF的效用25 - 75%在评估或治疗严重哮喘方面,目前尚不清楚。支气管刺激试验与运动或甲基胆碱支气管刺激可用于困难的病例。
转诊到专门的中心,病人可以在那里接受系统评估,结果导致30-50%以前被称为严重的病人,被归类为难以控制[131,137,138].许多患有哮喘的儿童在经过彻底的评估后,也会发现并没有严重的难治性哮喘[139]而且由于疾病管理不充分,约50%因严重哮喘转诊的儿童有持续症状和控制不佳[138].
问题1
对于有严重哮喘症状的患者(基于病史、症状和/或其他调查结果),在没有已知特定适应症的情况下,是否应该常规进行胸部HRCT扫描?
建议1
基于病史、症状和/或既往调查结果,对于没有特定适应症的严重哮喘儿童和成人,我们建议仅在表现不典型时进行胸部HRCT检查(有条件推荐,证据质量非常低)。
价值观和偏好
该建议相对重视替代诊断和合并症的识别,相对重视避免胸部HRCT潜在的并发症和费用。
讲话
严重哮喘的非典型表现包括以下因素,例如,难治性哮喘患儿粘液分泌过多,肺功能迅速下降,一氧化碳转移因子系数降低,无特异反应。
第二步:评估合并症和致病因素
难以控制的哮喘和严重的哮喘通常与同时存在的疾病有关(表7补充材料3,表S2)。所有难以控制的患者均应考虑不坚持治疗,因为报告显示不坚持治疗的比例可高达32-56% [131,137,140].不良的吸入器技术也很常见,应加以解决[138].检测不良的依从性可能具有挑战性。测量血清强的松龙、茶碱、全身皮质类固醇(CS)副作用和血清皮质醇水平的抑制可用于评估口服药物的依从性,但测量吸入CS依从性的方法,如罐重、压力驱动或电子计数器,在临床实践中并不广泛使用。确认病人曾从药房取过处方也可提供深入了解[140].如果存在不坚持用药的情况,临床医生应授权患者对药物做出知情选择,并制定个性化干预措施来管理不坚持用药[140].成本本身就会对依从性产生重大影响。
不良或不坚持治疗的有问题的儿童哮喘是特定的问题。青少年面临风险,因为他们对治疗的坚持程度降低,冒险行为(吸烟、非法使用药物)很常见,导致儿童哮喘致命发作的风险更高。治疗方案复杂、家庭不稳定、儿童监护不良以及与哮喘控制不良相关的潜在继发收益也可能导致依从性差。儿科哮喘的评估应包括在护士主导的家访期间检讨抢救吸入器及处方控制药物[138].提供者可能需要考虑在有监督的环境下给药,例如在学校。
长期以来,特异反应和过敏与哮喘有关,在某种程度上,与严重哮喘有关。然而,大多数大型流行病学研究报告称,与轻度哮喘相比,重度哮喘与特异反应/过敏的相关性较小,皮肤试验阳性的患者比例较低[120,141].过敏和哮喘严重程度之间的关联在儿童中更强[135,142].在所有患者中,确定特异性IgE(通过皮肤点刺试验或血清试验测量)、持续暴露和症状之间是否存在关联,可能有助于确定导致哮喘症状和恶化的因素[143].
据报道,鼻鼻窦炎的证据高达75-80% [141,144].鼻息肉见于一小部分成人。鼻息肉在哮喘患儿中不常见,常与囊性纤维化和原发性睫状体运动障碍有关。
胃食管反流(GOR)存在于60-80% [15,23,120,141,144],但抗反流疗法的临床试验通常显示对哮喘控制几乎没有影响[145- - - - - -147].一般来说,“沉默的”呼吸窘迫病(GORD)作为哮喘控制不佳的原因可能被过分强调,但有胃肠道症状和有问题的哮喘的儿童应该评估和治疗GORD [147].虽然治疗鼻窦炎和GORD对严重哮喘的影响尚不清楚,但当这些合并症存在时,应适当治疗以改善这些病情。GORD和鼻鼻窦炎均可加重声带功能障碍。此外,由GORD和鼻窦炎引起的症状可能伪装成哮喘。
肥胖也是难治性哮喘的常见共病,尽管肥胖与哮喘的关系可能因发病年龄而异,这对治疗有影响[27,28].
同时吸烟也会使哮喘更加难以控制。吸烟似乎改变了炎症过程,这可能导致他们对皮质类固醇治疗的反应较低[29,32].环境烟草烟雾暴露也与儿童和成人的不良哮喘结果有关[30.].尿液或唾液可替宁的测量通常可以揭示被动吸烟的证据[138].
患有严重哮喘的儿童早年接触各种过敏原并对其致敏,特别是对霉菌[135].支持重度哮喘对环境控制的治疗反应的证据不一致,研究也不充分,但在城市环境中,交通拥堵减少后环境臭氧水平的降低与哮喘预后的改善有关[148].需要进一步研究环境暴露作为严重哮喘的一个促成因素。
患有严重哮喘的成年人常出现焦虑和抑郁,比例为25%至49% [149].这些在孩子和他们的父母身上也很常见,母亲的抑郁和糟糕的应对技巧可能与哮喘相关的生活质量下降有关[150].这些情况通常诊断不足,因此建议进行适当的精神病学评估并转诊给专家。151].使用标准化问卷或直接访谈对家庭心理压力进行一些评估可能会有所帮助。不幸的是,精神病治疗对哮喘预后的益处尚未得到证实。151]最近的一项Cochrane元分析评估了成人和儿童的各种放松和行为技术的心理干预措施,但未能发现这些干预措施对哮喘结果的确切益处[152].
除了与哮喘相关的共病外,对于长期严重或难以控制的哮喘患者,应评估治疗诱导的共病,特别是当它们与高剂量吸入和全身使用皮质类固醇有关时(在线补充材料3,表S3)。
步骤3:哮喘表型的方法
哮喘,特别是严重哮喘,越来越多地被认为是异质的过程,并非所有的哮喘都可能对当前的治疗有相似的反应或具有相同的临床过程(见表型部分)。目前,还没有被广泛接受的特定哮喘表型的定义。然而,识别某些表型的某些特征可能最终促进有针对性和/或更有效的治疗,并有助于预测不同的自然史,这可能对一些患者有益[14,15].在这方面,嗜酸性粒细胞炎症、过敏/Th2过程和肥胖已被确定为特征或表型,这可能有助于考虑非特异性(皮质类固醇)和特异性(靶向)治疗(如。抗ige、抗il - 5及抗il - 13抗体治疗)[14,28,44,58,59,153- - - - - -156].
虽然尚未就具体的表型达成广泛共识,但临床、遗传学和统计学方法已经确定了一种具有不同自然历史的早发型过敏表型、晚发型肥胖(主要是女性)表型和晚发型嗜酸性粒细胞表型[14,15,17,22,27].哮喘的发病年龄,即。在儿童时期或成年时期开始与过敏、肺嗜酸性粒细胞和鼻窦疾病的差异有关。确定1)嗜酸性粒细胞性炎症或2)Th2炎症(或无Th2炎症)水平具有评估依从性/依从性水平、加重风险以及预测对皮质类固醇治疗的反应,以及可能对抗il -5或抗il -13等靶向治疗的反应的潜在益处[18,33,58,59,153- - - - - -155].痰中性粒细胞炎症在指导治疗中的作用通常研究较少,在严重哮喘患者中有相当大的日复一日的变化[51].它与皮质类固醇治疗反应降低有关[153].虽然这些测量方法在许多专门的中心都有,但在这些方法可以广泛使用之前,还需要进一步研究它们的效用以及方法的标准化。
类似地,与肥胖、早发性过敏性哮喘患者相比,成人发病的肥胖型哮喘患者对减肥策略的反应可能更好[28].这些特征可以通过询问发病年龄(尽管承认回顾性回忆的问题)、评估体重指数、测量肺嗜酸性粒细胞(通常在诱导痰中)和评估特异反应水平来解决,有或没有所谓的Th2炎症生物标志物。这些Th2标记包括F伊诺,以及血清骨膜蛋白(目前仅供研究使用,不适用于儿童),甚至血液嗜酸性粒细胞(详情见在线补充资料3,表S4和治疗部分)[59,157].在儿童中,外周嗜酸性粒细胞增多症的全血细胞计数或特异性(皮肤或血液测试)和总IgE测量可能有帮助,但特异性有限。F伊诺并不是所有患有慢性哮喘的儿童都升高了,但低水平表明有其他疾病,如囊性纤维化和睫状体运动障碍。
特异反应的生物标志物包括升高F伊诺和血清IgE能鉴别儿童严重哮喘,但不能鉴别成人严重哮喘,并支持普遍存在的th2驱动的气道炎症模式[135].然而,一项支气管镜研究并不支持Th2细胞因子在严重哮喘儿童中的决定性作用[61].此外,儿童严重哮喘的临床表现是高度可变的,不同的严重哮喘表型在儿童中比在成人中更不明确[16].虽然成人的痰液分析提示有各种炎症表型,但这种方法在儿童中信息较少,因为尚未确定稳定的主要痰液炎症表型[158].
除了血液嗜酸性粒细胞外,生物标志物测量需要专门的设备、培训或尚不容易获得的分析,并且需要确认任何这些生物标志物在识别临床意义和治疗上不同的哮喘表型方面的效用(见临床建议的治疗部分)。
4.治疗
本节讨论严重哮喘的管理,如本文件所定义的:1)已建立的治疗方法,2)最近开发的治疗方法和3)需要表型特征的未来方法。尽管它们被广泛使用和认可,但一些传统的控制药物,包括laba、白三烯调节剂和茶碱,在严重哮喘中的疗效还没有得到很好的记录。事实上,严重哮喘的定义本身的性质要求使用这些药物的混合组合治疗以保持控制或达到控制,这意味着这些治疗可能在该人群中疗效较低,前提是已经确定了治疗的依从性。直到最近,很少有临床试验专门用于研究严重哮喘患者的治疗方法,尽管这种情况现在正在迅速改变。新型分子靶向疗法的试验目前主要在成人重度哮喘人群中进行评估,有一些有效性的证据和短期安全性数据(表8).
使用现有的哮喘药物
皮质类固醇不敏感
根据本文的定义,严重哮喘包括皮质类固醇不敏感,在皮质类固醇治疗后仍持续缺乏控制,或在减少或停止皮质类固醇治疗后哮喘控制恶化。因此,尽管皮质类固醇是治疗轻度哮喘的主要手段,但在严重哮喘中可能需要替代的分子靶向治疗来调节炎症和改善皮质类固醇不敏感。严重哮喘常被称为皮质类固醇依赖、难治性或皮质类固醇不敏感哮喘。在30%的严重成人哮喘患者中,除了ICS外,还需要口服皮质类固醇(OCS)来维持一定程度的哮喘控制[23,120,124,141].肌注曲安奈德作为皮质类固醇治疗的最大剂量可改善哮喘控制,减少痰中嗜酸性粒细胞,增加FEV1[164,165],支持对这种治疗相对不敏感的存在,而不是完全抵抗。在一项针对儿童期难治性哮喘的研究中,102名患者中只有11%对曲安奈德单次肌内注射皮质类固醇“完全”无反应,这表明89%的患者对皮质类固醇有一定程度的反应[142].因此,术语皮质类固醇不敏感比皮质类固醇抵抗更合适。
皮质类固醇不敏感是可变的,可能有几个潜在的机制。它可以在外周血单个核细胞和肺泡巨噬细胞中得到证明,也可以在严重哮喘患者的气道平滑肌细胞等驻留细胞中得到证明[166- - - - - -169],而是它们之间的关系在体外研究在活的有机体内反应不是很好理解。皮质类固醇不敏感与不同的共病有关,如肥胖[170]、吸烟[171],维生素D水平低[172,173],非嗜酸粒细胞性(低th2炎症)主要发生于成人[174].在儿童中,人们对这些机制的作用知之甚少。
虽然嗜酸性或“Th2高”哮喘表型的特征是Th2细胞因子、IL-5和IL-13的高表达,确定了轻度哮喘患者的ICS反应性,但嗜酸性炎症可能在一些严重哮喘患者中持续存在,尽管高剂量ICS,甚至全身皮质类固醇[18,61,141,155,175,176].与成人严重哮喘相似,在儿童中观察到嗜酸性粒细胞为主的特征,但与支气管肺泡灌洗液或活检中可测量的Th2细胞因子水平无关[61].在成人中,非嗜酸性表型似乎形成了哮喘的一个大亚群[18,175,176],数据来自轻度至中度人群[176]表现出相对较差的皮质类固醇敏感性。了解这些不同类型皮质类固醇不敏感的机制可能会导致新的治疗方法,如p38丝裂原活化蛋白激酶抑制剂和组蛋白去乙酰化酶-2受体[177,178].
在20世纪90年代,一些具有免疫抑制特性的药物,如甲氨蝶呤,环孢素A,金盐和注射。研究了IgG作为皮质类固醇保留剂,目的是减少维持性OCS的剂量。虽然这些药物可被认为可改善皮质类固醇不敏感,但其疗效尚不确定,且与显著的副作用相关(见下面的GRADE问题)[179- - - - - -183].
吸入和口服皮质类固醇治疗
单个ICSs的高剂量范围示于表4.这些剂量高于在轻度哮喘中达到最大治疗效果所需的通常剂量。在中度哮喘中,将ICS剂量增加到中度以上几乎没有反应[184].然而,ICS的剂量治疗效果存在个体差异,一些证据表明较高的ICS剂量可能对严重哮喘更有效(包括系统性皮质激素保留效应)[184,185].虽然更高剂量的ICS(高于2000 μg·日−1(相当于倍氯米松当量剂量)和超细颗粒ICS通常用于重度哮喘,但支持这种方法的数据很少。
据报道,使用高剂量ICS可有效治疗轻至中度哮喘的哮喘加重,通常是维持剂量的四倍(相当于2400-4000 μg倍氯米松)。然而,对于严重哮喘患者来说,这通常是不现实的,因为这些患者已经维持了高剂量的ICS [186,187].因此,在标准药物不足的情况下,重度哮喘患者通常会加入OCSs作为维持治疗。
现时约有三分之一的SARP队列接受定期的OCS治疗,而超过半数的患者在上一年需要三次以上的OCS治疗[21,120,124,141].开始OCS治疗的最佳时间也尚未确定。同样,目前尚不清楚连续的低剂量OCS是否比多次不连续的发作更好地控制病情加重。虽然已经提出了使用生物标志物指导皮质类固醇使用的指南,但使用痰中嗜酸性粒细胞和/或呼出一氧化氮水平指导严重哮喘的治疗仍然存在争议[74)(见下面的GRADE问题)。
曲安奈德肌内治疗已用于严重哮喘,据报道改善嗜酸性粒细胞炎症和气流阻塞,并预防病情加重[164,165].其疗效的原因可能包括强制坚持或与临床使用的其他皮质类固醇相比,曲安奈德的效力更强。
全身使用皮质类固醇与骨折和白内障风险增加有关[188,189],而高剂量的ICS与儿童肾上腺抑制和生长迟缓的风险增加有关[188,190- - - - - -192].系统性皮质激素相关体重增加可能进一步对哮喘控制产生负面影响[193].在青春期前儿童中,最初每天使用400 μg布地奈德可导致初始身高小幅下降(平均为-1.3 cm),并伴随成年身高的持续下降,尽管这种下降既不是渐进性的,也不是累积性的[194].因此,使用持续的全身皮质类固醇,也许在较小程度上使用高剂量ICS,应该伴随着谨慎的体重、血压、血糖、眼睛和骨密度监测,以及儿童的适当生长。应根据指引采取预防骨密度减低的措施[195].
ICS与儿童肾上腺抑制风险增加有关。剂量阈值显示个体差异,目前尚不清楚潜在哮喘的严重程度是否会像成人那样影响氟替卡松的全身吸收[196].应尽一切努力尽量减少全身吸收,例如对ICS使用大体积间隔剂。目前还没有关于监测严重哮喘儿童肾上腺功能的循证指南,但由于根据定义,他们将接受高剂量的ICS,每年进行肾上腺功能测试,如皮质醇刺激测试,甚至由儿科内分泌学家进行评估可能会有所帮助。这样的孩子可能会从携带类固醇警告卡中受益,并且在压力大的时候可能需要全身使用皮质类固醇,例如在同时进行手术期间。
短期和长效β-肾上腺素能支气管扩张剂
许多患有严重哮喘的成人和儿童患者尽管使用ICS和短期和/或长效支气管扩张剂治疗,但仍有持续的慢性气流阻塞[23,124].与单独使用ICS相比,逐步增加ICS剂量并联合LABA可改善控制前景,包括在一些严重哮喘患者中。此外,一些未能实现症状最佳控制的患者在临床控制的某些特征上有所改善,达到更令人满意或可容忍的状态,即使他们的综合控制评分(如ACQ-7或ACT)仍处于无法控制的水平[185,197].在低剂量ICS控制不良的儿童哮喘中,与加倍剂量ICS或添加孟鲁司特相比,添加laba是ICS最有效的附加治疗,但治疗反应存在显著差异,突出表明需要定期监测和适当调整每个儿童的哮喘治疗[198].目前还没有关于严重儿科哮喘的研究报道。
在快速发作严重加重的哮喘患者(通常被标记为“脆性”哮喘),皮下给药β-激动剂特布他林已被使用,但其优于重复或连续吸入(雾化或雾化给药)β-激动剂尚未得到证实[199].
增加β-激动剂的使用可能矛盾地导致哮喘控制恶化,正如在使用短效β-激动剂(SABAs)或不含ICS的LABAs治疗的轻中度哮喘患者中所描述的那样[200- - - - - -203].严重哮喘患者也可以接受laba和必要的saba。吸入性β-激动剂的使用与哮喘死亡率之间有很强的相关性,据报道主要局限于β-激动剂的使用超过推荐限度[204].
对β-激动剂反应的种族差异也有报道。因此,与墨西哥裔美国人和波多黎各人相比,即使在ICS治疗后,非洲种族背景的个体对SABA的短效支气管扩张剂反应似乎更少[205].据报道,与美国白人相比,患有哮喘的非洲裔美国人治疗失败的次数更多,特别是在参加LABAs时[206].目前正在进行的研究着眼于种族和β-肾上腺素受体基因型对β-肾上腺素受体治疗反应性的影响。
过度使用β-激动剂是否会导致哮喘控制恶化尚不确定,但这些患者可能存在β-激动剂毒性的增加风险。在临床实践中,成人和儿童严重哮喘的剂量和治疗时间经常超过专家指南建议的剂量,因此很难确定“安全”的上限剂量。病例报告显示,在一些服用过量β-激动剂的严重成年哮喘患者在医学监督下减少β-激动剂后,“哮喘控制有所改善”[207].laba的一般安全问题适用于儿童和成人,在超过推荐剂量时应谨慎。使用β-激动剂对儿童没有特别的担忧。对于患有哮喘的儿童,无论其严重程度如何,没有证据表明减少laba的剂量可以改善哮喘控制。
使用异丙托溴铵气雾剂缓解症状通常用于严重哮喘患者,试图减少他们日常使用或过度使用β-激动剂,特别是在那些表现出β-激动剂不耐受副作用的患者,如震颤和心悸,以及在哮喘加重的治疗中[208,209].虽然被认为效果较差,但耐受性良好,可与β-激动剂交替使用,根据需要全天使用。不鼓励常规使用雾化雾化器,因为其给药效率相对较低,而且使用雾化雾化器与严重哮喘患者的死亡有关,这被认为是由于依赖雾化雾化器的使用以及在恶化期间延迟寻求帮助造成的[210].对于哮喘恶化或哮喘加重的成人和儿童,使用带间隔的加压计量吸入器已证明与雾化吸入器一样有效[211].
缓释茶碱
在中度哮喘患者中,茶碱加入ICS后可改善哮喘控制[212].在一项对皮质类固醇不敏感的吸烟哮喘患者的探索性研究中,茶碱与低剂量ICS可改善呼气流量峰值率和哮喘控制[213,这就增加了茶碱可以改善某些人皮质类固醇不敏感的可能性。然而,目前还没有对患有严重哮喘的儿童或成人进行此类研究[214].鉴于低剂量茶碱的安全性,在其他治疗方法之前,它已被用于严重哮喘儿童。
白三烯途径修饰剂
在ICS治疗中加入孟鲁司特在预防需要全身糖皮质激素的急性发作或改善中度哮喘症状方面不如laba有效[4,198].在三项对未服用laba的中度至重度哮喘患者的研究中,加入白三烯受体拮抗剂或合成抑制剂对肺功能有一定疗效。其中两项研究是在阿司匹林敏感性哮喘中进行的,其中35%的患者使用了全身皮质类固醇[215- - - - - -217].相比之下,在一项对72名接受LABA和ICS的非表型重度成年哮喘患者(其中一些人同时接受OCS)的研究中,孟鲁司特在14天内并没有改善临床结果[218].有阿司匹林敏感性哮喘表型的个体是否比没有阿司匹林敏感性哮喘的个体反应更好还没有正式的研究。目前还没有关于这些药物在患有严重哮喘的儿童中的具体研究。
针对严重哮喘的具体方法
委员会确定了几个临床问题,这些问题对临床医生管理严重哮喘患者很重要。这些问题都列在网上的补充资料中。对于这份初始文件,委员会选择评估两个关于严重哮喘表型管理的问题和五个关于成人和儿童治疗方法的问题。评估的前两种管理方法是生物标志物的实用使用来指导治疗,即痰嗜酸性粒细胞增多症和/或F伊诺.评估的治疗方案是使用抗ige治疗,甲氨蝶呤作为类固醇保留剂,使用大环内酯治疗,抗真菌治疗的作用,以及较新的支气管热成形术治疗。
目前可用于指导治疗的生物标志物问题2
重症哮喘患者是否应该以痰嗜酸性粒细胞计数为指导,而不是仅以临床标准为指导?
建议2
对于患有严重哮喘的成年人,我们建议以临床标准和在有经验使用该技术的中心进行的痰嗜酸性粒细胞计数为指导进行治疗,而不是仅根据临床标准(有条件推荐,证据质量非常低)。
对于患有严重哮喘的儿童,我们建议仅以临床标准为指导,而不是以临床标准和痰嗜酸性粒细胞计数为指导(有条件推荐,证据质量非常低)。
价值观和偏好
使用痰中嗜酸性粒细胞计数来指导成人治疗的建议,更重视在特定患者中调整治疗可能带来的临床益处,并避免不适当的治疗升级,而更不重视增加资源的使用。
不使用痰嗜酸性粒细胞计数来指导儿童治疗的建议,更重视避免不标准化和不广泛使用的干预,而更重视不确定和可能有限的临床效益。
讲话
因为目前,痰中嗜酸性粒细胞的测量还没有充分标准化,也没有广泛使用,我们建议这种方法只在有这种技术经验的专业中心使用。可能从这种方法中受益的患者是那些可以产生痰,表现出持续性或至少间歇性嗜酸性粒细胞增多,并患有严重哮喘并频繁恶化的患者。临床医生应该认识到,不同的病人有不同的选择。
问题3
治疗是否应该以F伊诺除临床标准外,而不是仅以临床标准为指导的治疗,是否适用于重度哮喘患者?
建议3
我们建议临床医生不要使用F伊诺指导成人或儿童严重哮喘的治疗(有条件推荐,证据质量很低)。
价值观和偏好
该建议高度重视避免额外的资源支出,而不重视监测的不确定收益F伊诺.
治疗方法问题4
单克隆抗ige抗体是否适用于严重过敏性哮喘患者?
推荐4
对于严重过敏性哮喘患者,我们建议在成人(有条件推荐,证据质量低)和儿童(有条件推荐,证据质量非常低)中进行omalizumab治疗试验。
价值观和偏好
这一建议认为,奥玛珠单抗在一些严重过敏性哮喘患者中的临床益处具有更高的价值,而增加资源使用的价值则较低。
讲话
考虑进行omalizumab试验的成人和儿童(≥6岁)严重哮喘患者,如果他们的血清总IgE水平为30-700 IU·mL,尽管进行了最佳的药物和非药物管理,并适当避免了过敏原,但仍应证实IgE依赖性过敏性哮喘未得到控制−1(在三项研究中,其范围更大,为30-1300 IU·mL−1).治疗反应应由治疗医师全面评估,同时考虑哮喘控制的改善、急性发作和非计划医疗保健利用的减少以及生活质量的改善。如果患者在开始治疗的4个月内没有反应,则进一步给予omalizumab不太可能有益。
问题5
甲氨蝶呤是否应用于治疗严重哮喘?
建议5
我们建议临床医生不要在患有严重哮喘的成人或儿童中使用甲氨蝶呤(有条件推荐,证据质量低)。
价值观和偏好
这一建议相对较高地重视避免甲氨蝶呤的不良反应,而相对较低地重视减少全身皮质类固醇剂量的可能益处。
讲话
来自随机试验的证据仅适用于成年人。由于甲氨蝶呤可能的不良反应和监测治疗的需要,我们建议甲氨蝶呤的任何使用仅限于专门的中心和仅在需要每日OCS的患者。如果决定使用甲氨蝶呤,胸片,全血计数和血小板,肝功能检查,血清肌酐和DLCO,建议在开始治疗之前和之后。
问题6
严重哮喘患者是否应使用大环内酯类抗生素?
推荐6
我们建议临床医生不要在患有严重哮喘的成人和儿童中使用大环内酯类抗生素治疗哮喘(有条件推荐,证据质量非常低)。
价值观和偏好
该建议对预防大环内酯类抗生素产生耐药的重视程度相对较高,对临床疗效不确定的重视程度相对较低。
讲话
这一建议仅适用于哮喘的治疗;它不适用于大环内酯类抗生素的其他适应症,如.治疗支气管炎、鼻窦炎或其他细菌感染。
问题7
严重哮喘患者应该使用抗真菌药物吗?
建议7
我们建议重度哮喘和过敏性支气管肺曲菌病(ABPA)复发的成人使用抗真菌药物(有条件推荐,证据质量很低)。
我们建议临床医生不要使用抗真菌药物治疗没有ABPA的成人和儿童严重哮喘患者的哮喘,无论对真菌是否敏感(即。皮肤点刺试验或血清真菌特异性IgE阳性)(有条件推荐,证据质量很低)。
价值观和偏好
对于严重哮喘和ABPA患者使用抗真菌药物的建议,更高的价值在于可能减少加重风险和改善症状,而更低的价值在于避免可能的不良反应、药物相互作用和增加资源的使用。
对于没有确定ABPA的严重哮喘患者(无论是否致敏),不建议使用抗真菌药物,这一建议高度重视避免可能的不良反应、抗真菌药物与其他药物的相互作用以及增加资源的使用,而不太重视不确定的可能益处。
讲话
对于没有证实ABPA的严重哮喘患者不使用抗真菌药物的建议仅适用于哮喘的治疗;它不适用于抗真菌药物的其他适应症,如.侵袭性真菌感染的治疗。在儿童方面,证据仅限于孤立的病例报告。只有在重症哮喘专科转诊中心进行最详细的评估后,儿童才应使用抗真菌药物治疗。由于抗真菌疗法与显著且有时严重的副作用相关,包括肝毒性,临床医生应熟悉这些药物,并遵循相关预防措施监测这些药物,观察每种药物推荐的治疗时间限制。
问题8
支气管热成形术是否适用于严重哮喘患者?
推荐8
我们建议仅在经机构审查委员会批准的独立系统注册或临床研究的情况下,对患有严重哮喘的成年人实施支气管热成形术(强烈建议,证据质量非常低)。
价值观和偏好
这一建议高度重视避免不良反应和增加资源使用,以及缺乏对哪些患者可能受益的了解,而不太重视症状和生活质量的不确定改善。
讲话
这是一个强烈的建议,因为目前对严重哮喘患者支气管热成形术效果的估计可信度很低。潜在的好处和危害都可能很大,这种利用侵入性物理干预的哮喘治疗新方法的长期后果尚不清楚。需要专门设计的研究来确定其对相关客观主要结局(如加重率)的影响,以及对肺功能的长期影响。还需要进行研究以更好地了解响应患者的表型,其对严重阻塞性哮喘(FEV)患者的影响1<预测值的60%)或全身性使用皮质类固醇的患者,及其长期益处和安全性。进一步的研究可能会对这一建议产生重要影响。
新的实验性分子治疗严重哮喘
慢性严重哮喘具有不同的潜在机制(或内型),其复杂性表明,对严重哮喘患者进行表型分析和个性化治疗可以改善预后,减少副作用。针对严重哮喘的抗ige疗法的引入开启了针对某些严重哮喘患者的特定疗法时代,尽管预测治疗的反应仍然存在问题。最近针对特定哮喘炎症途径的实验生物学方法已报道了积极的结果,并开始帮助定义免疫炎症表型/内型(表8而且9).
虽然抗il5抗体mepolizumab对未选择的中度哮喘成年患者没有益处[222],在对持续性痰嗜酸性粒细胞增多的严重哮喘患者进行研究时,两种抗il -5抗体mepolizumab和reslizumab已被证明可以减少急性发作和OCS的使用,并在不同程度上改善症状和肺功能[57,58,157].一项更大规模的mepolizumab研究显示,mepolizumab在成人和青少年中的疗效仅在降低恶化率方面,而没有改善FEV1以及生活质量[56].
IL-13抗体lebrikizumab改善FEV1在不影响哮喘加重和哮喘症状的情况下[59].在事后分析中,该抗体改善了支气管扩张剂前FEV1在有Th2炎症证据的组中,通过血清骨膜蛋白水平升高来测量,这是Th2活性的替代标记或F伊诺[59,223].另一种抗il -13抗体tralokinumab没有改善症状,但导致FEV无显著增加1与安慰剂相比。与lebrikizumab一样,它似乎在痰中IL-13水平可检测的患者中表现更好[60].一项针对IL-4受体-α的单克隆抗体(阻断IL-4和IL-13)在中重度哮喘中的研究结果为阴性[160].目前尚不清楚先前的生物表型是否会产生不同的结果。同样,一种抗tnf -α抗体golimumab在一项针对成人严重持续性哮喘患者的研究中也无效[99),但事后分析表明在一个亚组中有影响。然而,由于严重的副作用,包括治疗组感染流行率的增加,进一步的研究不太可能。
其他两种生物学方法已报道用于严重哮喘,但没有任何特定的表型适合所选目标。与安慰剂相比,酪氨酸激酶抑制剂马西替尼(masitinib)靶向干细胞因子受体和血小板衍生生长因子,在面对减少剂量的OCS时改善了成人哮喘控制;然而,对肺功能没有影响[161].Daclizumab是一种针对活化淋巴细胞IL-2受体α链的人源IgG1单克隆抗体,改善了FEV1对ICS控制不足的中重度哮喘患者的哮喘控制[162].CXCR2拮抗剂SCH527123可减少严重成人哮喘患者的痰中性粒细胞增多,并与轻度加重的适度减少有关,但对哮喘控制没有改善[163].由于痰中性粒细胞的定义仍不令人满意,目前尚不清楚是否会有更好的疗效。除了omalizumab之外,目前尚无在儿童中使用单克隆抗体治疗的经验。成人研究的数据只能非常谨慎地外推到儿童身上。
结论
成人和儿童严重哮喘的治疗仍然严重依赖于皮质类固醇和支气管扩张剂的最大优化使用,以及推荐用于中重度哮喘的其他控制药物。首个被批准用于哮喘的靶向生物治疗方法——单克隆抗ige抗体的加入,使人们对一些过敏性严重哮喘患者的预后改善再次感到乐观。在重度哮喘治疗中,其他生物制剂有可能带来其他附加好处,特别是如果可以识别和选择适当的响应者特异性表型的患者进行这些高度特异性的治疗。这一前景为研究严重哮喘的机制、途径和生物标志物提供了动力。希望目前对严重哮喘的免疫病理、生物制剂和新出现的炎症和分子表型的新认识将产生并导致安全有效的生物标志物驱动的治疗严重哮喘的方法。
脚注
由于2014年4月,2018年7月和2022年6月发表的更正欧洲呼吸杂志,这篇文章的在线版本进行了修改。
有关编辑评论,请参阅315页.
这篇文章有补充资料可从www.www.qdcxjkg.com
利益冲突:可以在本文的在线版本中找到信息披露www.www.qdcxjkg.com
- 收到了2013年11月19日。
- 接受2013年11月26日。
- ©2014人队
参考文献
- ↵
- ↵
- ↵
- ↵
-
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵